Trắc nghiệm Hóa học 10 Bài 15. Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng có đáp án
Trắc nghiệm Hóa học 10 Bài 15. Phương trình tốc độ phản ứng và hằng số tốc độ phản ứng có đáp án
-
659 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Tốc độ phản ứng của một phản ứng hóa học là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Tốc độ phản ứng của một phản ứng hóa học là đại lượng đặc trưng cho sự biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian.
Câu 2:
Kí hiệu và đơn vị của tốc độ phản ứng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Tốc độ phản ứng kí hiệu là 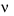 , đơn vị là (đơn vị nồng độ) / đơn vị thời gian.
, đơn vị là (đơn vị nồng độ) / đơn vị thời gian.
Câu 3:
Biểu thức tốc độ trung bình của phản ứng: aA + bB ⟶ cC + dD là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Biểu thức tốc độ trung bình của phản ứng: aA + bB ⟶ cC + dD là
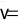
 .
.
Trong đó:
 là tốc độ trung bình của phản ứng.
là tốc độ trung bình của phản ứng.
 là sự biến thiên nồng độ.
là sự biến thiên nồng độ.
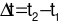 là biến thiên thời gian.
là biến thiên thời gian.
C1, C2 là nồng độ của một chất tại hai thời điểm tương ứng t1, t2.
Câu 4:
Cho phản ứng ở 45°C
2N2O5 (g) ⟶ O2 (g) + 2N2O4 (g)
Sau 275 giây đầu tiên, nồng độ của O2 là 0,188 M. Tính tốc độ trung bình của phản ứng theo O2 trong khoảng thời gian trên.
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Vì O2 là sản phẩm nên nồng độ tại thời điểm ban đầu của O2 bằng 0, do đó: 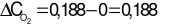 (M)
(M)
Theo bài ta có:
 =
= 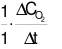 =
= 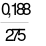 ≈ 6,8.10−4 (M / giây).
≈ 6,8.10−4 (M / giây).
Câu 5:
Cho phản ứng:
2N2O5 (g) ⟶ O2 (g) + 4NO2 (g)
Sau thời gian từ giây 57 đến giây 116, nồng độ N2O5 giảm từ 0,4 M về 0,35 M. Tốc độ trung bình của phản ứng trong khoảng thời gian trên là
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Tốc độ trung bình của phản ứng trong khoảng thời gian từ giây 57 đến giây 116 là:
 =
= 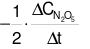 =
= 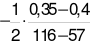 ≈ 4,24.10−4 (M / giây).
≈ 4,24.10−4 (M / giây).
Câu 6:
Cho phản ứng đơn giản có dạng: aA + bB ⟶ cC + dD
Mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Cho phản ứng đơn giản có dạng: aA + bB ⟶ cC + dD
Theo định luật tác dụng khối lượng, mối quan hệ giữa nồng độ và tốc độ tức thời của phản ứng hóa học được biểu diễn bằng biểu thức  =
= 
Trong đó, k là hằng số tốc độ phản ứng; CA, CB là nồng độ (M) chất A, chất B tại thời điểm đang xét.
Câu 7:
Cho phản ứng: 2SO2 (g) + O2 (g) 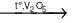 2SO3 (g)
2SO3 (g)
Biểu thức tốc độ thức thời của phản ứng theo định luật tác dụng khối lượng là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Phản ứng: 2SO2 (g) + O2 (g) 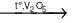 2SO3 (g)
2SO3 (g)
Biểu thức tốc độ thức thời của phản ứng theo định luật tác dụng khối lượng là:
 =
= 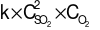
Câu 8:
Hằng số tốc độ phản ứng k chỉ phụ thuộc vào
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Hằng số tốc độ phản ứng k chỉ phụ thuộc vào bản chất của phản ứng và nhiệt độ.
Câu 9:
Hằng số tốc độ phản ứng k bằng vận tốc tức thời 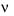 khi
khi
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Hằng số tốc độ phản ứng k bằng vận tốc tức thời 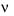 khi nồng độ chất phản ứng bằng đơn vị (1 M), khi đó k là tốc độ phản ứng và được gọi là tốc độ riêng.
khi nồng độ chất phản ứng bằng đơn vị (1 M), khi đó k là tốc độ phản ứng và được gọi là tốc độ riêng.
Câu 10:
Cho phản ứng đơn giản xảy ra trong bình kín: 2CO (g) + O2 (g) ⟶ 2CO2 (g).
Tốc độ phản ứng thay đổi như thế nào nếu tăng nồng độ CO gấp 2 lần, nồng độ O2 không đổi.
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Theo định luật tác dụng khối lượng, tốc độ tức thời của phản ứng là: 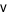 =
= 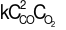
Nếu tăng nồng độ CO gấp 2 lần, ta có:  =
= 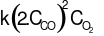 =
= 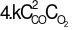 =
= 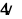
Vậy tốc độ phản ứng tăng gấp 4 lần.
Câu 11:
Cho phản ứng đơn giản xảy ra trong bình kín: 3H2(g) + N2 (g) ⟶ 2NH3 (g).
Tốc độ phản ứng thay đổi như thế nào nếu nồng độ H2 và N2 đều tăng 3 lần.
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Theo định luật tác dụng khối lượng, tốc độ tức thời của phản ứng là: 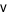 =
= 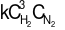
Nếu nồng độ H2 và N2 đều tăng lên 3 lần, ta có:  =
= 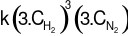 =
= 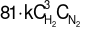
= 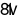
Vậy tốc độ phản ứng tăng 81 lần.
Câu 12:
Cho phản ứng đơn giản xảy ra trong bình kín: H2(g) + Cl2 (g) ⟶ 2HCl (g).
Tốc độ phản ứng thay đổi như thế nào nếu nồng độ H2 giảm 4 lần và nồng độ Cl2 tăng 2 lần.
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Theo định luật tác dụng khối lượng, tốc độ tức thời của phản ứng là: 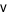 =
= 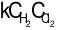
Nếu nồng độ H2 giảm 4 lần và nồng độ Cl2 tăng 2 lần, ta có:  =
= 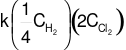 =
= 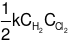 =
= 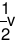
Vậy tốc độ phản ứng giảm 2 lần.
Câu 13:
Cho phản ứng: Br2 (l) + HCOOH (aq) 2HBr (aq) + CO2 (s)
Nồng độ ban đầu của Br2 là aM, sau 50 giây nồng độ Br2 còn lại là 0,02M. Tốc độ trung bình của phản ứng trên là 4.10-5M/s. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án đúng là:
Áp dụng công thức tính tốc độ trung bình của phản ứng, ta có:
 =
= 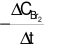
Do đó 4.10-5 = 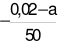 ⇒ a = 0,022 (M)
⇒ a = 0,022 (M)
Câu 14:
Cho phản ứng: 2H2O2 (aq) O2 (s) +2H2O (l)
O2 (s) +2H2O (l)
Cho chất xúc tác MnO2 vào 100 ml dung dịch H2O2, sau 60 giây thu được 33,6 ml khí O2 (ở đktc). Tốc độ trung bình của phản ứng (tính theo H2O2) trong 60 giây trên là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Ta có: 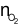 =
= 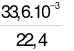 = 1,5.10−3 (mol)
= 1,5.10−3 (mol)
Theo phương trình: 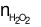 phản ứng = 2
phản ứng = 2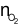 = 2. 1,5.10−3 = 3.10−3 (mol)
= 2. 1,5.10−3 = 3.10−3 (mol)
 phản ứng =
phản ứng = 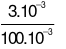 = 0,03 (M)
= 0,03 (M)
Mà  phản ứng =
phản ứng =  (bđ) −
(bđ) −  (sau 60 giây) =
(sau 60 giây) = 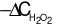
Do đó:  = − 0,03 (M)
= − 0,03 (M)
Tốc độ trung bình của phản ứng (tính theo H2O2) trong 60 giây trên là
 =
=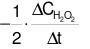 =
= 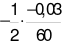 = 2,5.10−4 (M/s)
= 2,5.10−4 (M/s)
Câu 15:
Hiện tượng nào dưới đây xảy ra với tốc độ nhanh nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Hiện tượng xảy ra với tốc độ nhanh nhất là đốt gas khi nấu ăn.
