15 câu trắc nghiệm Lưu huỳnh cực hay (có đáp án)
-
867 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Nguyên tố lưu huỳnh có số hiệu nguyên tử là 16. Vị trí của lưu huỳnh trong bảng tuần hoàn các nguyên tố hóa học là
 Xem đáp án
Xem đáp án
Đáp án A
Cấu hình electron nguyên tử S là: 1s22s22p63s23p4.
→ Lưu huỳnh ở chu kỳ 3 (do có 3 lớp electron); nhóm VIA (do có 6 electron hóa trị, nguyên tố p).
Câu 2:
Cho các phản ứng hóa học sau:
(a)
(b)
(c)
(d)
Trong các phản ứng trên, số phản ứng trong đó S thể hiện tính khử là
 Xem đáp án
Xem đáp án
Đáp án A
Lưu huỳnh thể hiện tính khử khi tác dụng với phi kim mạnh như: F2; Cl2; O2 ... và các hợp chất có tính oxi hóa mạnh như: HNO3; H2SO4 đặc …
→ Các phản ứng trong đó S thể hiện tính khử là:
Câu 3:
Hơi thủy ngân rất dộc, bởi vậy khi làm vỡ nhiệt kế thủy ngân thì chất bột được dùng để rắc lên thủy ngân rồi gom lại là
 Xem đáp án
Xem đáp án
Đáp án D
Thủy ngân phản ứng với lưu huỳnh ở ngay điều kiện thường.
Hg + S → HgS
Câu 4:
Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hóa trong phản ứng nào sau đây
 Xem đáp án
Xem đáp án
Đáp án A
Câu 5:
Đun nóng 4,8 gam bột Mg với 9,6 gam bột lưu huỳnh (trong điều kiện không có không khí), thu được chất rắn X. Cho toàn bộ X vào lượng dư dung dịch HCl, thu được V lít khí (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 6:
Cho 11 gam hỗn hợp bột sắt và bột nhôm tác dụng với bột lưu huỳnh (trong điều kiện không có không khí) thấy có 12,8 gam lưu huỳnh tham gia phản ứng. Khối lượng sắt có trong 11 gam hỗn hợp đầu là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 7:
Trong 5,6 gam bột sắt với 2,4 gam bột lưu huỳnh rồi nung nóng (trong điều kiện không có không khí), thu được hỗn hợp rắn M. Cho M tác dụng với lượng dư dung dịch HCl, giải phóng hỗn hợp khí X và còn lại một phần không tan G. Để đốt cháy hoàn toàn X và G cần vừa đủ V lít khí (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 8:
Nung nóng hỗn hợp bột X gồm a mol Fe và b mol S trong khí trơ, hiệu suất phản ứng bằng 50%, thu được hỗn hợp rắn Y. Cho Y vào dung dịch HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối so với bằng 5. Tỉ lệ a:b bằng
 Xem đáp án
Xem đáp án
Đáp án A
Câu 9:
Lưu huỳnh tác dụng với axit sunfuric đặc, nóng:
Trong phản ứng này, tỉ lệ số nguyên tử lưu huỳnh bị khử và số nguyên tử lưu huỳnh bị oxi hoá là:
 Xem đáp án
Xem đáp án
Đáp án D
Chất khử (chất bị oxi hóa): ;
Chất oxi hóa (chất bị khử):
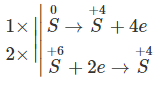
→ Tỉ lệ số nguyên tử lưu huỳnh bị khử () và số nguyên tử lưu huỳnh bị oxi hoá () là 2 : 1.
Câu 10:
Lưu huỳnh có thể tồn tại ở những trạng thái số oxi hoá nào
 Xem đáp án
Xem đáp án
Đáp án C
Số oxi hóa phổ biến của S là -2; 0; +4; +6.
Câu 11:
Cấu hình electron ở trạng thái kích thích của S khi tạo là:
 Xem đáp án
Xem đáp án
Đáp án B
Khi tạo , S ở trạng thái kích thích, 1 e của phân lớp 3p được chuyển lên phân lớp 3d tạo ra 4e độc thân.
Vậy cấu hình e ở trạng thái kích thích của S là:
Câu 12:
Tính chất vật lí nào sau đây không phải của lưu huỳnh?
 Xem đáp án
Xem đáp án
Đáp án C
Lưu huỳnh tà phương nóng chảy ở , lưu huỳnh đơn tà nóng chảy ở
→ Nhiệt độ nóng chảy của S cao hơn nhiệt độ sôi của nước.
Câu 13:
So sánh tính chất cơ bản của oxi và lưu huỳnh ta có
 Xem đáp án
Xem đáp án
Đáp án B
→ Tính oxi hóa của Oxi mạnh hơn lưu huỳnh; tính khử của lưu huỳnh mạnh hơn oxi.
Câu 14:
S vừa là chất khử, vừa là chất oxi hóa trong phản ứng nào sau đây
 Xem đáp án
Xem đáp án
Đáp án D
→ Vậy S vừa là chất khử, vừa là chất oxi hóa
Câu 15:
Ứng dụng nào sau đây không phải của S
 Xem đáp án
Xem đáp án
Đáp án C
90% lượng S sản xuất được dùng để sản xuất axit sunfuric;
10% lượng còn lại được dùng lưu hóa cao su, chế tạo diêm, sản xuất chất tẩy trắng bột giấy, chất dẻo ebonit, dược phẩm, phẩm nhuộm, chất trừ sâu, diệt nấm trong nông nghiệp, thuốc súng đen…
