Bài tập Tốc độ phản ứng có đáp án
-
193 lượt thi
-
18 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Làm thế nào có thể so sánh sự nhanh, chậm của các phản ứng hoá học để thúc đẩy hoặc kìm hãm nó theo mong muốn?
 Xem đáp án
Xem đáp án
Để so sánh sự nhanh, chậm của các phản ứng hóa học, chúng ta có thể dựa vào tốc độ phản ứng hóa học.
Câu 2:
Xét phản ứng: H2 + Cl2 → 2HCl.
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị sau:
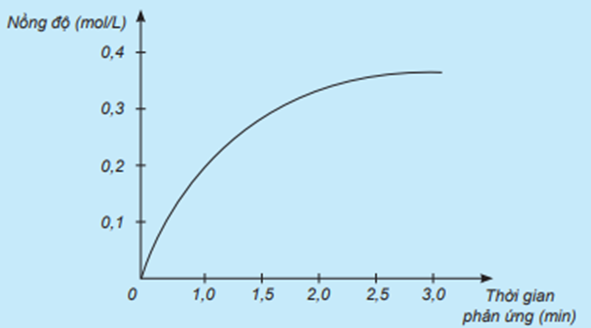
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
b) Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
 Xem đáp án
Xem đáp án
a) Đồ thị trên mô tả sự thay đổi nồng độ theo thời gian của HCl vì nồng độ của HCl tăng dần từ 0 mol/L theo thời gian.
b) Đơn vị của tốc độ phản ứng trong trường hợp này là mol/(L.min).
Câu 3:
Phản ứng phân hủy H2O2:
H2O2 ⟶ H2O + O2
Kết quả thí nghiệm đo nồng độ H2O2 tại các thời điểm khác nhau được trình bày trên Bảng 19.1.
Bảng 19.1. kết quả thí nghiệm phản ứng phân hủy H2O2
|
Thời gian phản ứng (h) |
0 |
3 |
6 |
9 |
12 |
|
Nồng độ H2O2 (mol/L) |
1,000 |
0,707 |
0,500 |
0,354 |
0,250 |
Biến thiên nồng độ trong khoảng thời gian từ 0 giờ đến 3 giờ là:
0,707 – 1,000 = – 293 (mol/L)
(Dấu "–" thể hiện rằng nồng độ H2O2 giảm dần khi phản ứng xảy ra.)
Tốc độ phản ứng trong khoảng thời gian từ 0 giờ đến 3 giờ được tính như sau:
= (mol/ (L.h))
(Đặt dấu "–" trước biểu thức để tốc độ phản ứng có giá trị dương.)
Trả lời câu hỏi:
1. Hãy tính tốc độ phản ứng theo nồng độ H2O2 trong các khoảng thời gian từ:
a) 3 giờ đến 6 giờ; b) 6 giờ đến 9 giờ c) 9 giờ đến 12 giờ.
2. Nhận xét về sự thay đổi tốc độ phản ứng theo thời gian.
 Xem đáp án
Xem đáp án
1.
a) Tốc độ phản ứng trong khoảng thời gian từ 3 giờ đến 6 giờ là:
=(mol/ (L.h))
b) Tốc độ phản ứng trong khoảng thời gian từ 6 giờ đến 9 giờ là:
=(mol/ (L.h))
c) Tốc độ phản ứng trong khoảng thời gian từ 9 giờ đến 12 giờ là:
=(mol/ (L.h))
2. Nhận xét: Tốc độ phản ứng giảm dần theo thời gian.
Câu 5:
Nghiên cứu ảnh hưởng của nồng độ đến tốc độ phản ứng:
Na2S2O3 + H2SO4 → Na2SO4 + S + SO2 + H2O
Chuẩn bị: Các dung dịch: Na2S2O3 0,05 M, Na2S2O3 0,10 M, Na2S2O3 0,30 M, H2SO4 0,5 M; 3 bình tam giác, đồng hồ bấm giờ, tờ giấy trắng có kẻ chữ X.
Tiến hành:
- Cho vào mỗi bình tam giác 30 mL dung dịch Na2S2O3 với các nồng độ tương ứng là 0,05 M; 0,10 M và 0,30 M. Đặt các bình lên tờ giấy trắng có kẻ sẵn chữ X.
- Rót nhanh vào mỗi bình 30 mL dung dịch H2SO4 0,5 M và bắt đầu bấm giờ.
Lưu ý: Phản ứng có sinh ra khí độc. Cần tiến hành cẩn thận và tránh ngửi trực tiếp trên miệng bình tam giác.

Hình 19.3 Thí nghiệm nghiên cứu ảnh hưởng của nồng độ đến tốc độ phản ứng
Quan sát vạch chữ X trên tờ giấy dưới đáy bình, ghi lại thời điểm không nhìn thấy vạch chữ X nữa và trả lời câu hỏi:
1. Phản ứng ở bình nào xảy ra nhanh nhất? Chậm nhất?
2. Nồng độ ảnh hưởng thế nào đến tốc độ phản ứng?
 Xem đáp án
Xem đáp án
1. Phản ứng ở bình chứa dung dịch Na2S2O3 có nồng độ 0,3M xảy ra nhanh nhất.
Phản ứng ở bình chứa dung dịch Na2S2O3 có nồng độ 0,05M xảy ra chậm nhất.
2. Khi nồng độ các chất tham gia tăng, tốc độ phản ứng sẽ tăng.
Câu 6:
Cho phản ứng của các chất ở thể khí: I2 + H2 → 2HI.
Biết tốc độ phản ứng tỉ lệ thuận với nồng độ của các chất tham gia phản ứng với số mũ là hệ số tỉ lượng của chất đó trong phương trình hoá học.
a) Hãy viết phương trình tốc độ của phản ứng này.
b) Ở một nhiệt độ xác định, hằng số tốc độ của phản ứng này là 2,5.10-4 L/(mol.s). Nồng độ đầu của I2 và H2 lần lượt là 0,02 M và 0,03 M. Hãy tính tốc độ phản ứng:
– Tại thời điểm đầu.
– Tại thời điểm đã hết một nửa lượng I2.
 Xem đáp án
Xem đáp án
a) Phương trình tốc độ của phản ứng:
v = k.
b) Tốc độ phản ứng tại thời điểm đầu là:
v = 2,5.10-4.0,02.0,03 = 1,5.10-7 (mol/(L.s))
- Tại thời điểm đã hết một nửa lượng I2
⇒ Tại thời điểm xét, nồng độ I2 còn 0,01M và đã phản ứng 0,01M
⇒ Theo phương trình, nồng độ H2 phản ứng là 0,01M
⇒ Tại thời điểm xét, nồng độ H2 còn 0,02M
⇒ v = 2,5.10-4.0,01.0,02 = 5.10-6 (mol/(L.s))
Câu 7:
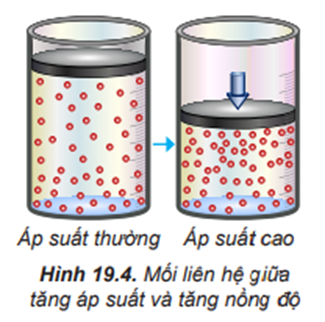
Nêu mối liên hệ giữa nồng độ và áp suất của khí trong hỗn hợp.
 Xem đáp án
Xem đáp án
Trong hỗn hợp khí, nồng độ mỗi khí tỉ lệ thuận với áp suất của nó. Khi nén hỗn hợp khí (giảm thể tích) thì nồng độ mỗi khí tăng lên và ngược lại.
Câu 8:
Áp suất ảnh hưởng đến tốc độ phản ứng nào sau đây?
N2(g) + 3H2(g) 2NH3(g) (1)
CO2(g) + Ca(OH)2(aq) ⟶ CaCO3(s) + H2O (l) (2)
SiO2(s) + CaO(s) ⟶ CaSiO3(s) (3)
BaCl2(aq) + H2SO4(aq) ⟶ BaSO4(s) + 2HCl(aq) (4)
 Xem đáp án
Xem đáp án
(1) và (2): Tăng áp suất làm tăng tốc độ phản ứng.
(3) và (4): Thay đổi áp suất không làm ảnh hưởng đến tốc độ của phản ứng vì không có sự tham gia của chất khí.
Câu 9:
Nghiên cứu ảnh hưởng của nhiệt độ đến tốc độ phản ứng:
Mg + 2H2O → Mg(OH)2 + H2↑
Chuẩn bị: Mg dạng phoi bào, dung dịch phenolphtalein, nước cất, 2 ống nghiệm, đèn cồn, kẹp gỗ.
Tiến hành:
- Cho vào mỗi ống nghiệm khoảng 3 mL nước cất.
- Nhỏ vào mỗi ống nghiệm 1 – 2 giọt phenolphtalein và cho vào mỗi ống 1 mẫu phoi bào Mg.
- Đun nóng 1 ống nghiệm.
Lưu ý: Làm sạch bề mặt Mg trước khi tiến hành thí nghiệm.
Quan sát và trả lời câu hỏi:
1. Sự thay đổi màu sắc trong ống nghiệm nào nhanh hơn?
2. Nhiệt độ ảnh hưởng như thế nào đến tốc độ phản ứng?
 Xem đáp án
Xem đáp án
1. Ống nghiệm được đun nóng, màu của dung dịch chuyển sang màu hồng nhanh hơn.
2. Khi tăng nhiệt độ, các hạt (phân tử, nguyên tử hoặc ion) sẽ chuyển động nhanh hơn, động năng cao hơn. Khi đó, số va chạm hiệu quả giữa các hạt tăng lên, dẫn đến tốc độ phản ứng tăng.
Câu 10:
Hãy giải thích tại sao khi nhiệt độ tăng thì tốc độ phản ứng tăng.
 Xem đáp án
Xem đáp án
Khi tăng nhiệt độ, các hạt (phân tử, nguyên tử hoặc ion) sẽ chuyển động nhanh hơn, động năng cao hơn. Khi đó, số va chạm hiệu quả giữa các hạt tăng lên, dẫn đến tốc độ phản ứng tăng.
Câu 11:
Nêu ý nghĩa của hệ số nhiệt độ Van't Hoff.
 Xem đáp án
Xem đáp án
Trong đó, γ là hệ số nhiệt độ Van’t Hoff, vT là tốc độ phản ứng tại nhiệt độ T, vT+10 là tốc độ phản ứng tại nhiệt độ T +10.
⇒ Ý nghĩa: Giá trị của γ càng lớn thì ảnh hưởng của nhiệt độ đến tốc độ phản ứng càng mạnh.
Câu 12:
Ở 20 °C, tốc độ một phản ứng là 0,05 mol/(L.min). Ở 30 °C, tốc độ phản ứng này là 0,15 mol/(L.min).
a) Hãy tính hệ số nhiệt độ Van't Hoff của phản ứng trên.
b) Dự đoán tốc độ phản ứng trên ở 40 °C (giả thiết hệ số nhiệt độ γ trong khoảng nhiệt độ này không đổi).
 Xem đáp án
Xem đáp án
a) Hệ số nhiệt độ Van't Hoff của phản ứng là
b) Ta có: = 3.0,15 = 0,45 mol/(L.min)
Câu 13:
Nghiên cứu ảnh hưởng của diện tích bề mặt đến tốc độ phản ứng:
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Chuẩn bị: 2 bình tam giác, dung dịch HCl 0,5 M, đá vôi dạng viên, đá vôi đập nhỏ.
Tiến hành:
- Cho cùng một lượng (khoảng 2 g) đá vôi dạng viên vào bình tam giác (1) và đá vôi đập nhỏ vào bình tam giác (2).
- Rót 20 mL dung dịch HCl 0,5 M vào mỗi bình.
Quan sát hiện tượng và trả lời câu hỏi:
1. Phản ứng trong bình nào có tốc độ thoát khí nhanh hơn?
2. Đá vôi dạng nào có tổng diện tích bề mặt lớn hơn?
3. Nêu ảnh hưởng của diện tích bề mặt tiếp xúc đến tốc độ phản ứng.
 Xem đáp án
Xem đáp án
1. Phản ứng trong bình tam giác (2) chứa đá vôi đập nhỏ có tốc độ thoát khí nhanh hơn.
2. Đá vôi khi đập nhỏ có diện tích bề mặt lớn hơn.
3. Khi tăng diện tích bề mặt tiếp xúc, số va chạm giữa các chất đầu tăng lên, số va chạm hiệu quả cũng tăng theo, dẫn đến tốc độ phản ứng tăng.
Câu 14:
Nghiên cứu ảnh hưởng của chất xúc tác đến tốc độ phản ứng:
2H2O2 ⟶ 2H2O + O2
Chuẩn bị: 2 bình tam giác, dung dịch H2O2 10%, MnO2.
Tiến hành:
- Rót vào 2 bình tam giác, mỗi bình 20 mL dung dịch H2O2 10%.
- Thêm khoảng 0,1 g xúc tác MnO2 vào một bình và lắc đều.
Quan sát hiện tượng và trả lời câu hỏi:
1. So sánh tốc độ thoát khí ở hai bình.
2. Chất xúc tác ảnh hưởng thế nào đến tốc độ phản ứng?
 Xem đáp án
Xem đáp án
1. Bình tam giác cho xúc tác MnO2 có tốc độ thoát khí lớn hơn.
2. Khi có xúc tác, phản ứng sẽ xảy ra qua nhiều giai đoạn. Mỗi giai đoạn đều có năng lượng hoạt hoá thấp hơn so với phản ứng không xúc tác. Do đó số hạt có đủ năng lượng hoạt hoá sẽ nhiều hơn, dẫn đến tốc độ phản ứng tăng.
Câu 15:
Thực hiện hai phản ứng phân huỷ H2O2 một phản ứng có xúc tác MnO2, một phản ứng không xúc tác. Đo thể tích khí oxygen theo thời gian và biểu diễn trên đồ thị như hình bên:
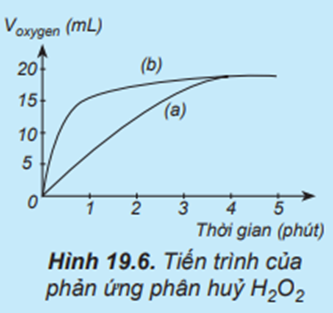
Đường phản ứng nào trên đồ thị (Hình 19.6) tương ứng với phản ứng có xúc tác, với phản ứng không có xúc tác?
 Xem đáp án
Xem đáp án
Đường phản ứng (a) trên đồ thị tương ứng với phản ứng không có xúc tác.
Đường phản ứng (b) trên đồ thị tương ứng với phản ứng có xúc tác vì lượng khí oxygen thoát ra ngay từ phút đầu tiên đã nhiều hơn.
Câu 16:
Yếu tố nào đã được áp dụng để làm thay đổi tốc độ của các phản ứng trong Hình 19.7?

 Xem đáp án
Xem đáp án
Yếu tố được áp dụng để làm thay đổi tốc độ của các phản ứng trong Hình 19.7 là:
a) Đèn xì oxygen – acetylene: nồng độ (tăng oxygen).
b) Tủ lạnh bảo quản thức ăn: nhiệt độ.
c) Bình dưa muối: chất xúc tác.
Câu 17:
Phản ứng tạo NO từ NH3 là một giai đoạn trung gian trong quá trình sản xuất nitric acid: 4NH3(g) +5O2(g) → 4NO(g) + 6H2O(g)
Hãy nêu một số cách để tăng tốc độ phản ứng này.
 Xem đáp án
Xem đáp án
Các cách để tăng tốc độ phản ứng:
- Tăng nồng độ của chất tham gia phản ứng.
- Sử dụng chất xúc tác: Platinum (Pt) ( hoặc Fe2O3, Cr2O3)
- Tăng nhiệt độ.
Câu 18:
Giải thích được tại sao nhiều phản ứng hoá học trong công nghiệp cần tiến hành ở nhiệt độ cao và sử dụng chất xúc tác.
 Xem đáp án
Xem đáp án
Trong công nghiệp, tổng hợp với số lượng lớn các chất hóa học từ những nguồn nguyên liệu dồi dào. Tuy nhiên, có những chất tham gia cần năng lượng lớn để phá vỡ liên kết mới tham gia phản ứng được hoặc có những phản ứng phản ứng xảy ra chậm.
⇒ Có nhiều phản ứng trong công nghiệp cần tiến hành ở nhiệt độ cao và sử dụng chất xúc tác.
