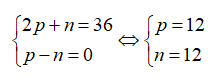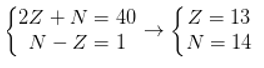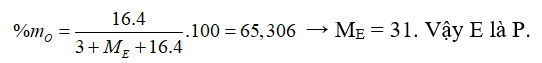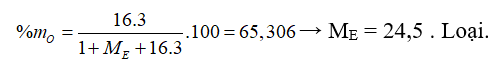Đề thi giữa kì 1 Hóa 10 có đáp án (Bài số 2 - Đề 3)
-
1117 lượt thi
-
30 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Liên kết được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung, gọi là
 Xem đáp án
Xem đáp án
Chọn B
Câu 2:
Liên kết hoá học giữa H và O trong phân tử là liên kết
(Cho độ âm điện H và O lần lượt là 2,2 và 3,44)
 Xem đáp án
Xem đáp án
Chọn C
Nguyên tử oxi có độ âm điện lớn hơn nhiều so với nguyên tử hiđro.
Ngoài ra, xét liên kết H – O, có hiệu độ âm điện 1,24
→ Liên kết cộng hóa trị phân cực
Câu 4:
Tổng số hạt trong nguyên tử một nguyên tố R là 36. Số hạt mang điện gấp đôi hạt không mang điện. R là
 Xem đáp án
Xem đáp án
Chọn A
Gọi số proton, nơtron và electron của R lần lượt là p, n và e.
Ta có:
Vậy R là Mg.
Câu 5:
Nguyên tử các nguyên tố thuộc nhóm VA có số electron lớp ngoài cùng là
 Xem đáp án
Xem đáp án
Chọn C
Số electron lớp ngoài cùng = STT nhóm A = 5.
Câu 6:
Cho nguyên tố X có số hiệu nguyên tử là 18, vị trí của nguyên tố trong bảng tuần hoàn các nguyên tố hoá học là
 Xem đáp án
Xem đáp án
Chọn A
Cấu hình electron nguyên tử X:
X ở ô số 18 (z = 18), chu kỳ 3 (có 3 lớp e), nhóm VIIIA (8 electron lớp ngoài cùng, nguyên tố p).
Câu 7:
Nguyên tố R thuộc nhóm VIA. Công thức oxit cao nhất của R và công thức hợp chất khí với hiđro của R là
 Xem đáp án
Xem đáp án
Chọn D
R thuộc nhóm VIA → Hóa trị của R trong oxit cao nhất là VI, hóa trị của R trong hợp chất khí với H là II.
→ Công thức oxit cao nhất của R và công thức
hợp chất khi với hiđro lần lượt là
Câu 8:
Nguyên tử của nguyên tố R có 3 electron thuộc phân lớp 3d. Vị trí của nguyên tố R trong bảng tuần hoàn là vị trí nào sau đây
 Xem đáp án
Xem đáp án
Chọn A
Cấu hình electron của nguyên tử R là:
R thuộc chu kỳ 4 do có 4 lớp electron, nhóm VB do 5 electron hóa trị và nguyên tố d. Nguyên tử R có 23 electron vậy R thuộc ô số 23.
Câu 9:
Có những tính chất sau đây của nguyên tố:
(1) Hóa trị của nguyên tố trong hợp chất với oxi;
(2) Bán kính nguyên tử;
(3) Tính kim loại – phi kim;
(4) Tính axit – bazơ của hợp chất hiđroxit.
Trong các tính chất trên, số tính chất biến đổi tuần hoàn trong một nhóm A là
 Xem đáp án
Xem đáp án
Chọn C
Trong một nhóm A, các tính chất 1, 3, 4 biến đổi tuần hoàn
Câu 10:
Tổng số các hạt proton, nơtron và electron trong nguyên tử của một nguyên tố là 40. Biết số hạt nơtron lớn hơn số hạt proton là 1. Cho biết nguyên tố trên thuộc loại nguyên tố nào?
 Xem đáp án
Xem đáp án
Chọn B
Giả sử số proton, số nơtron, số electron của nguyên tố trên lần lượt là p; n và e.
Trong đó: p =e =z.
Ta có hpt:
Cấu hình electron của nguyên tố là:
Nhận thấy electron cuối cùng điền vào phân lớp p → nguyên tố trên thuộc loại nguyên tố p
Câu 12:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Chọn D
A sai vì trong nguyên tử, số p = số e.
B sai vì nguyên tử có cùng số proton thuộc cùng nguyên tố hóa học.
C sai vì không phải nguyên tử nào cũng có số p = số n.
D đúng vì M có cấu hình electron nguyên tử: [Ne] nên thuộc chu kỳ 3, nhóm IA.
Câu 13:
Anion đơn nguyên tử Xn- có tổng số hạt mang điện là 18. Vị trí của nguyên tố X trong bảng tuần hoàn các nguyên tố hóa học là
 Xem đáp án
Xem đáp án
Chọn D
Vì X có Z < 18 : 2= 9
Câu 15:
Chỉ ra nội dung sai khi nói về ion :
 Xem đáp án
Xem đáp án
Chọn B
Ion âm gọi là anion, ion dương gọi là cation.
Câu 21:
E là một nguyên tố có công thức hợp chất khí với H và oxit có hóa trị cao nhất của E lần lượt là: EHa và có 2a + 3b = 21. % khối lượng của O trong hiđroxit có hóa trị cao nhất của E là 65,306%. Nguyên tố E là
 Xem đáp án
Xem đáp án
Chọn B
Từ công thức oxit cao nhất và công thức hợp chất khí với H ta có: a + b = 8.
Theo bài ra: 2a + 3b = 21
→ a = 3 và b = 5.
Vậy E thuộc nhóm VA.
Trường hợp 1: Công thức hiđroxit tương ứng của E là:
Trường hợp 2: Công thức hiđroxit tương ứng là
Câu 24:
Tổng số electron trong ion là:
 Xem đáp án
Xem đáp án
Chọn D
Trong nguyên tử Cl, số e = số p = z = 17.
Ta có: Cl + 1e → Cl-
Vậy số electron của Cl- là 17 + 1 = 18.
Câu 25:
Trong bảng tuần hoàn, nguyên tố có tính phi kim mạnh nhất là
 Xem đáp án
Xem đáp án
Chọn B
Phi kim mạnh nhất là Flo (F).
Câu 26:
Cation M+ có cấu hình electron Vậy M là nguyên tố:
 Xem đáp án
Xem đáp án
Chọn C
M → M+ + 1e
Vậy cấu hình e của M là . Do đó M ở chu kỳ 3, nhóm IA.
Câu 27:
Trong số các nguyên tử sau, chọn nguyên tử có số nơtron nhỏ nhất
 Xem đáp án
Xem đáp án
Chọn A
A: số n = 235 – 92 = 143
B: số n = 239 – 93 = 146
C: số n = 239 – 94 = 145.
D: số n = 243 – 95 = 148.
Câu 28:
Cho biết nguyên tố A ở chu kì 3, nhóm VIIA. Cấu hình electron của A là
 Xem đáp án
Xem đáp án
Chọn A
A ở chu kỳ 3 nên có 3 lớp electron; A thuộc nhóm VIIA nên số electron lớp ngoài cùng là 7.
Cấu hình electron của A là