125 câu trắc nghiệm Oxi - Lưu huỳnh cơ bản phần 3 (có đáp án)
-
3836 lượt thi
-
25 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Hòa tan hoàn toàn hỗn hợp chứa 16,8 gam Fe và 4,4 gam FeS vào dung dịch H2SO4 loãng, dư, thể tích khí thu được ở đktc sau phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án B
Câu 2:
Khí nào sau đây có thể thu được bằng phương pháp dời chỗ nước?
 Xem đáp án
Xem đáp án
Đáp án A.
Do oxi tan ít trong nước
Câu 4:
Cho 11,3 gam hỗn hợp gồm Mg và Cu tác dụng hết với dung dịch H2SO4 loãng, thấy thoát ra 2,24 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 5:
Đốt 6,5 gam Zn trong lưu huỳnh. Khối lượng lưu huỳnh tham gia phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án A.
nZn = 0,1 (mol)
Zn + S → ZnS
0,1 0,1
mS = 0,1.32 = 3,2 (g)
Câu 6:
Trong những câu sau, câu nào sai khi nói về tính chất hóa học của ozon?
 Xem đáp án
Xem đáp án
Đáp án A.
Ozon có khả năng oxi hóa hầu hết các kim loại, trừ Au, Pt.
Câu 8:
Hòa tan hoàn toàn 6,72 lít SO2 (đktc) vào 100 ml dd KOH 3,5M, muối thu được sau phản ứng là:
 Xem đáp án
Xem đáp án
Đáp án C
Tạo K2SO3 và KHSO3
Câu 10:
Oxi hóa hoàn toàn m gam kim loại X cần vừa đủ 0,25m gam khí O2. X là
 Xem đáp án
Xem đáp án
Đáp án C
Chọn m = 32 gam
⇒ = 0,25 mol
Bảo toàn electron
⇒ nX.n = 0,25.4 ⇒ X=32n ⇒ n=2; X=64 (Cu)
Câu 11:
Nhiệt phân hoàn toàn 31,6 gam KMnO4, thu được V lít O2 (đktc), biết hiệu suất phản ứng 80%. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 12:
Tiến hành phản ứng hết a gam ozon thì thu được 94,08 lít khí O2 (đktc). Xác định giá trị của a.
 Xem đáp án
Xem đáp án
Đáp án B
Ta có: nO2 = 4,2 (mol)
Phản ứng: 2O3 → 3O2 (1)
2,8 ← 4,2 (mol)
mozon = 2,8 × 16.3 = 134,4 (gam)
Câu 13:
Cho các phản ứng sau:
Số phản ứng trong đó S thể hiện tính khử là :
 Xem đáp án
Xem đáp án
Đáp án B.
S thể hiện tính khử trong các phương trình a, b, c.
Câu 14:
Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hoá trong phản ứng nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A.
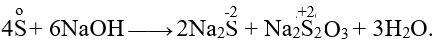
Câu 15:
Để phân biệt oxi và ozon có thể dùng chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án D.
KI + → không phản ứng
I2 sinh ra sau phản ứng làm hồ tinh bột chuyển sang màu xanh.
Câu 17:
Cho 1,3 gam kẽm tác dụng với 0,32 gam lưu huỳnh chất thu được sau khi phản ứng xảy ra hoàn toàn là
 Xem đáp án
Xem đáp án
Đáp án C.
Zn + S → ZnS
0,02 0,01 (mol)
Sau phản ứng thu được: ZnS: 0,01 mol và Zn dư 0,01 mol.
Câu 18:
Dẫn 2,24 lít khí H2S vào dung dịch chứa 0,2 mol NaOH thu được dung dịch chứa chất tan là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 19:
Hòa tan hoàn toàn 3,22 gam hỗn hợp X gồm Fe, Mg và Zn bằng một lượng vừa đủ dung dịch H2SO4 loãng, thu được 1,344 lít hiđro (ở đktc) và dung dịch chứa m gam muối. Giá trị của m là?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 20:
Cho phản ứng hoá học:
H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
Vai trò của H2S trong phản ứng là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 21:
Lưu huỳnh đioxit có thể tham gia phản ứng:
SO2 + 2Mg → 2MgO + S;
SO2+ Br2 + H2O → 2HBr + H2SO4.
Tính chất của SO2 được diễn tả đúng nhất là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 22:
Cho phản ứng Hệ số cân bằng của H2SO4 là (biết hệ số cân bằng của phản ứng là các số nguyên, tối giản)
 Xem đáp án
Xem đáp án
Đáp án C
Câu 23:
Trong số những tính chất sau, tính chất nào không là tính chất của axit H2SO4 đặc nguội?
 Xem đáp án
Xem đáp án
Đáp án C
