125 câu trắc nghiệm Oxi - Lưu huỳnh cơ bản phần 4 (có đáp án)
-
3835 lượt thi
-
25 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Hoà tan hết hỗn hợp gồm Zn và Cu cần vừa đủ 200ml dung dịch H2SO4 loãng 0,1M thu được V lít khí (đktc). V có giá trị là
 Xem đáp án
Xem đáp án
Đáp án D
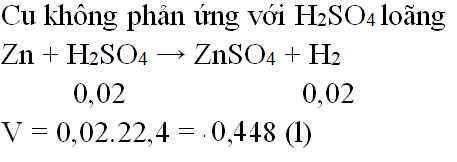
Câu 2:
Người ta thường dùng các vật dụng bằng bạc để cạo gió cho người bị trúng gió (khi người bị mệt mỏi, chóng mặt…do trong cơ thể tích tụ các khí độc như H2S…). Khi đó vật bằng bạc bị đen do phản ứng:
4Ag + O2 + 2H2S → 2Ag2S + 2H2O
Câu nào diễn tả đúng tính chất của các chất phản ứng?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 3:
Dẫn khí H2S vào dung dịch KMnO4 và H2SO4 loãng, hiện tượng quan sát được là:
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 4:
Thực hiện các phản ứng sau:
Có bao nhiêu trường hợp thường dùng để điều chế oxi trong phòng thí nghiệm?
 Xem đáp án
Xem đáp án
Đáp án A.
Các phản ứng là a,b
Câu 5:
Thuốc thử dùng để phân biệt 3 dung dịch H2SO4 loãng, Ba(OH)2, HCl đựng trong lọ mất nhãn là
 Xem đáp án
Xem đáp án
Đáp án B.
- Dùng BaCl2 nhận ra H2SO4 nhờ hiện tượng kết tủa trắng.
- Dùng H2SO4 vừa nhận ra cho vào hai ống nghiệm đựng hai chất còn lại.
+ Có kết tủa trắng → Ba(OH)2
+ Không hiện tượng → HCl.
Câu 6:
Hòa tan hoàn toàn 2,4 gam kim loại Mg vào dung dịch H2SO4 đặc, nóng, giả sử chỉ thu được V lít khí SO2 là sản phẩm khử duy nhất (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D.
nMg = 0,1 (mol)
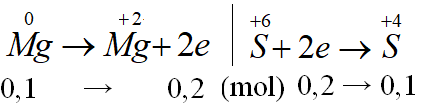
Câu 9:
Một chất dùng để làm sạch nước, dùng để chữa sâu răng và có tác dụng bảo vệ các sinh vật trên trái đất không bị bức xạ cực tím. Chất này là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 10:
Hoà tan hoàn toàn 2,16 gam kim loại M hóa trị III bởi lượng dư dung dịch H2SO4 đặc, nóng thu được 2,688 gam khí SO2 (là sản phẩm khử duy nhất). M là
 Xem đáp án
Xem đáp án
Đáp án D
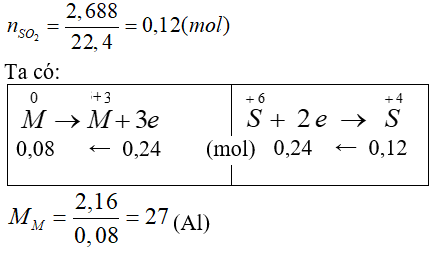
Câu 11:
Có thể điều chế O2 bằng cách phân huỷ KMnO4, KClO3, H2O2. Nếu lấy cùng một lượng mol các chất trên đem phân huỷ hoàn toàn thì thể tích oxi trong cùng điều kiện thu được
 Xem đáp án
Xem đáp án
Đáp án B
PTHH:
2KMnO4 → K2MnO4 + MnO2 + O2
2 1 mol
2H2O2 → 2H2O + O2
2 1 mol
2KClO3 → 2KCl + 3O2
2 3 mol
Câu 12:
Có 3 dung dịch đựng trong các bình mất nhãn: HCl, Na2SO4, Na2SO3. Có thể chọn thuốc thử nào sau đây để nhận biết ba chất trên?
 Xem đáp án
Xem đáp án
Đáp án D
Lấy BaCl2 cho lần lượt vào 3 mẫu thử.
Các phương trình phản ứng xảy ra:
Mẫu không có kết tủa là HCl. Lấy HCl cho vào kết tủa, BaSO3 tan.
Câu 13:
Lưu huỳnh đioxit có thể tham gia các phản ứng sau:
SO2 + Br2+ 2H2O → 2HBr + H2SO4 (1)
2H2S + SO2 → 3S + 2H2O (2).
Câu nào sau đây diễn tả không đúng tính chất của các chất trong những phản ứng trên?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 14:
Để đánh giá độ nhiễm bẩn không khí của một nhà máy, người ta lấy hai lít không khí rồi dẫn qua dung dịch Pb(NO3)2 dư thấy có kết tủa màu đen xuất hiện. Hiện tượng này chứng tỏ trong không khí có hiện diện khí nào sau?
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 15:
Dung dịch X chứa: FeCl3; CuCl2; AlCl3; NaCl, CdCl2; ZnCl2; MgCl2. Sục khí H2S đến dư vào dung dịch X. Số kết tủa khác nhau thu được là:
 Xem đáp án
Xem đáp án
Đáp án D
Các kết tủa thu được là: S; CuS; CdS
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
CuCl2 + H2S → CuS + 2HCl
CdCl2 + H2S → CdS + 2HCl
Câu 16:
Để nhận biết hai bình chứa khí không màu CO2 và SO2, cách làm nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án B
Do cả SO2 và CO2 đều phản ứng với Ca(OH)2 tạo kết tủa CaSO3 và CaCO3 đều màu trắng, sau đó nếu khí dư đều hòa tan kết tủa, không thể phân biệt được.
Câu 17:
Đốt cháy hoàn toàn 17,4 gam hỗn hợp Mg và Al trong khí oxi (dư) thu được 30,2 gam hỗn hợp oxit. Thể tích khí oxi (đktc) đã tham gia phản ứng là
 Xem đáp án
Xem đáp án
Đáp án B.
Bảo toàn khối lượng:
V = 0,4.22,4 = 8,96 (lít)
Câu 18:
Dẫn a mol khí H2S vào dung dịch chứa b mol NaOH. Để thu được muối trung hòa thì:
 Xem đáp án
Xem đáp án
Đáp án C
Câu 19:
Hấp thụ 2,24 lít khí SO2 (đktc) vào 300 ml dung dịch NaOH 1M, thu được dung dịch X. Chất tan trong X là
 Xem đáp án
Xem đáp án
Đáp án C
Tạo Na2SO3, NaOH dư
Câu 20:
Dẫn V lít (đktc) khí SO2 vào 200 ml dung dịch KOH 1M thu được 12 gam muối KHSO3. Vậy V có giá trị là:
 Xem đáp án
Xem đáp án
Đáp án B
Các phương trình phản ứng xảy ra:
SO2 + KOH → KHSO3
0,1 0,1 0,1 mol
SO2 + 2KOH → K2SO3 + H2O
0,05 0,1 mol
Tổng số mol SO2 = 0,15 mol
→ V = 3,36 lit
Câu 21:
Nhiệt phân hoàn toàn 24,5 gam KClO3 sau phản ứng thấy thoát ra V lít khí oxi (đktc). Giá trị của V là:
 Xem đáp án
Xem đáp án
Đáp án B
V = 0,3.22,4 = 6,72 lít
Câu 22:
Hòa tan 12,8 gam hh Fe, FeO bằng dd HCl vừa đủ, thu được 2,24 lít (đktc). Thành phần phần trăm theo khối lượng của FeO trong hỗn hợp là:
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 23:
Trong sơ đồ chuyển hoá:
S → FeS → H2S → H2SO4 → SO2 → S
có ít nhất bao nhiêu phản ứng thuộc loại phản ứng oxi hoá-khử?
 Xem đáp án
Xem đáp án
Đáp án A
Ta có dãy chuyển đổi số oxi hóa của S như sau:
Phản ứng thuộc loại phản ứng oxi hoá-khử khi S thay đổi số oxi hóa.
Nhưng từ H2SO4 → SO2 có thể là phản ứng:
là phản ứng trao đổi
→ Có ít nhất 3 phản ứng là phản ứng oxi hóa - khử.
Câu 24:
Phát biểu nào sau đây là sai?
 Xem đáp án
Xem đáp án
Đáp án D
Ý "O3 là nguyên nhân chính gây nên biến đổi khí hậu toàn cầu." → sai, nguyên nhân chính là CO2
