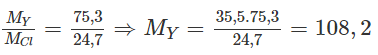Giải SBT Bài 22: Clo
-
2878 lượt thi
-
15 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
PTHH nào sau đây biểu diễn đúng phản ứng của dây sắt nóng đỏ cháy trong khí Cl2
 Xem đáp án
Xem đáp án
Đáp án B
Câu 2:
Lá đồng khi đốt nóng có thể cháy sáng trong khí A.
A là khí nào trong số các khí sau ?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 5:
Trong phòng thí nghiệm khí clo thường được điểu chế bằng cách oxi hóa hợp chất nào sau đây
 Xem đáp án
Xem đáp án
Đáp án B
Câu 8:
Số mol Cl2 thu được khi cho 0,2 mol KClO3 tác dụng với dung dịch HCl đặc, dư là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 9:
Khí Cl2 điều chế bằng cách cho MnO2 tác dụng với dung dịch HCl đặc thường bị lẫn tạp chất là khí HCl. Có thể dùng dung dịch nào sau đây để loại tạp chất là tốt nhất
 Xem đáp án
Xem đáp án
Đáp án D
Câu 12:
Phản ứng nào xảy ra khi sục khí clo vào dung dịch Na2CO3
 Xem đáp án
Xem đáp án
+ Khí clo tác dụng với nước tạo ra các axit :
Cl2 + H2O → HCl + HClO
+ Axit mạnh (HCl) tác dụng với muối :
2HCl + Na2CO3 → 2NaCl + H2O + CO2
Câu 13:
Dẫn khí Cl2 vào
a) Dung dịch KOH ở nhiệt độ thường.
b) Dung dịch KOH đun nóng tới gần 100°C.
Hãy viết PTHH của phản ứng xảy ra trong mỗi trường hợp. Cho biết vai trò của clo trong mỗi phản ứng oxi hoá - khử đó
 Xem đáp án
Xem đáp án
a) 3Cl2 + 2KOH → KCl + KClO + 3H2O
b) 3KCl + 6KOH → 5KCl + KClO3 + 4H2O
Trong các phản ứng trên, clo vừa là chất oxi hoá, vừa là chất khử. Đó là các phản ứng tự oxi hoá, tự khử (hay còn gọi là phản ứng tự oxi hoá - khử).
Câu 14:
Nêu nguyên tắc của việc điều chế khí Cl2 trong phòng thí nghiệm. Viết PTHH của 5 phản ứng minh hoạ.
 Xem đáp án
Xem đáp án
Cho chất oxi hoá mạnh tác dụng với dung dịch HCl đặc (từng chất oxi hoá mạnh để oxi hoá ion clorua Cl- thành đơn chất clo).
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
KClO3 + 6HCl → KCl + 3Cl2 + 3H2O
CaOCl2 + 2HCl → CaCl2 + Cl2 + H2O
K2Cr2O7 + 14HCl → 2KCl + 2CrCl3 + 3Cl2 + 7H2
Câu 15:
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp (ZX < ZY) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
 Xem đáp án
Xem đáp án
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
(MY và MCl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))