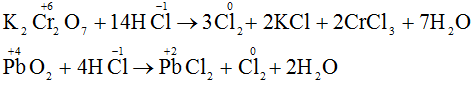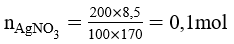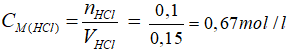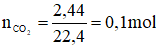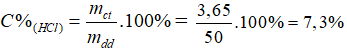Bài 23: Hiđro clorua - Axit clohiđric và muối clorua
-
2970 lượt thi
-
7 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Cho 20g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 1g khí bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
 Xem đáp án
Xem đáp án
= 
= x; = y.
= x + y = 0,5 mol.
= 24x + 56y = 20g.
Giải hệ phương trình ta có x = y =0,25 mol.
= 0, 25 × 95 = 23,75g.
= 0,25 × 127 = 31,75g
Khối lượng muối clorua = 23,75 + 31,75= 55,5
Câu 2:
Nêu những tính chất vật lí của khí hiđro clorua HCl.
 Xem đáp án
Xem đáp án
Hiđro clorua là chất khí không màu, mùi xốc, nặng hơn không khí, khí hiđro clorua tan nhiều trong nước tạo thành dung dịch axit, ở một thể tích nước hòa tan 500 thể tích hiđro clorua.
Câu 3:
Có các chất sau: axit sunfuric đặc, nước, kali clorua rắn. Hãy viết các phương trình phản ứng để điều chế hidro clorua.
 Xem đáp án
Xem đáp án
Phương trình hóa học của phản ứng điều chế hidro clorua
.
Câu 4:
Hãy dẫn ra những phản ứng hóa học của axit clohiđric để làm thí dụ.
a) Đó là những phản ứng oxi hóa – khử.
b) Đó không phải là phản ứng oxi hóa – khử.
 Xem đáp án
Xem đáp án
a) Những ví dụ phương trình phản ứng hóa học của axit clohidric là phản ứng oxi hóa – khử:
Với vai trò là chất khử:
Với vai trò là chất oxi hóa :
Mg + 2HCl →
b) Những ví dụ phương trình phản ứng hóa học của axit clohidric là không phải là phản ứng oxi hóa – khử:
+ 2HCl → +
CuO + 2HCl → .
Câu 5:
Bản chất của các phản ứng điều chế hiđro clorua bằng phương pháp sunfat và phương pháp tổng hợp khác nhau như thế nào? Các phương pháp trên đã dựa vào những tính chất hóa học nào của các chất tham gia phản ứng?
 Xem đáp án
Xem đáp án
Bản chất của phương pháp sunfat là dùng phản ứng trao đổi.
NaCl + → + HCl.
Bản chất của phương pháp tổng hợp là dùng phương pháp hóa hợp (phản ứng oxi hóa – khử).
+ → 2HCl.
Câu 6:
Sục khí đi qua dung dịch thấy có khí thoát ra. Hãy viết phương trình hóa học của các phản ứng đã xảy ra.phương trình hóa học của các phản ứng đã xảy ra.
 Xem đáp án
Xem đáp án
+ ⇆ HCl + HClO
2HCl + → 2NaCl + ↑ + .
Câu 7:
Tính nồng độ của hai dung dịch axit clohiđric trong các trường hợp sau:
a) Cần phải dùng 150ml dung dịch HCl để kết tủa hoàn toàn 200g dung dịch 8,5%.
b) Khi cho 50g dung dịch HCl vào một cốc đựng (dư) thì thu được 2,24 lít khí ở đktc.
 Xem đáp án
Xem đáp án
a)
Phương trình hóa học của phản ứng:
Theo pt = 0,1 mol
b)
Phương trình hóa học của phản ứng:
Theo pt: = 0,1 mol ⇒ = 0,1. 36,5 = 3,65 g