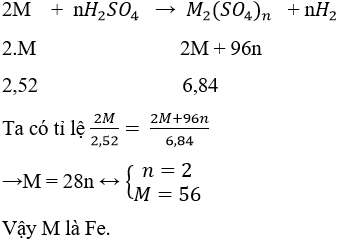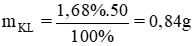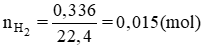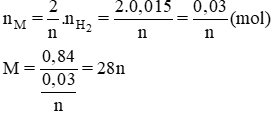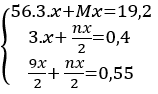Bài 31: Sắt
-
2538 lượt thi
-
5 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Các kim loại nào sau đây đều phản ứng với dung dịch CuCl2?
 Xem đáp án
Xem đáp án
Đáp án B.
Các phản ứng xảy ra:
Fe + CuCl2 → FeCl2 + Cu
2Na + 2H2O → 2NaOH + H2
2NaOH + CuCl2 → 2NaCl + Cu(OH)2
Mg + CuCl2 → MgCl2 + Cu
Câu 2:
Cấu hình electron nào sau đây là của Fe3+ ?
 Xem đáp án
Xem đáp án
Đáp án B.
Cấu hình e của Fe: [Ar]3d64s2
⇒ cấu hình e của Fe3+: [Ar]3d5
Câu 3:
Cho 3,52 gam một kim loại tác dụng hết với dung dịch H2SO4 loãng, thu được 6,84 gam muối sunfat. Kim loại đó là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 4:
Ngâm một lá kim loại có khối lượng 50 gam trong dung dịch HCl. Sau khi thu được 336ml khí H2 (đktc) thì khối lượng lá kim loại giảm 1,68 %. Kim loại đó là :
 Xem đáp án
Xem đáp án
Đáp án B.
Khối lượng kim loại phản ứng là
Số mol H2 là
2M + 2n HCl → 2MCl2 + nH2
Số mol của M là:
→ {n = 2, M = 56} → M: Fe
Câu 5:
Hỗn hợp A chứa Fe và kim loại M có hóa trị không đổi trong mọi hợp chất. Tỉ lệ số mol của M và Fe trong hỗn hợp là 1 : 3. Cho 19,2 gam hỗn hợp A tan hết vào dung dịch HCl thu được 8,96 lít khí H2 Cho 19,2 gam hỗn hợp A tác dụng hết với Cl2 thì cần dùng 13,32 lít khí Cl2. Xác định kim loại M và phần trăm khối lượng các kim loại trong hỗn hợp A. Các thể tích khí đo ở đktc.
 Xem đáp án
Xem đáp án
Gọi hóa trị của M là n
Gọi nMg = x mol ⇒ nFe = 3.x mol
Số mol H2 là: nH2 = 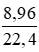
Số mol Cl2 là: nCl2 = 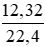
Các PTHH
Theo bài ra ta có hệ phương trình:
Giải hệ pt ⇒ x = 0,1 mol ⇒ n = 2 ⇒ M = 24
Vậy M là Mg
nMg = 0,1 mol ⇒ nFe = 0,3 mol
Thành phần % theo khối lượng