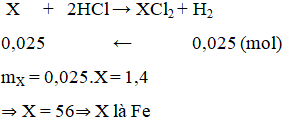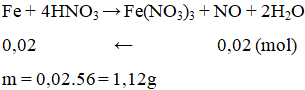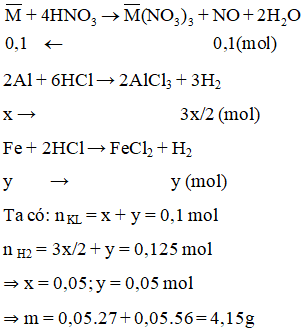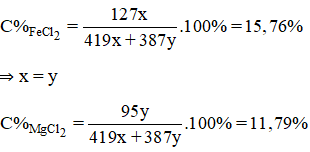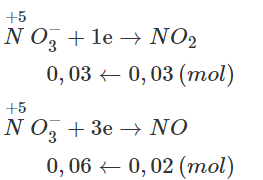SBT Hóa học 12 Bài 31: Sắt
-
429 lượt thi
-
21 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 3:
Cho 1,4 g kim loại X tác dụng với dung dịch HCl thu được dung dịch muối trong đó kim loại có sô oxi hoá +2 và 0,56 lít H2 (đktc). Kim loại X là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 4:
Cho m gam Fe tác dụng với dung dịch HNO3 loãng, dư thu được 0,448 lít khí NO duy nhất (đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 5:
Cho 8 g hỗn hợp bột kim loại Mg và Fe tác dụng hết với dung dịch HCl thấy thoát ra 5,6 lít H2 (đktc). Khối lượng muối tạo ra trong dung dịch là
 Xem đáp án
Xem đáp án
Đáp án D
nH2 = 0,25 mol ⇒ nH = 0,5 mol
Khi có 0,5 mol nguyên tử H thoát ra thì cũng có 0,5 mol ion Cl- tạo muối
mmuối = mKL + mgốc axit = 8 + 35,5.0,5 = 25,75(g)
Câu 6:
Cho m gam hỗn hợp Al và Fe phản ứng hoàn toàn với dung dịch HNO3 loãng thu được 2,24 lít NO duy nhất (đktc). Mặt khác cho m gam hỗn hợp này phản ứng với dung dịch HCl thu được 2,80 lít H2 (đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 13:
Fe tác dụng được với dung dịch muối FeCl3 theo phản ứng:
Fe + 2FeCl3→ 3FeCl2 là do:
 Xem đáp án
Xem đáp án
Đáp án B
Câu 14:
Hoà tan hoàn toàn hỗn hợp X gồm Fe và Mg bằng một lượng vừa đủ dung dịch HC1 20% thu được dung dịch Y. Nồng độ của FeCl2 trong dung dịch Y là 15,76%. Nồng độ phần trăm của MgCl2 trong dung dịch Y là
 Xem đáp án
Xem đáp án
Đáp án D
Gọi số mol Fe, Mg lần lượt là: x, y ⇒ nHCl pư = 2(x + y)
mdd sau pư = mkl + mdd HCl – mH2
⇒ mdd = 56x + 24y + 73(x+y).100/20 – 2(x+y) = 419x + 387y (g)
Câu 15:
Cho các chất sau: (1) Cl2; (2) I2; (3) HNO3; (4) H2SO4 đặc nguội. Khi cho Fe tác dụng với chất nào trong số các chất trên đều tạo được hợp chất trong đó sắt có hóa trị (III)
 Xem đáp án
Xem đáp án
Đáp án D
Câu 16:
Đốt một kim loại trong bình kín đựng khí clo thu được 32,5 g muối clorua và nhận thấy thể tích khí clo trong bình giảm 6,72 lít (đktc). Hãy xác định tên của kim loại đã dùng.
 Xem đáp án
Xem đáp án
Gọi kim loại là M, có hoá trị n.
2M + nCl2 → 2MCln
Theo phương trình hoá học, cứ :
n mol Cl2 thu được 2 mol muối
Vậy 6,72/22,4 = 0,3 mol Cl2 thu được 32,5/(M +32,5n) muối
Do đó ta có : n. 32,5/(M +32,5n) = 2.0,3 → M = 56n/3
Vì n là số nguyên, dương nên chỉ có n = 3 và M = 56 là hợp lí. Vậy kim loại đã dùng là Fe.
Câu 17:
Sắt tác dụng như thế nào với dung dịch đặc và loãng của các axit HCl, H2SO4, HNO3 ở nhiệt độ thường và nhiệt độ cao ? Viết phương trình hoá học của các phản ứng.
 Xem đáp án
Xem đáp án
Fe + 2HCl(l) → FeCl2 + H2
2Fe + 3H2SO4(l) → Fe2(SO4)3 + 3H2
2Fe + 6H2SO4 to→ Fe2(SO4)3 + 6SO2 + 3H2O
Fe + H2SO4 (đ, nguội) → không phản ứng
Fe + 4HNO3 (l) → Fe(NO3)3 + NO + 2H2O
Fe + HNO3 (đ, nguội) → không phản ứng
Fe + HNO3 (đ) to→ Fe(NO3)3 + 3NO2 + 3H2O
Câu 18:
Đốt nóng một lượng bột sắt trong bình đựng khí O2, sau đó để nguội và cho vào bình một lượng dư dung dịch HCl. Viết phương trình hoá học của các phản ứng có thể xảy ra
 Xem đáp án
Xem đáp án
Đốt Fe trong khí O2, sản phẩm có thể là FeO, Fe3 O4 , Fe2O3 và Fe (dư).
Cho dd HCl vào có các phản ứng:
FeO + 2HCl → FeCl2 + H2O
Fe + 2HCl(l) → FeCl2 + H2
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + H2O
Fe2O3 + 6HCl → 2FeCl2 + 3H2O
Fe + 2FeCl3 → 3FeCl2
Câu 19:
Cho 3,04 g hỗn hợp bột kim loại sắt và đồng tác dụng hết với dung dịch HNO3 loãng, thu được 0,896 lít khí NO duy nhất (đktc). Xác định thành phần phần trăm khối lượng của mỗi kim loại trong hỗn hợp.
 Xem đáp án
Xem đáp án
Fe+ 4HNO3 (l) → Fe(NO3)3 + NO + 2H2O (1)
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O (2)
Đặt x và y la số mol Fe và Cu trong hỗn hợp ta có hệ pt:
56x + 64y = 3,04
x + 2y/3 = 0,04
→ x= 0,02 , y= 0,03
%mFe = 56.0,02/3,04 . 100% = 36,8%
%m Cu = 100 – 36,8= 63,2%.
Câu 20:
Hoà tan 4 gam một đinh sắt đã bị gỉ trong dung dịch H2SO4 loãng, dư tách bỏ phần không tan được dung dịch A. Dung dịch A này phản ứng vừa hêt với 100 ml dung dịch KMnO4 0,1M. Tính % tạp chất trong đinh sắt giả sử gỉ sắt không phản ứng với dung dịch axit.
 Xem đáp án
Xem đáp án
Giả sử phần oxit không phản ứng, vậy chỉ có sắt nguyên chất phản ứng, thứ tự phản ứng như sau :
Fe H2SO4→ Fe2+
phương trình cho - nhận e :
Fe2+ → Fe3+ + le Mn7+O4- + 5e → Mn2+
Số mol KMnO4 là 0,01mol ⟹ n Fe3+ = 0,05
⟹ nFe = nFe2+ = nFe3+ = 0,05 (mol)
⟹ nFe = 56.0,05 = 2,8 (gam) ⟹ m tạp chất = 1,2 (gam)
=> % tạp chất = 1,2/4 . 100% = 30%
Câu 21:
Cho Fe tác dụng với dung dịch HNO3 thấy sinh ra hỗn hợp khí gồm 0,03 mol NO2 và 0,02 mol NO. Xác định khối lượng Fe đã phản ứng.
 Xem đáp án
Xem đáp án
Sử dụng phương trình cho - nhận e và áp dụng ĐLBTĐT, ta có :
Fe→ Fe3+ + 3e
0,03 ← 0,09
⟹ Khối lượng Fe phản ứng : mFe = 1,68 (g).