Giải SGK Hoá học 11 Kết nối tri thức Bài 25: Ôn tập chương 6 có đáp án
-
138 lượt thi
-
9 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Cho bốn hợp chất sau: ethanol, propanal, acetone, acetic acid.
a) Chất nào trong các chất trên có nhiệt độ sôi cao nhất?
b) Trình bày cách phân biệt các chất trên bằng phương pháp hoá học.
 Xem đáp án
Xem đáp án
a) Trong 4 chất trên acetic acid có nhiệt độ sôi cao nhất. Do phân tử acetic acid chứa nhóm carbonyl phân cực, các phân tử carboxylic acid liên kết hydrogen với nhau tạo thành dạng dimer hoặc dạng liên phân tử.
b) Cách phân biệt: ethanol, propanal, acetone, acetic acid:
- Trích mẫu thử.
- Cho vào mỗi mẫu thử 1 mẩu quỳ tím:
+ Quỳ tím chuyển sang màu đỏ → acetic acid (CH3COOH).
+ Quỳ tím không đổi màu → ethanol, propanal, acetone (nhóm I).
- Cho từng mẫu thử ở nhóm I tác dụng với Na:
+ Mẩu Na tan dần, có khí thoát ra → ethanol (C2H5OH).
Phương trình hoá học: 2C2H5OH + 2Na → 2C2H5ONa + H2.
+ Không hiện tượng → propanal, acetone (nhóm II).
- Cho từng mẫu thử ở nhóm II tác dụng với dung dịch bromine:
+ Dung dịch bromine nhạt dần đến mất màu → propanal.
Phương trình hoá học:
CH3 – CH2 – CHO + Br2 + H2O → CH3 – CH2 – COOH + 2HBr.
+ Không hiện tượng → acetone.
Câu 2:
Viết công thức cấu tạo và gọi tên theo danh pháp thay thế của các aldehyde, ketone có công thức phân tử C4H8O và carboxylic acid có công thức phân tử C4H8O2.
 Xem đáp án
Xem đáp án
Các aldehyde, ketone có công thức phân tử C4H8O:
- Hợp chất aldehyde:
CH3 – CH2 – CH2 – CHO: butanal;
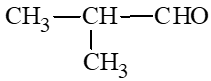 : 2 – methylpropanal;
: 2 – methylpropanal;- Hợp chất ketone:
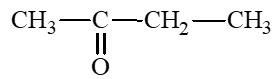 : butanone.
: butanone.Carboxylic acid có công thức phân tử C4H8O2
CH3 – CH2 – CH2 – COOH: butanoic acid;
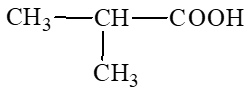 : 2 – methylpropanoic acid.
: 2 – methylpropanoic acid.Câu 3:
Viết công thức cấu tạo của các hợp chất có tên gọi dưới đây.
a) 3-methylbutanal;
b) pentan-2-one;
c) pentanoic acid;
d) 2-methylbutanoic acid.
 Xem đáp án
Xem đáp án
a) 3-methylbutanal:
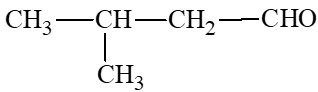
b) pentan-2-one:
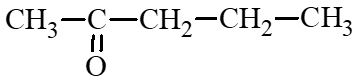
c) pentanoic acid: CH3 – CH2 – CH2 – CH2 – COOH.
d) 2-methylbutanoic acid.
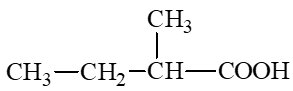
Câu 4:
Hãy viết các phương trình hoá học để chứng minh các aldehyde vừa có tính oxi hoá, vừa có tính khử.
 Xem đáp án
Xem đáp án
- Phương trình hoá học chứng minh aldehyde có tính oxi hoá:
CH3CHO + H2 CH3CH2OH
- Phương trình hoá học chứng minh aldehyde có tính khử:
CH3CHO + 2[Ag(NH3)2]OH CH3COONH4 + 2Ag + 3NH3 + H2O.
Câu 5:
Xác định sản phẩm của các phản ứng sau:
a) propanal + 2[H] →
b) ethanal + AgNO3 + NH3 + H2O →
c) butanone + HCN →
d) propanone + I2 + NaOH →
 Xem đáp án
Xem đáp án
Ta có các sơ đồ:
a) CH3CH2CHO CH3CH2CH2OH;
b) CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag + 2NH4NO3;
c) ![Xác định sản phẩm của các phản ứng sau: a) propanal + 2[H] → b) ethanal + AgNO3 + NH3 + H2O → c) butanone + HCN → d) propanone + I2 + NaOH → (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2023/03/blobid6-1679503883.png)
d) CH3 – CO – CH3 + 3I2 + 4NaOH → CH3 – COONa + 3NaI + CHI3 + 3H2O.
Câu 6:
Viết phương trình phản ứng giữa propanoic acid với các chất sau:
a) Zn;
b) MgO;
c) CaCO3;
d) CH3OH/ H2SO4 đặc.
 Xem đáp án
Xem đáp án
a) 2CH3 – CH2 – COOH + Zn → (CH3 – CH2 – COO)2Zn + H2;
b) 2CH3 – CH2 – COOH + MgO → (CH3 – CH2 – COO)2Mg + H2O;
c) 2CH3 – CH2 – COOH + CaCO3 → (CH3 – CH2 – COO)2Ca + CO2 + H2O;
d) CH3 – CH2 – COOH + CH3OH CH3 – CH2 – COOCH3 + H2O.
Câu 7:
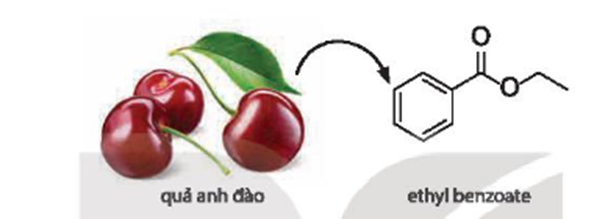
Ethyl benzoate là hợp chất chính tạo mùi thơm của quả anh đào (cherry). Hãy viết phương trình hoá học của phản ứng tổng hợp ethyl benzoate từ carboxylic acid và alcohol tương ứng.
 Xem đáp án
Xem đáp án
Câu 8:
Cho 12 g acetic acid phản ứng với 12 g ethanol (có H2SO4 đặc làm xúc tác) thu được 8 g ester. Tính hiệu suất phản ứng ester hoá.
 Xem đáp án
Xem đáp án
Phương trình hoá học:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
0,2 0,26 0,2 mol
Theo phương trình hoá học, giả sử H = 100% thì C2H5OH dư, do đó số mol ester theo lí thuyết sẽ tính theo số mol CH3COOH.
mester lý thuyết = 0,2 . 88 = 17,6 gam.
Hiệu suất phản ứng ester hoá là:
Câu 9:
Trong thành phần của bột vệ sinh lồng máy giặt thường có mặt nitric acid (acid chanh). Hãy giải thích vai trò của citric acid trong trường hợp này.
 Xem đáp án
Xem đáp án
Trong trường hợp này, citric acid đóng vai trò loại bỏ gỉ sét và cặn (CaCO3, MgCO3…) bám trên lồng máy giặt.
