Trắc nghiệm Sự điện ly có đáp án (Vận dụng)
-
850 lượt thi
-
13 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Hòa tan các chất sau vào nước để được các dung dịch riêng rẽ: NaCl, CaO, SO3, C6H12O6, CH3COOH, C2H5OH, Al2(SO4)3. Trong các dung dịch tạo ra có bao nhiêu dung dịch có khả năng dẫn điện?
 Xem đáp án
Xem đáp án
Các dung dịch có khả năng dẫn điện là các dung dịch tan trong nước phân li ra các ion
Đó là : NaCl; CaO; SO3; CH3COOH; Al2(SO4)3
CaO và SO3 tan vào nước xảy ra phản ứng:
CaO + H2O → Ca(OH)2 ; dd Ca(OH)2 thu được là bazo mạnh nên dẫn được điện
SO3 + H2O → H2SO4; dd H2SO4 thu được là axit mạnh nên dẫn được điện
Đáp án cần chọn là: A
Câu 2:
Cho các chất sau: SO2, C6H6 , C2H6, Ca(HCO3)2, H2SO4, NaClO, Mg(OH)2. Số chất hòa tan vào trong nước tạo thành chất điện li là:
 Xem đáp án
Xem đáp án
Các chất thỏa mãn: SO2 (tác dụng với nước tạo thành dung dịch axit), Ca(HCO3)2 ; H2SO4 ; NaClO ; Mg(OH)2 (phần hòa tan).
Vậy có 5 chất thỏa mãn.
Đáp án cần chọn là: B
Câu 3:
Có 4 dung dịch: Natri clorua, rượu etylic (C2H5OH), axit axetic (CH3COOH), kali sunfat đều có nồng độ 0,1 mol/l. Khả năng dẫn điện của các dung dịch đó tăng dần theo thứ tự nào trong các thứ tự sau:
 Xem đáp án
Xem đáp án
- C2H5OH tan trong nước nhưng không phân li ra ion=>không có khả năng dẫn điện.
- CH3COOH là chất điện li yếu =>dẫn điện yếu hơn so với 2 muối
Cùng nồng độ 0,1 mol/l thì: NaCl →Na+ + Cl− ; K2SO4 →2K+ + SO42−
K2SO4 phân li ra nhiều ion hơn nên dẫn điện mạnh hơn NaCl.
=> C2H5OH < CH3COOH < NaCl < K2SO4
Đáp án cần chọn là: B
Câu 4:
Hòa tan 6 gam NaOH vào 44 gam nước được dung dịch A có khối lượng riêng bằng 1,12 g/ml. Cần lấy bao nhiêu ml A để có số mol ion OH– bằng 2.10–3 mol
 Xem đáp án
Xem đáp án
mdd = mNaOH +![]() = 6+44 = 50(g)
= 6+44 = 50(g)
=> Vdd= m : d = 50 : 1,12 = ![]() (ml)
(ml)
nNaOH = ![]() = 0,15 (mol)
= 0,15 (mol)
=>CMNaOH = n : Vdd = ![]() = 3,36 (M)
= 3,36 (M)
NaOH → Na+ + OH−
Theo pt: nNaOH = nOH- = 2.10-3 (mol)
=> Thể tích dd A cần lấy là: V = n: CM = 2.10-3 : 3,36 = 6.10-4 lít = 0,6 ml
Đáp án cần chọn là: C
Câu 5:
Trộn 150 ml dung dịch MgCl2 0,5M với 50 ml dung dịch NaCl 1M thì nồng độ ion Cl- trong dung dịch mới là
 Xem đáp án
Xem đáp án
![]() = 0,15.0,5 = 0,075 mol; nNaCl = 0,05.1 = 0,05 mol
= 0,15.0,5 = 0,075 mol; nNaCl = 0,05.1 = 0,05 mol
MgCl2 và NaCl là các chất điện li mạnh, khi hòa tan vào nước phân li hoàn toàn thành các ion:
MgCl2 → Mg2+ + 2Cl-
0,075 → 0,15 (mol)
NaCl → Na+ + Cl-
0,05 → 0,05 (mol)
=> nCl- = 0,15 + 0,05 = 0,2 mol
=> [Cl-] = n : V = 0,2 : (0,15 + 0,05) = 1M
Đáp án cần chọn là: C
Câu 6:
Cho các mệnh đề sau
1 Chất điện ly mạnh có độ điện ly (α) > 1.
2 Chất điện ly mạnh có độ điện ly (α) = 1.
3 Chất không điện ly có độ điện ly (α) = 0.
4 Chất điện ly yếu có độ điện ly (α) = 1.
5 Chất điện ly yếu có độ điện ly 0 < (α) < 1.
Chọn đáp án đúng
 Xem đáp án
Xem đáp án
Mệnh đề đúng là (2), (3), (5)
Đáp án cần chọn là: B
Câu 7:
Trong các yếu tố sau
(1) Nhiệt độ
(2) Áp suất
(3) Xúc tác
(4) Nồng độ chất tan
(5) Diện tích tiếp xúc
(6) Bản chất chất điện li
Yếu tố nào ảnh hưởng đến hằng số điện li ?
 Xem đáp án
Xem đáp án
Hằng số điện ki (Kc) phụ thuộc vào nhiệt độ và bản chất của chất tan
Đáp án cần chọn là: B
Câu 8:
A là dung dịch HCl nồng độ 0,01M. Nồng độ của các ion trong dung dịch khi pha loãng A 100 lần là
 Xem đáp án
Xem đáp án
Khi pha loãng dung dịch 100 lần thì nồng độ các ion trong dung dịch cũng giảm 100 lần
HCl→H+ + Cl−
Trước khi pha loãng: [H+] = [Cl−] = 0,0 1M
Sau khi pha loãng: [H+] = [Cl−] = 1,0.10−4M => chọn B
Đáp án cần chọn là: B
Câu 9:
Độ điện li của dung dịch axit HCOOH 0,005M (biết trong dung dịch có [H+] = 0,001M) là
 Xem đáp án
Xem đáp án
HCOOH ⇆ HCOO- + H+
Ban đầu: 0,005M 0
Phân li: 0,005α M → 0,005α M
Cân bằng: 0,005(1-α) M 0,005α M
Vì [H+] = 0,001 → 0,005α = 0,001 → α = 0,2
Đáp án cần chọn là: B
Câu 10:
Tính nồng độ mol của CH3COOH, CH3COO− và H+ trong dung dịch CH3COOH 0,056M, biết rằng độ điện li α của CH3COOH bằng 20%.
 Xem đáp án
Xem đáp án
HCOOH ⇆ HCOO- + H+
Nồng độ ban đầu(mol/l) 0,056 0 0
Nồng độ phân li (mol/l) x x x
Nồng độ cân bằng(mol/l) 0,056-x x x
Độ điện li : α= ![]() . 100% = 20%
. 100% = 20%
=> x=0,0112( M) => [CH3COO-] = 0,0112M; [H+] = 0,0112M
[CH3COOH] = 0,056 - 0,0112 = 0,0448M
Đáp án cần chọn là: D
Câu 11:
Dung dịch HF 0,02M có độ điện li α = 0,015. Nồng độ ion H+ có trong dung dịch là
 Xem đáp án
Xem đáp án
Độ điện li α = 0,015 → [HF]phân li = 0,015.0,02 = 3.10-4 M
HF ⇆ H+ + F-
Ban đầu: 0,02M 0
Phân li: 3.10-4 M → 3.10-4 M
Cân bằng: 0,0197 M 3.10-4 M
Đáp án cần chọn là: A
Câu 12:
Dung dịch BaCl2 2M có nồng độ mol/l của anion là
 Xem đáp án
Xem đáp án
Theo định luật bảo toàn nguyên tố:
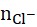 =
=![]()
Mặt khác BaCl2 là chất điện li mạnh, phân li hoàn toàn thành các ion => [Cl-] = 2.CM dd BaCl2 = 4M
Đáp án cần chọn là: A
