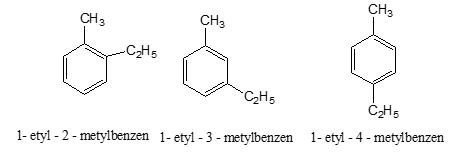
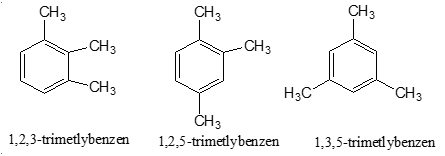
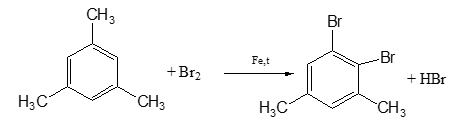Trắc nghiệm chuyên đề Hóa 11 Chủ đề 6. Phản ứng oxi hóa benzen và đồng đẳng có đáp án
Trắc nghiệm chuyên đề Hóa 11 Chủ đề 6. Phản ứng oxi hóa benzen và đồng đẳng có đáp án
-
526 lượt thi
-
14 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Chất A là một đồng đẳng của benzen. Khi đốt cháy hoàn toàn 1,5 g chất A, người ta thu được 2,52 lít khí CO2 ( đktc).
a. Xác định CTPT.
 Xem đáp án
Xem đáp án
Cứ ( 14n -6)g A tạo ra n mol CO2
Cứ 1,5g A tạo ra
CTPT: C9H12
Câu 4:
Đốt cháy hết 9,18 g 2 đồng đẳng của benzen A, B thu được 8,1 g H2O và CO2. Dẫn toàn bộ lượng CO2 vào 100ml dd NaOH 1M thu được m g muối. Giá trị của m và thành phần của muối:
 Xem đáp án
Xem đáp án
mC = 9,18 – 0,45.2 = 8,28 gam; = 0,69 mol; T = = 0,14 ⇒ tạo muối NaHCO3
= 0,1. 84 = 8,4 g
Câu 5:
Để oxi hoá hết 10,6 gam o-xylen (1,2-đimetylbenzen) cần bao nhiêu lít dung dịch KMnO4 0,5M trong môi trường H2SO4 loãng. Giả sử dùng dư 20% so với lượng phản ứng.
 Xem đáp án
Xem đáp án
no-Xilen = = 0,1 mol ⇒ pư = 0,1.2 = 0,2 mol; dùng dư 20%
⇒ = = 0,24 mol ⇒ V = = 0,48 lít.
Câu 6:
Đốt cháy hết 9,18 g 2 đồng đẳng của benzen A, B thu được H2O và 30,36 g CO2. Cộng thức phân tử của A và B lần lượt là:
 Xem đáp án
Xem đáp án
= 0,36 mol ⇒ nhh = ⇒ M = ⇒ ntb = 8,625 ⇒ CTPT A và B là: C8H10; C9H12
Câu 7:
Đốt cháy hoàn toàn 9,2g một ankyl benzen A thu được 30,8g CO2. Công thức phân tử của A là:
 Xem đáp án
Xem đáp án
Đáp án: C
= 0,7 mol; MA = 13,1n ⇒ n = 7
Câu 8:
Đốt cháy 12,72 g A (CxHy) → 10,8g H2O. A có chứa 1 vòng benzen. Công thức phân tử của A là:
 Xem đáp án
Xem đáp án
Đáp án: C
= 0,6 mol; MA =⇒ n = 8
Câu 9:
Đốt cháy hoàn toàn m g A đồng đẳng của benzen thu được 20,16 lít CO2 (đktc) và 10,8 ml H2O (lỏng). Công thức của A là:
 Xem đáp án
Xem đáp án
Đáp án: C
= 0,9 mol; = 0,6 mol; ⇒ n = 9
Câu 10:
Đốt cháy hoàn toàn 0,1 mol CxHy thu được 15,68 lít CO2 (đktc) và 7,2 g H2O (lỏng). Công thức của CxHy là:
 Xem đáp án
Xem đáp án
Đáp án: A
= 0,7 mol; = 0,4 mol; ⇒ x = 7; y = 8
Câu 11:
Đốt cháy hết m gam 2 đồng đẳng của benzen A, B thu được 4,05 gam H2O và 7,728 lítCO2 (đktc). Giá trị của m và số tổng số mol của A, B là:
 Xem đáp án
Xem đáp án
Đáp án: A
= 0,345 mol; = 0,225 ⇒ m= mC + mH = 0,345.12 + 0,225.2 = 4,59 g;
n == 0,04 mol
Câu 12:
Đốt cháy hoàn toàn ankybenzen X thu được 7,84 lít CO2 (đktc) và 3,6 gam H2O. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Đáp án: B
Đặt CTPT X là CnH2n-6
3nX = = 0,35 – 0,2 = 0,15 mol → nX = 0,05 mol
→ 0,05n = 0,35 → n = 7 → CTPT C7H8
Câu 13:
Đốt cháy hoàn toàn Hiđrocacbon X, thu đuộc CO2 và H2O có số mol theo tỉ lệ tương ứng 2 : 1. Mặt khác, 1 mol X tác dụng được tối đa với 4 mol H2 (Ni, t°) : 1 mol X tác dụng được tối đa 1 mol Br2. Công thức của X là.
 Xem đáp án
Xem đáp án
Đáp án: D
nC : nH = 2 : (1.2) = 1 : 1 → CTPT: CnHn
1 mol X + 4 mol H2 (Ni, to); 1 mol X + 1 mol Br2
→ X chứa vòng benzen + 1 liên kết đôi ở nhánh → k = 5
CTPT X: CnH2n+2-2k → 2n + 2 – 2k = n → k = 5; n = 8 → CTPT: C8H8
Câu 14:
Đốt cháy hoàn toàn 5,3 gam ankybenzen X thu được 8,96 lít CO2 (đktc). Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Đáp án: D
Đặt CTPT X là CnH2n-6
→ CTPT: C8H10