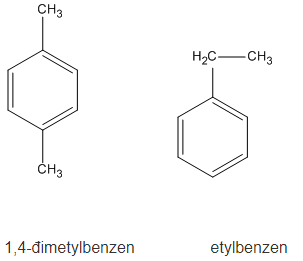
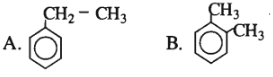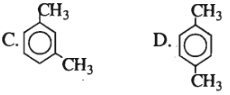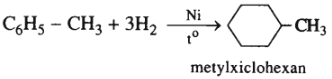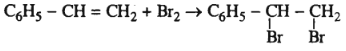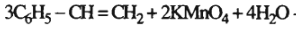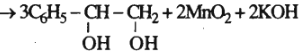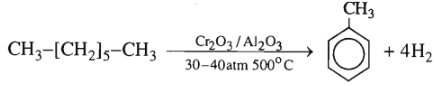Giải SBT Hóa học 11 Chương 7: Hidrocacbon thơm. Nguồn hidrocacbon thiên nhiên. Hệ thống hóa về hidrocacbon
Bài 35: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác - SBT Hóa học 11
-
1068 lượt thi
-
12 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 3:
Stiren có công thức phân tử C8H8 và có công thức cấu tạo: C6H5-CH=CH2. Nhận xét nào cho dưới đây đúng ?
 Xem đáp án
Xem đáp án
Đáp án: C
Câu 5:
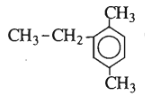
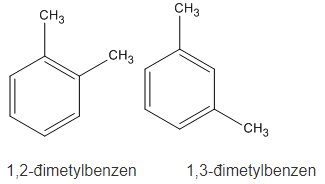
Có bao nhiêu chất đồng đẳng của benzen có cùng công thức phân tử C9H12
 Xem đáp án
Xem đáp án
Đáp án: C.
8 chất gồm: 2 chất C6H5C3H7; 3 chất C2H5-C6H4-CH3 và 3 chất C6H3(CH3)3
Câu 6:
Hoàn thành các phương trình hoá học dưới đây. Viết các chất sản phẩm hữu cơ ở dạng công thức cấu tạo và kèm theo tên.
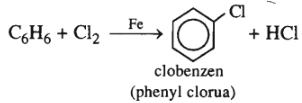
1. C6H6 + Cl2 Fe→
(1 mol) (1 mol)
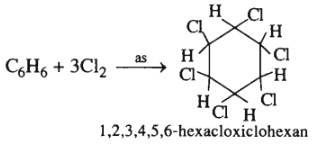
2. C6H6 + Cl2 as→
(1 mol) 3 mol)
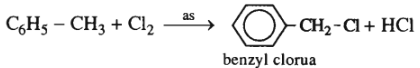
3. C6H5−CH3 + Cl2 as→
(1 mol) (1 mol)
4. C6H5−CH3 + H2 (dư) Ni, 300oC→
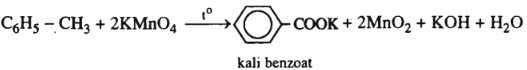
5. C6H5−CH3 + KMnO4 (dd) to→
 Xem đáp án
Xem đáp án
1.
2.
3.
4.
5.
Câu 7:
Benzen không tác dụng với dung dịch Br2 và dung dịch KMnO4 nhưng stiren thì có phản ứng với cả hai dung dịch đó.
1. Giải thích vì sao stiren có khả năng phản ứng đó.
2. Viết phương trình hoá học biểu diễn các phản ứng đó.
 Xem đáp án
Xem đáp án
1. Vì stiren có liên kết đôi ở nhánh vinyl.
2.
Câu 8:
Chất A là một đồng đẳng của benzen. Để đốt cháy hoàn toàn 13,25 g chất A cần dùng vừa hết 29,40 lít O2 (đktc).
1. Xác định công thức phân tử chất A.
2. Viết các công thức cấu tạo có thể có của chất A. Ghi tên ứng với mỗi công thức cấu tạo đó.
 Xem đáp án
Xem đáp án
1.
Theo phương trình:
Cứ (14n - 6)g A tác dụng với mol O2
Theo đầu bài:
Cứ 13,24g A tác dụng với mol O2
Ta có
⇒ n = 8 ⇒ CTPT: C8H10
2. Các công thức cấu tạo
Câu 9:
Khi đốt cháy hoàn toàn hiđrocacbon A, thu được khí CO2 và hơi nước theo tỉ lệ 77 : 18 về khối lượng. Nếu làm bay hơi hết 5,06 gam A thì thể tích hơi thu được đúng bằng thể tích của 1,76 g O2 ở cùng nhiệt độ và áp suất.
1. Xác định công thức phân tử của chất A.
2. Chất A không tác dụng với nước brom nhưng tác dụng được với dung dịch KMnO4 khi đun nóng. Viết công thức cấu tạo và tên chất A.
 Xem đáp án
Xem đáp án
1.
Theo đầu bài ta có:
Tức là 12x + y = 92,0 ⇒ x = 7 ; y = 8
Công thức phân tử chất A là C7H8.
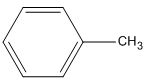
2. Công thức cấu tạo
Câu 10:
Hỗn hợp M ở thể lỏng, chứa hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Đốt cháy hoàn toàn 2,62 g M, thu được 8,8 g CO2.
Nếu làm bay hơi hết 6,55 gam M thì thể tích hơi thu được đúng bằng thể tích của 2,4 g khí oxi ở cùng điều kiện.
Xác định công thức phân tử và phần trăm (về khối lượng) của từng chất trong hỗn hợp M.
 Xem đáp án
Xem đáp án
Số mol 2 chất trong 6,55 g M là:
Số mol 2 chất trong 2,62 g M là:
Giả sử trong 2,62 g M có a mol CxHy và b mol Cx+1Hy+2
xa + (x + 1)b = 0,2 (3)
Từ (3), ta có x(a + b) + b = 0,2
b = 0,2 - 0,03x
Vì 0 < b < 0,03 nên 0 < 0,2 - 0,03x < 0,03.
⇒ 5,67 < x < 6,67 ⇒ x = 6 .
b = 0,2 - 0,03.6 = 0,02; a = 0,03 - 0,02 = 0,01
Thay giá trị của a và b vào (2), tìm được y = 6.
Khối lương C6H6 chiếm
Khối lương C7H8 chiếm 100 - 29,8% = 70,2%.
Câu 11:
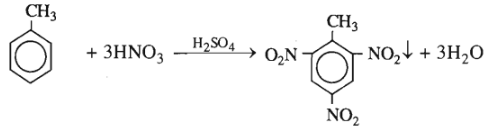
Cho 23 kg toluen tác dụng với hỗn hợp gồm 88 kg axit nitric 66% và 74 kg axit suníuric 96%. Giả sử toluen được chuyển hoàn toàn thành trinitrotoluen và sản phẩm này được tách hết khỏi hỗn hợp axit còn dư. Tính:
1. Khối lượng trinitrotuluen thu được.
2. Khối lượng hỗn hợp axit còn dư và nồng độ phần trăm của từng axit trong hỗn hợp đó.
 Xem đáp án
Xem đáp án
1. Số mol TNT = số mol toluen =
Khối lượng TNT =
2. Khối lượng hỗn hợp axit còn lại sau phản ứng :
23 + 88 + 74 - 5675.10-2 = 12825.10−2 (kg)
Khối lương HNO3 trong đó :
C% của HNO3 là:
Khối lương H2SO4 là:
C% của H2SO4 là:
Câu 12:
Có thể điều chế toluen bằng phản ứng đehiđro hoá - đóng vòng đối với heptan ở 500oC, 30 - 40 atm, chất xúc tác Cr2O3 / Al2O3.
1. Viết phương trình hoá học của phản ứng (các chất hữu cơ viết bằng công thức cấu tạo).
2. Tính khối lượng toluen thu được nếu phản ứng tạo ra 336 lít H2 (đktc).
 Xem đáp án
Xem đáp án
1.
2. Số mol toluen = số mol H2 / 4
Khối lượng toluen là: 3,75.92 = 345 (g).