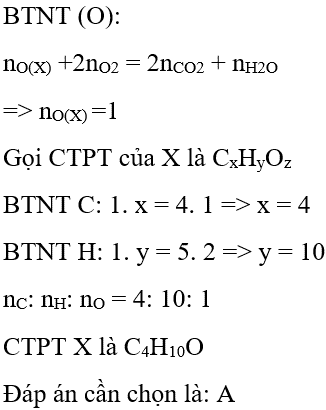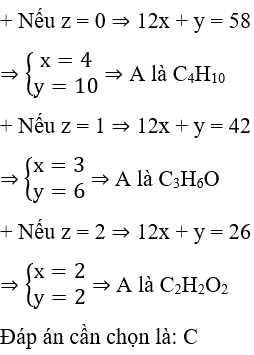Trắc nghiệm Công thức phân tử hợp chất hữu cơ có đáp án (Thông hiểu)
-
3082 lượt thi
-
15 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
Một hiđrocacbon A có M = 26. Phân tích 1 gam A thu được gam hiđro. Trong X có số nguyên tử H là
 Xem đáp án
Xem đáp án
1 gam X chứa gam H
=> 26 gam X chứa 2 gam H
=> nH = mH : MH = 2 : 1 = 2
=> Số nguyên tử H trong 1 phân tử X là 2
Đáp án cần chọn là: A
Câu 2:
Một hidrocacbon X có M = 58, phân tích 1 gam X thu được gam hidro. Trong X có số nguyên tử H là:
 Xem đáp án
Xem đáp án
1 gam X chứa gam H
=> 58 gam X chứa 10 gam H
=> nH = mH : MH = 10 : 1 = 10
=> Số nguyên tử H trong 1 phân tử X là 10
Đáp án cần chọn là: A
Câu 4:
Đốt cháy hoàn toàn 3 gam hợp chất hữu cơ X thu được 4,4 gam CO2 và 1,8 gam H2O. Biết tỉ khối của X so với He là 7,5. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
nC= = 0,1 mol => mC= 1,2 g
nH=2 = 0,2 mol => mH= 0,2 g
mO= mX – mC – mH = 1,6 g => nO = 0,1 mol
nC: nH: nO = 0,1 : 0,2 : 0,1 => CTĐGN X: (CH2O)n
MX = 30 <=> 30n = 30 => n = 1
Vậy CTPT của X là CH2O
Đáp án cần chọn là: D
Câu 12:
Oxi hóa hoàn toàn 4,02 gam một hợp chất hữu cơ X chỉ thu được 3,18 gam Na2CO3 và 0,672 lít khí CO2. CTĐGN của X là:
 Xem đáp án
Xem đáp án
nNa2CO3 = 0,03 mol; nCO2 = 0,03 mol
Vì đốt cháy X thu được CO2 và Na2CO3 => trong X chứa C, Na có thể có O
Bảo toàn nguyên tố Na: nNa(trongX) = 2. = 0,06 mol
Bảo toàn nguyên tố C: nC(trongX) = + = 0,03 + 0,03 = 0,06 mol
⇒ nO(trongX) = = 0,12 mol
nC : nNa : nO = 0,06 : 0,06 : 0,12 = 1 : 1 : 2
Vậy CTĐGN của X là: CNaO2.
Đáp án cần chọn là: A
Câu 13:
Đốt cháy hoàn toàn 1,605 gam hợp chất hữu cơ A thu được 4,62 gam CO2; 1,215 gam H2O và 168 ml N2 (đktc). Tỷ khối hơi của A so với không khí không vượt quá 4. Công thức phân tử của A là
 Xem đáp án
Xem đáp án
Vì đốt cháy X thu được CO2 và H2O và N2 => trong X chứa C, H, N có thể có O
nC = = 4,62 : 44 = 0,105 mol
nH = 2= 2. (1,215: 18) = 0,135 mol
nN = 2 = 0,015 mol
mC + mH + mN = 1,605 => Trong A không có O
= 0,105: 0,135: 0,015= 7: 9: 1
Vậy CTPT của A là C7H9N
Đáp án cần chọn là: C
Câu 15:
Đốt cháy hoàn toàn 0,6 gam hợp chất hữu cơ X rồi cho sản phẩm cháy qua bình đựng dung dịch Ca(OH)2 dư thấy có 2 gam kết tủa và khối lượng bình tăng thêm 1,24 gam. Tỷ khối của X so với H2 bằng 15. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Các phản ứng xảy ra:
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
mol: 0,02 ← 0,02
Khối lượng bình tăng = + = 1,24 gam
⇒ = 1,24 − 0,02.44 = 0,36 gam
⇒ nH = 2. = 0,04 mol
nO = = 0,02 mol
⇒ nC : nH : nO = 0,02 : 0,04 : 0,02 = 1 : 2 : 1
Vậy CTĐGN của X là (CH2O)n
Do MX = 30 <=> 30n = 30 => n = 1. Vậy CTPT của X là CH2O
Đáp án cần chọn là: B