Đề thi Học kì 2 Hóa học 10 cực hay có đáp án (Đề 17)
-
7183 lượt thi
-
20 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Tác nhân chủ yếu gây mưa axit là:SO2và NO2.
Câu 2:
Cho các chất: S, SO2, H2S, H2SO4. Trong số 4 chất đã cho, số chất vừa có tính oxi hóa, vừa có tính khử là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:A
Các chất vừa có tính oxi hóa, vừa có tính khử là: S; SO2; H2S.
+ Trong đơn chất S thì S có số oxi hóa 0, đây là số oxi hóa trung gian, do đó S vừa có tính oxi hóa, vừa có tính khử.
+ Trong SO2thì S có số oxi hóa +4, đây là số oxi hóa trung gian của lưu huỳnh, do đó SO2vừa có tính oxi hóa, vừa có tính khử.
+ Trong H2S, tính khử gây ra bởi S-2; tính oxi hóa gây ra bởi H+1.
Câu 3:
Halogen ở thể rắn (điều kiện thường), có tính thăng hoa là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:C
Halogen ở thể rắn (điều kiện thường), có tính thăng hoa là: iot.
Câu 4:
Các số oxi hóa của lưu huỳnh là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:C
Các số oxi hóa của lưu huỳnh là -2, 0, +4, +6
Câu 5:
Các kim loại thụ động với H2SO4đặc nguội là
 Xem đáp án
Xem đáp án
Đáp án đúng là:C
Các kim loại thụ động với H2SO4đặc nguội là: Al, Fe.
Câu 6:
Axit halogenhiđric nào là axit mạnh nhất?
 Xem đáp án
Xem đáp án
Đáp án đúng là:A.
Axit halogenhiđric mạnh nhất là: HI.
Câu 7:
Khi đốt cháy khí hidro sunfua trong điều kiện dư oxi thì sản phẩm cháy thu được gồm các chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là:A
Khi đốt cháy khí hidrosunfua trong điều kiện dư oxi thì sản phẩm cháy thu được gồm: H2O và SO2
2H2S + 3O2 2SO2+ 2H2O
2SO2+ 2H2O
Câu 8:
Khí HCl khô khi gặp quỳ tím thì làm quỳ tím
 Xem đáp án
Xem đáp án
Đáp án đúng là:D
Khí HCl khô khi gặp quỳ tím thì làm quỳ tím không chuyển màu.
Câu 9:
Chất khí màu xanh nhạt, có mùi đặc trưng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:B
Chất khí màu xanh nhạt, có mùi đặc trưng là:O3.
Câu 10:
Thành phần nước Gia-ven gồm:
 Xem đáp án
Xem đáp án
Đáp án đúng là:D
Thành phần nước Gia-ven gồm: NaCl, NaClO, H2O.
Câu 11:
Nguyên tố halogen nào có trong hợp chất tạo nên men răng của người và động vật?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Flo có trong hợp chất tạo nên men răng của người và động vật
Câu 12:
Ở điều kiện thường, phi kim duy nhất ở thể lỏng là
 Xem đáp án
Xem đáp án
Đáp án đúng là:B
Ở điều kiện thường, phi kim duy nhất ở thể lỏng là: Brom.
Câu 13:
Mg + H2SO4(đặc)  MgSO4+ H2S + H2O. Hệ số cân bằng (là các số nguyên đơn giản nhất) của phản ứng lần lượt là
MgSO4+ H2S + H2O. Hệ số cân bằng (là các số nguyên đơn giản nhất) của phản ứng lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là:A
4Mg + 5H2SO4(đặc)  4MgSO4+ H2S + 4H2O
4MgSO4+ H2S + 4H2O
Câu 14:
Số oxi hoá của clo trong các chất: NaCl, NaClO, KClO3, Cl2, KClO4lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:B
Số oxi hoá của clo trong các chất: NaCl, NaClO, KClO3, Cl2, KClO4lần lượt là: –1, +1, +5, 0, +7.
Câu 15:
Các nguyên tử halogen có cấu hình electron lớp ngoài cùng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là:D
Các nguyên tử halogen có cấu hình electron lớp ngoài cùng là: ns2np5.
Câu 16:
Trong sản xuất, oxi được dùng nhiều nhất
 Xem đáp án
Xem đáp án
Đáp án đúng là:C
Trong sản xuất, oxi được dùng nhiều nhất để luyện thép.
Câu 17:
Hoàn thành các phương trình sau (ghi rõ điều kiện nếu có)
 Xem đáp án
Xem đáp án
a. 2Fe + 3Cl2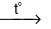 2FeCl3
2FeCl3
b. H2+ F2→ 2HF
c. 2Al + 3S 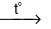 Al2S3
Al2S3
d. SO2 + H2O 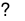 H2SO3
H2SO3
Câu 18:
Nhận biết các dung dịch mất nhãn sau bằng phương pháp hóa học:
, Na2SO4, HCl, HNO3
 Xem đáp án
Xem đáp án
Hướng dẫn giải
- Trích các mẫu thử
- Cho quỳ tím vào các mẫu thử:
+ HNO3và HCl làm quỳ tím hóa đỏ (1)
+ Na2SO4và NaNO3: không đổi màu quỳ tím (2)
- Cho AgNO3vào nhóm (1):
+ Xuất hiện kết tủa trắng → HCl
Phương trình phản ứng: HCl + AgNO3→ AgCl↓ + HNO3
+ Không phản ứng: HNO3
- Cho BaCl2vào mẫu thử nhóm (2):
+ Xuất hiện kết tủa trắng → Na2SO4
Phương trình phản ứng: BaCl2+ Na2SO4 → BaSO4↓ + 2NaCl
+ Không hiện tượng: NaNO3
Câu 19:
Hòa tan 24,9gam một oleum vào nước thu được dung dịch A. Để trung hòa A cần 600 ml dung dịch KOH 1M. Hãy xác định công thức của oleum?
 Xem đáp án
Xem đáp án
Hướng dẫn giải
Gọi công thức oleum là H2SO4.nSO3a mol
Hòa tan vào H2O tổng 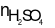 = (a + an) mol
= (a + an) mol
Có nKOHcần = 0,6 mol
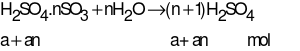


Suy ra a + an = 0,3 (1)
Mà moleum= 24,9= a(98 + 80n) (2)
Từ (1) và (2) suy ra a= 0,05 và an = 0,25
Suy ra n = 5
Vậy công thức của oleum H2SO4.5SO3
Câu 20:
Cho 25,20 gam hỗn hợp X gồm Zn, Mg và Al tác dụng với dung dịch H2SO4đặc nguội 98% (vừa đủ) thu được dung dịch Y; phần không tan Z và 8,96 lít khí SO2 (đktc). Cho phần không tan Z tác dụng hết với dung dịch HCl thu được 11,76 lít khí H2 (đktc) thu được dung dịch A. Tính nồng độ phần trăm của các chất trong dung dịch A?
 Xem đáp án
Xem đáp án
Al không tác dụng với H2SO4đặc nguội suy ra Z là Al (phần không tan)
Y: ZnSO4, MgSO4
2Al + 6HCl → 2AlCl3+ 3H2
Có  = 0,525 mol
= 0,525 mol
a. Có 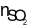 = 0,4 mol
= 0,4 mol

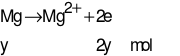
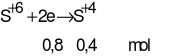
Suy ra 2x + 2y = 0,8 (1)
 ,
, 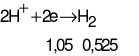
Có 3z = 1,05 ⇒ z = 0,35 mol
⇒ mAl= 0,35.27 = 9,45 gam.
Có 65x + 24y = 25,20 – 9,45 = 15,75 (2)
Từ (1) và (2) suy ra x = 0,15, y = 0,25
Vậy %mZn= 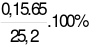 = 38,69%
= 38,69%
%mAl= 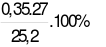 = 37,5%
= 37,5%
%mMg= 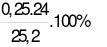 = 23,81%
= 23,81%
b. Dung dịch H2SO4đặc nguội 98%, có
 (trong muối) = 0,8 mol
(trong muối) = 0,8 mol
⇒ 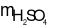 = 0,8.98 = 78,4 gam,
= 0,8.98 = 78,4 gam,
Vậy mdd(98%)= 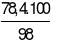 = 80 gam
= 80 gam
Dung dịch H2SO455%: 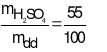 ⇒ mdd= 142,54 gam
⇒ mdd= 142,54 gam
Suy ra  (cần thêm) = 142,54 – 80 = 62,54 gam
(cần thêm) = 142,54 – 80 = 62,54 gam
Vậy thể tích nước cần dùng để pha loãng là: 62,54 ml.
c. Ta có: mdd= D.V = 1,20.105 = 126 g.
20% = 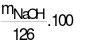 ⇒ mNaOH= 25,2 gam ⇒ nNaOH= 0,63 mol
⇒ mNaOH= 25,2 gam ⇒ nNaOH= 0,63 mol
Phương trình phản ứng:

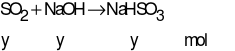
Có 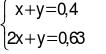
Giải hệ được x = 0,23, y = 0,17
⇒  = 0,23.126 = 28,98 gam,
= 0,23.126 = 28,98 gam, 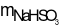 = 0,17.104 = 17,68
= 0,17.104 = 17,68
Vậy 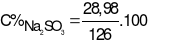 %= 23%
%= 23%
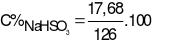 % = 14,03%
% = 14,03%
