Đề thi cuối kì 2 Hóa 11 có đáp án (Đề 9)
-
8290 lượt thi
-
8 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
CH ≡ CH  CH3CHO
CH3CHO  C2H5OH
C2H5OH  CH3COOH
CH3COOH  CH3COONa
CH3COONa  NaCl
NaCl
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
(1) CH≡CH + H2O 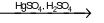 CH3CHO
CH3CHO
(2) CH3CHO + H2 CH3CH2OH
CH3CH2OH
(3) C2H5OH + CuO  CH3CHO + Cu + H2O
CH3CHO + Cu + H2O
(4) C2H5OH + O2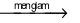 CH3COOH + H2O
CH3COOH + H2O
(5) CH3COOH + NaOH → CH3COONa + H2O
(6) CH3COONa + HCl → CH3COOH + NaCl
Câu 2:
a) CH3-CH2-CH2-OH 
b) CH3COOH + C2H5OH 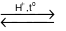
c) CH3OH 
d) CH3COOH + Mg →
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
a) CH3-CH2-CH2-OH  CH3-CH=CH2+ H2O
CH3-CH=CH2+ H2O
b) CH3COOH + C2H5OH  CH3COOC2H5+ H2O
CH3COOC2H5+ H2O
c) 2CH3OH  CH3-O-CH3+ H2O
CH3-O-CH3+ H2O
d) 2CH3COOH + Mg → (CH3COO)2Mg + H2↑
Câu 3:
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
Nhận biết: CH3OH, CH3CHO, C2H4(OH)2, CH3COOH.
- Đánh số thứ tự từng bình mất nhãn, trích mỗi bình một ít sang ống nghiệm đánh số tương ứng (trích mẫu thử).
- Dùng quỳ tím:
+ Dung dịch làm quỳ tím hóa đỏ là CH3COOH.
+ Dung dịch không làm đổi màu quỳ tím: CH3OH, CH3CHO, C2H4(OH)2(nhóm I)
- Dùng dung dịch AgNO3/NH3thực hiện phản ứng tráng gương với các dung dịch ở nhóm I.
+ Thấy xuất hiện kết tủa là CH3CHO.
CH3CHO + 2AgNO3+ H2O + 3NH3→ CH3COONH4+ 2NH4NO3+ 2Ag↓
+ Không có hiện tượng gì là: CH3OH, C2H4(OH)2(nhóm II)
Dùng Cu(OH)2phản ứng với lần lượt từng dung dịch ở nhóm II.
+ Thấy tạo thành dung dịch màu xanh thẫm đặc trưng là C2H4(OH)2.
2C2H4(OH)2+ Cu(OH)2→ [C2H4(OH)O]2+ 2H2O
+ Không có hiện tượng gì là CH3OH.
Câu 4:
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
Axit axetic (CH3COOH) là một axit yếu, nhưng vẫn mạnh hơn axit cacbonic (H2CO3); còn phenol (C6H5OH) là một axit yếu hơn axit cacbonic.
→ So sánh tính axit: CH3COOH >H2CO3>C6H5OH.
Phương trình hóa học chứng minh:
2CH3COOH + Na2CO3→ 2CH3COONa + CO2↑ + H2O
C6H5ONa + CO2+ H2O → C6H5OH + NaHCO3
Câu 5:
Tên | Công thức cấu tạo | ||
1 | Axit metanoic | A | CH3CHO |
2 | Ancol isopropylic | B | CH3 –CH(CH3)- CHO |
3 | Etanal | C | (CH3)2CH-OH |
4 | Metanol | D | HCOOH |
5 | 3-metylbutanal | E | CH3OH |
6 | 2-metylpropanal | F | CH3-CH(CH3)-CH2-CHO |
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
1D, 2C, 3A, 4E, 5F, 6B.
Axit metanoic: HCOOH
Ancol isopropylic: (CH3)2CH-OH
Etanal: CH3CHO
Metanol: CH3OH
3-metylbutanal: CH3-CH(CH3)-CH2-CHO
2-metylpropanal: CH3 –CH(CH3)- CHO
Câu 6:
- X có rất nhiều ứng dụng trong đời sống như làm nhiên liệu, sản xuất mĩ phẫm, thức uống… và X chiếm 5% về thể tích trong xăng E5.
- Y là một chất lỏng có vị chua, có thể được điều chế từ X bằng phương pháp lên men.
- Z dễ tan trong nước tạo dung dịch có tính kháng khuẩn, thường được sử dụng làm chất bảo quản với các mẫu vật (ướp xác).
Xác định công thức cấu tạo của X, Y, Z và sắp xếp X, Y, Z theo thứ tự tăng dần nhiệt độ sôi.
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
X có rất nhiều ứng dụng trong đời sống như làm nhiên liệu, sản xuất mĩ phẫm, thức uống… và X chiếm 5% về thể tích trong xăng E5.
→ X là C2H5OH (ancol etylic).
Y là một chất lỏng có vị chua, có thể được điều chế từ X bằng phương pháp lên men.
→ Y là CH3COOH (axit axetic)
Điều chế Y bằng phương pháp lên men X:
C2H5OH + O2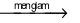 CH3COOH + H2O.
CH3COOH + H2O.
Z dễ tan trong nước tạo dung dịch có tính kháng khuẩn, thường được sử dụng làm chất bảo quản với các mẫu vật (ướp xác).
→ Z là HCHO (fomanđehit).
→ So sánh nhiệt độ sôi: CH3COOH (Y) >C2H5OH (X) >HCHO (Z).
Câu 7:
a) Tính số mol mỗi chất trong hỗn hợp B.
b) Để tác dụng hoàn toàn với 32,6 gam hỗn hợp B cần bao nhiêu mol dung dịch Br2?
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
a) Phương trình hóa học:
HCOOH + NaOH → HCOONa + H2O
x x (mol)
C6H5OH + NaOH → C6H5ONa + H2O
Y y (mol)
Gọi số mol của HCOOH và C6H5OH trong B lần lượt là x, y (mol).
Ta có hệ phương trình:
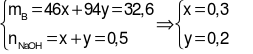 .
.
b) Phương trình hóa học:
HCOOH + Br2→ 2HBr + CO2
0,3 0,3 (mol)
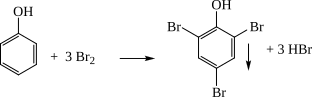
0,2 0,6 (mol)
→  = 0,3 + 0,6 = 0,9 (mol).
= 0,3 + 0,6 = 0,9 (mol).
Câu 8:
 Xem đáp án
Xem đáp án
Hướng dẫn giải:
X (ROH) phản ứng với Na:
2ROH + 2Na → 2RONa + H2↑.
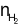 = 0,1 (mol) → nX= 2
= 0,1 (mol) → nX= 2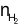 = 20,1 = 0,2 (mol).
= 20,1 = 0,2 (mol).
Đốt cháy X:
X + O2 CO2+ H2O.
CO2+ H2O.
X là ancol no, đơn chức → nX=  = 0,2 (*)
= 0,2 (*)
 = 53,2 (gam) →
= 53,2 (gam) → 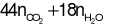 = 53,2 (**)
= 53,2 (**)
Từ (*) và (**), suy ra: 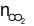 = 0,8 (mol);
= 0,8 (mol);  = 1 (mol).
= 1 (mol).
→ Số C(X)= 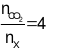 ; Số H(X)=
; Số H(X)= 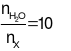 .
.
→ Công thức phân tử của X là C4H10O.
X là ancol bậc 3 → Công thức cấu tạo của X là:
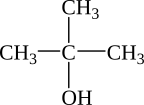
Cho Na=23; Br=80; C=12; O=16; H=1; N=14
