(2023) Đề thi thử Hóa học Sở giáo dục và đào tạo Bắc Kạn (Lần 1) có đáp án
(2023) Đề thi thử Hóa học Sở giáo dục và đào tạo Bắc Kạn (Lần 1) có đáp án
-
203 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 4:
Nếu thuỷ phân không hoàn toàn pentapeptit Gly-Ala-Gly-Val-Ala thì thu được tối đa bao nhiêu đipeptit mạch hở chứa Gly?
 Xem đáp án
Xem đáp án
Sản phẩm chứa tối đa 3 đipeptit mạch hở chứa Gly là:
Gly-Ala; Ala-Gly; Gly-Val
Chọn C
Câu 5:
Cho dãy các kim loại: Fe, Na, K, Ca. Số kim loại trong dãy tác dụng được với nước ở nhiệt độ thường là
 Xem đáp án
Xem đáp án
Có 3 kim loại trong dãy tác dụng được với nước ở nhiệt độ thường là: Na, K, Ca.
Chọn B
Câu 6:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
A. Sai, amilozơ có cấu trúc mạch không phân nhánh.
B. Sai, poliacrilonitrin được điều chế bằng phản ứng trùng hợp CH2=CH-CN
C. Đúng
D. Sai, poli(vinyl clorua) được điều chế bằng phản ứng trùng hợp CH2=CH-Cl
Chọn C
Câu 7:
X, Y là hai cacbohiđrat. X, Y đều không bị oxi hóa bởi AgNO3/NH3. Khi thủy phân hoàn toàn X hoặc Y trong môi trường axit đều thu được một chất hữu cơ Z duy nhất. X, Y lần lượt là
 Xem đáp án
Xem đáp án
X, Y tham gia phản ứng thủy phân tạo một chất hữu cơ Z duy nhất và X, Y không tráng gương → Chọn X, Y là tinh bột và xenlulozơ.
Chọn D
Câu 8:
Trước đây có rất nhiều vụ tử vong thương tâm xảy ra do sử dụng bếp than tổ ong để sưởi ấm trong nhà vào mùa đông. Nguyên nhân là do hàm lượng khí độc X trong không khí cao vượt mức cho phép. X là khí nào sau đây?
 Xem đáp án
Xem đáp án
Chọn C
Câu 16:
Người ta gắn tấm kẽm vào vỏ ngoài của tàu thủy ở phần chìm trong nước biển để
 Xem đáp án
Xem đáp án
Người ta gắn tấm kẽm vào vỏ ngoài của tàu thủy ở phần chìm trong nước biển để chống ăn mòn kim loại bằng phương pháp điện hóa vì Zn có tính khử mạnh hơn Fe nên Zn là cực âm và bị ăn mòn, Fe là cực dương và được bảo vệ.
Chọn D
Câu 18:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
A. Đúng, saccarozơ có nhiều nhóm OH kề nhau nên có tính chất của ancol đa chức: phản ứng với Cu(OH)2 tạo dung dịch màu xanh lam.
B. Sai
C. Sai, xenlulozơ không bị thuỷ phân trong dung dịch kiềm đun nóng.
D. Sai, glucozơ là monosaccarit nên không bị thủy phân.
Chọn A
Câu 19:
Kim loại nào sau đây có thể dát thành lá mỏng 0,01 nm và dùng làm giấy gói kẹo, gói thuốc lá?
 Xem đáp án
Xem đáp án
Chọn D
Câu 21:
Thủy phân hoàn toàn hỗn hợp etyl axetat và metyl axetat trong dung dịch NaOH, thu được sản phẩm gồm
 Xem đáp án
Xem đáp án
CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
CH3COOCH3 + NaOH → CH3COONa + CH3OH
→ Sản phẩm có 1 muối + 2 ancol
Chọn C
Câu 23:
Vào mùa lũ, để có nước sử dụng, dân cư ở một số vùng thường sử dụng chất X (có công thức K2SO4.Al2(SO4)3.24H2O) để làm trong nước. Chất X được gọi là
 Xem đáp án
Xem đáp án
Chọn D
Câu 24:
Supephotphat kép được sản xuất từ H2SO4 đặc và nguyên liệu là quặng photphorit (chứa 40% Ca3(PO4)2, còn lại là tạp chất không chứa photpho). Từ 465 tấn quặng photphorit ở trên sản xuất được tối đa m tấn supephotphat kép có độ dinh dưỡng 50%. Biết hiệu suất của cả quá trình sản xuất là 90%. Giá trị gần nhất của m là
 Xem đáp án
Xem đáp án
mCa3(PO4)2 = 465.40% = 186 tấn
Bảo toàn P → nP2O5 = nCa3(PO4)2 = 0,6
→ m phân = 0,6.142.90%/50% = 153,36 tấn
Chọn B
Câu 25:
Cho 5,34 gam hỗn hợp X chứa ba amin no, đơn chức, mạch hở tác dụng vừa đủ với HCl thu được 8,99 gam muối. Mặt khác, đốt cháy hoàn toàn lượng X trên thu được a mol khí N2. Giá trị của a là
 Xem đáp án
Xem đáp án
nN = nHCl = (m muối – mX)/36,5 = 0,1
Bảo toàn N → nN2 = 0,05
Chọn B
Câu 26:
Cho các phát biểu sau:
(a) Ở điều kiện thường, chất béo (C17H33COO)3C3H5 ở trạng thái lỏng.
(b) Fructozơ là monosaccarit duy nhất có trong mật ong.
(c) Dầu mỡ dùng để bôi trơn xe máy có thành phần chính là chất béo.
(d) Thành phần chính của giấy là xenlulozơ.
(e) Amilozơ và amilopectin đều có cấu trúc mạch phân nhánh.
(f) Dầu chuối (chất tạo hương liệu mùi chuối chín) có chứa isoamyl axetat.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Đúng, (C17H33COO)3C3H5 là chất béo không no nên ở trạng thái lỏng.
(b) Sai, mật ong chứa nhiều fructozo và glucozo
(c) Sai, dầu mỡ bôi trơn có thành phần hidrocacbon
(d) Đúng
(e) Sai, amilozo không nhánh
(f) Đúng
Chọn D
Câu 27:
Nhiệt phân hoàn toàn 17,4 gam hỗn hợp gồm M2CO3 và CaCO3. Đến khi phản ứng kết thúc thu được 8,6 gam chất rắn X và V lít khí CO2 (đktc). Giá trị của V và kim loại M tương ứng là
 Xem đáp án
Xem đáp án
nCO2 = (17,4 – 8,6)/44 = 0,2 → V = 4,48 lít
Nếu chỉ có CaCO3 bị phân hủy thì mCaCO3 = 0,2.100 > 17,4: Vô lí
Vậy cả M2CO3 và CaCO3 bị phân hủy.
→ n hỗn hợp = 0,2 → M hỗn hợp = 17,4/0,2 = 86
→ 2M + 60 < 86 → M < 13 → M = 7: M là Li
Chọn C
Câu 28:
Cho 4,2 gam hỗn hợp chứa Mg và Cu với tỷ lệ mol tương ứng là 1 : 4 vào dung dịch chứa 0,12 mol Fe(NO3)3. Sau khi phản ứng hoàn toàn thu được m gam kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
nMg = 0,015; nCu = 0,06
Dung dịch muối sau phản ứng chứa Mg2+ (0,015), NO3- (0,12.3 = 0,36), Fe2+ (0,12), bảo toàn điện tích → nCu2+ = 0,045
→ nCu dư = 0,06 – 0,045 = 0,015 → m = 0,96 gam
Chọn A
Câu 29:
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí H2 ở nhiệt độ cao. Mặt khác, kim loại M khử được ion H+ trong dung dịch axit loãng thành H2. Kim loại M là
 Xem đáp án
Xem đáp án
Kim loại M có thể được điều chế bằng cách khử ion của nó trong oxit bởi khí H2 ở nhiệt độ cao → M đứng sau Al
Kim loại M khử được ion H+ trong dung dịch axit loãng thành H2 → M đứng trước H
→ Chọn M là Fe.
Chọn B
Câu 30:
Cho Na vào dung dịch chứa Al2(SO4)3 và CuSO4 thu được khí A, dung dịch B và kết tủa C. Nung kết tủa C thu được chất rắn D. Cho khí A dư tác dụng với rắn D thu được rắn E. Chất rắn E tan một phần trong dung dịch HCl dư thu được rắn F. Vậy E chứa
 Xem đáp án
Xem đáp án
E tan một phần trong HCl nên E gồm Al2O3 và Cu.
A là H2; C gồm Al(OH)3 và Cu(OH)2; D gồm Al2O3 và CuO
Chọn D
Câu 31:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch Ba(HCO3)2 vào dung dịch KHSO4.
(b) Cho K vào dung dịch CuSO4 dư.
(c) Cho dung dịch NH4NO3 vào dung dịch Ba(OH)2.
(d) Cho dung dịch HCl tới dư vào dung dịch C6H5ONa.
(e) Cho khí CO2 tới dư vào dung dịch gồm NaOH và Ca(OH)2.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được cả chất rắn và khí là
 Xem đáp án
Xem đáp án
(a) Ba(HCO3)2 + KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
(b) K + H2O → KOH + H2
KOH + CuSO4 → K2SO4 + Cu(OH)2
(c) NH4NO3 + Ba(OH)2 → Ba(NO3)2 + NH3 + H2O
(d) HCl + C6H5ONa → C6H5OH + NaCl
(e) CO2 dư + Ca(OH)2 → Ca(HCO3)2
CO2 dư + NaOH → NaHCO3
Chọn A
Câu 32:
Cho sơ đồ chuyển hóa:
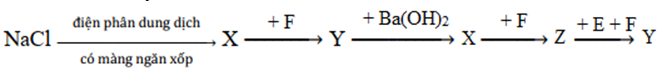
Biết: X, Y, Z, E, F là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học. Các chất Y, Z thỏa mãn sơ đồ trên lần lượt là?
 Xem đáp án
Xem đáp án
X: NaOH
F: CO2
Y: NaHCO3
Z: Na2CO3
(a) Ba(HCO3)2 + KHSO4 → BaSO4 + K2SO4 + CO2 + H2O
(b) K + H2O → KOH + H2
KOH + CuSO4 → K2SO4 + Cu(OH)2
(c) NH4NO3 + Ba(OH)2 → Ba(NO3)2 + NH3 + H2O
(d) HCl + C6H5ONa → C6H5OH + NaCl
(e) CO2 dư + Ca(OH)2 → Ca(HCO3)2
CO2 dư + NaOH → NaHCO3
Chọn B
Câu 33:
Cho 2,72 gam CH3COOC6H5 (chứa vòng benzen) vào 500 ml dung dịch NaOH 0,1M. Cô cạn dung dịch sau phản ứng thu được số gam chất rắn là
 Xem đáp án
Xem đáp án
CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O
nCH3COOC6H5 = 0,02; nNaOH = 0,05 → nH2O = 0,02
Bảo toàn khối lượng → m rắn = mCH3COOC6H5 + mNaOH – mH2O = 4,36 gam
CHọn A
Câu 34:
Xăng sinh học E5 chứa 5% etanol về thể tích (D = 0,8 g/ml), còn lại là xăng truyền thống, giả thiết xăng truyền thống chỉ chứa hai ankan là C8H18 và C9H20 có tỉ lệ mol tương ứng là 4 : 3; (D = 0,7 g/ml). Khi được đốt cháy hoàn toàn, 1 mol etanol tỏa ra lượng nhiệt là 1365 kJ, 1 mol C8H18 tỏa ra lượng nhiệt là 5072 kJ và 1 mol C9H20 tỏa ra nhiệt lượng là 6119 kJ. Trung bình, một chiếc xe máy tay ga di chuyển được 1 km thì cần một nhiệt lượng chuyển thành công cơ học có độ lớn là 212 kJ. Nếu xe máy tay ga đó đã sử dụng hết 6,5 lít xăng E5 ở trên thì quãng đường xe di chuyển được là y km (biết hiệu suất sử dụng nhiên liệu của động cơ là 40%). Vậy y gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
nC2H5OH = 6500.5%.0,8/46 = 5,6522 mol
nC8H18 = 4x; nC9H20 = 3x
→ 6500.95%.0,7 = 114.4x + 128.3x → x = 5,1458
Xe chạy được y km thì hết 6,5 lít xăng, bảo toàn năng lượng:
(5,6522.1365 + 5072.4x + 6119.3x).40% = 212y
→ y ≈ 390 km
Chọn A
Câu 35:
Trong bình kín không có không khí chứa 18,40 gam hỗn hợp rắn X gồm FeCO3, Fe(NO3)2, FeS và Fe (trong đó oxi chiếm 15,65% về khối lượng). Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp rắn Y và 0,08 mol hỗn hợp khí Z gồm ba khí có tỉ khối hơi so với He bằng a. Hòa tan hết rắn Y trong 91,00 gam dung dịch H2SO4 84%, kết thúc phản ứng thu được dung dịch T và 0,40 mol khí SO2 (không có sản phẩm khử khác). Cho 740 ml dung dịch NaOH 1M vào dung dịch T, thu được 23,54 gam kết tủa duy nhất. Giá trị gần nhất của a là
 Xem đáp án
Xem đáp án
Trong A có nO = 0,18 mol
Khí X (0,08 mol) gồm CO2, NO2, SO2
→ Trong B chứa O (0,18 – 0,08.2 = 0,02 mol), Fe (x mol) và S (y mol)
nNaOH = 0,74
nFe(OH)3 = 0,22 → nNaOH đã trung hòa axit dư = 0,74 – 0,22.3 = 0,08 → nH2SO4 = 0,04
nH2SO4 bđ = 0,78 → nH2SO4 pư = 0,74
Bảo toàn S: y + 0,74 = 3x/2 + 0,4
Bảo toàn electron: 3x + 6y = 0,02.2 + 0,4.2
→ x = 0,24 và y = 0,02
Bảo toàn khối lượng: mX = mA – mB = 4
→ MX = 4/0,08 = 50
→ dX/He = 12,5
Chọn C
Câu 36:
X và Y là hai axit cacboxylic hai chức, mạch hở kế tiếp nhau trong dãy đồng đẳng; Z và T là hai este thuần chức (chỉ chứa chức este) hơn kém nhau 14 đvC, đồng thời Y và Z là đồng phân của nhau (MX < MY < MT). Đốt cháy hoàn toàn 8,64 gam hỗn hợp E chứa X, Y, Z, T cần dùng 5,376 lít oxi (đktc). Mặt khác, 8,64 gam hỗn hợp E tác dụng vừa đủ với 100 ml dung dịch NaOH 1,5M, thu được 2,1 gam hỗn hợp ba ancol có cùng số mol. Số mol của Y trong E là?
 Xem đáp án
Xem đáp án
nNaOH = 0,15 → nE = 0,075
nCO2 = u và nH2O = v → 44u + 18v = 8,64 + 0,24.32
Bảo toàn O → 2u + v = 0,075.4 + 0,24.2
→ u = 0,285; v = 0,21
Số C = nCO2/nE = 3,8 → X là CH2(COOH)2 (x mol); Y là C2H4(COOH)2 (y mol); Z là C4H6O4 và T là C5H8O4
Sản phẩm chứa 3 ancol có cùng số mol nên cấu tạo của Z là (HCOO)2C2H4 (z mol) và của T là CH3OOC-COOC2H5 (z mol)
mAncol = 62z + 32z + 46z = 2,1 → z = 0,015
nE = x + y + 2z = 0,075
nCO2 = 3x + 4y + 4z + 5z = 0,285
→ x = 0,03; y = 0,015
Chọn B
Câu 37:
Điện phân dung dịch chứa x mol NaCl và y mol CuSO4 với điện cực trơ, màng ngăn xốp đến khi nước bị điện phân ở 2 điện cực thì dừng lại. Thể tích khí ở anot sinh ra gấp 1,5 lần thể tích khí ở catot ở cùng điều kiện nhiệt độ và áp suất. Quan hệ giữa x và y là?
 Xem đáp án
Xem đáp án
CuSO4 + 2NaCl → Cu + Cl2 + Na2SO4 (1)
CuSO4 + H2O → Cu + 0,5O2 + H2SO4 (2)
2NaCl + H2O → H2 + Cl2 + 2NaOH (3)
Khi H2O bị điện phân ở cả 2 điện cực thì đã có khí ở cả 2 điện cực nên phải xảy ra phản ứng (1) và (3)
nNaCl = x → nCl2 = x/2 → nH2 = x/3
nCuSO4 = y → nCu = y
Bảo toàn electron: 2x/2 = 2x/3 + 2y
→ x = 6y
Chọn C
Câu 38:
Cho E (C3H6O3) và F (C4H6O5) là các chất hữu cơ mạch hở. Trong phân tử chất F chứa đồng thời các nhóm -OH, -COO- và -COOH. Cho các chuyển hóa sau:
(1) E + NaOH → X + Y
(2) F + NaOH → X + H2O
(3) X + HCl → Z + NaCl
Biết X, Y, Z là các hợp chất hữu cơ. Cho các phát biểu sau:
(a) Đốt cháy hoàn toàn 1,25 mol X cần 42 lít (đktc) O2 (hiệu suất phản ứng 100%).
(b) Phân tử chất E chứa đồng thời nhóm -OH và nhóm -COO-.
(c) Y là chất gây nghiện, có trong thành phần của rượu, bia.
(d) Nhiệt độ sôi của chất Y nhỏ hơn nhiệt độ sôi của anđehit fomic.
(e) Dung dịch Z hòa tan Cu(OH)2 tạo thành dung dịch phức chất màu xanh thẫm.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
F (C4H6O5) chứa đồng thời các nhóm -OH, -COO- và -COOH, mặt khác thủy phân F chỉ tạo 1 muối hữu cơ nên F có cấu tạo:
HO-CH2-COO-CH2-COOH
→ X là HO-CH2-COONa
→ E là HO-CH2-COOCH3 và Y là CH3OH
Z là HO-CH2-COOH
(a) Đúng, X là C2H3O3Na:
2C2H3O3Na + 3O2 → Na2CO3 + 3CO2 + 3H2O
nX = 1,25 → V = 1,25.1,5.22,4 = 42 lít
(b) Đúng.
(c) Sai, chất gây nghiện có trong rượu, bia là C2H5OH.
(d) Sai, Y có liên kết H liên phân tử nên nhiệt độ sôi của Y cao hơn HCHO.
(e) Sai, Z hòa tan Cu(OH)2 tạo muối (HOCH2COO)2Cu xanh nhạt.
Chọn D
Câu 39:
Khi phân tích một hỗn hợp E chứa đồng thời các triglixerit và axit béo tự do (không có tạp chất khác) xác định được cacbon và oxi lần lượt chiếm 76,74% và 11,31% theo khối lượng. Xà phòng hóa hoàn toàn m gam E bằng dung dịch NaOH (lấy dư 20% so với lượng phản ứng) đun nóng, sau phản ứng thu được dung dịch chứa 0,021 mol NaOH và (m + 1,17) gam hỗn hợp các muối C15H31COONa, C17H31COONa, C17H33COONa, C17H35COONa. Mặt khác, m gam E phản ứng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
 Xem đáp án
Xem đáp án
nNaOH dư = 0,021 → nNaOH phản ứng = 0,105
n chất béo = u và n axit béo = v → 3u + v = 0,105
Bảo toàn khối lượng:
m + 0,105.40 = m + 1,17 + 92u + 18v
→ u = 0,03; v = 0,015
nO(E) = 2nNaOH phản ứng = 0,21
→ m = 0,21.16/11,31% = 29,71
nCO2 = nC = 76,74%.29,71/12 = 1,9
→ nH2O = nH/2 = (mE – mC – mO)/2 = 1,775
n chất béo = u = [nCO2 – (nH2O + nBr2)]/2
→ nBr2 = 0,065
Chọn C
Câu 40:
Thủy phân 68,4 gam saccarozơ trong môi trường axit với hiệu suất 90%, sau phản ứng thu được hỗn hợp X. Cho toàn bộ X tác dụng với lượng dư dung dịch AgNO3 trong NH3, đun nóng, phản ứng hoàn toàn thu được m gam Ag. Giá trị của m là
 Xem đáp án
Xem đáp án
Saccarozơ → 2C6H12O6 → 4Ag
nSaccarozơ = 0,2 → nAg thực tế = 0,2.4.90% = 0,72
→ mAg = 77,76 gam
Chọn D
