Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (30 đề)
Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (Đề 1)
-
6187 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại có độ cứng lớn nhất và là một trong những nguyên liệu chính để sản xuất thép không gỉ là:
 Xem đáp án
Xem đáp án
Chọn đáp án A. Cr
Câu 3:
Khí gas dân dụng và công nghiệp chủ yếu gồm C3H8 và C4H10. Tên gọi của 2 khí này lần lượt là:
 Xem đáp án
Xem đáp án
Câu 4:
 Xem đáp án
Xem đáp án
Câu 6:
 Xem đáp án
Xem đáp án
Câu 10:
Cho Metylaxetat vào dung dịch NaOH (đun nóng), sinh ra các sản phẩm là:
 Xem đáp án
Xem đáp án
Câu 15:
Khí cười (bóng cười) là nhóm chất gây nghiện, thuộc nhóm gây ảo giác có xu hướng tăng liều. Khí cười có tên là hóa học là đinitơ oxit và có công thức phân tử là:
 Xem đáp án
Xem đáp án
Câu 16:
Loại nhựa ký hiệu số 5 là an toàn để đựng thực phẩm và đặc biệt là sử dụng được cho lò vi sóng. Loại này còn kí hiệu là PP (Polipropilen), vậy nhựa số 5 được điều chế từ monome nào sau đây?
 Xem đáp án
Xem đáp án
Câu 17:
 Xem đáp án
Xem đáp án
Câu 18:
Cho các chất sau: Tripanmitin, saccarozơ, peptit, nilon-6. Số chất bị thủy phân trong dung dịch kiềm là:
 Xem đáp án
Xem đáp án
Câu 19:
Tinh bột được tạo thành trong cây xanh nhờ quá trình quang hợp sau: X (ánh sáng,clorophin) → Y (glucozơ) → Z (tinh bột). Hỏi nhận định nào sau đây đúng?
 Xem đáp án
Xem đáp án
Câu 20:
Hoa cẩm tú cầu là loài cây đặc biệt, có thể sống trên đất chua, trung tính hoặc có tính kiềm. Không những thế, màu sắc của hoa có thể thay đổi tuỳ theo độ pH trong đất. Ở đất chua cây sẽ cho hoa màu lam, đất trung tính hoa có màu trắng sữa, đất có độ kiềm hoa có màu tím, hồng. Hỏi nếu ta bón vôi (Ca(OH)2) thì hoa sẽ có màu gì?
 Xem đáp án
Xem đáp án
Câu 21:
Nọc kiến có chứa axit fomic, khi bị kiến đốt ta thường bôi vôi để giảm đau, vậy khi đó xảy ra phản ứng gì?
 Xem đáp án
Xem đáp án
Câu 22:
Cho các polime sau: PVC, Nilon-6,6, cao su Buna, PE. Số polime có thể được điều chế bằng phương pháp trùng hợp là:
 Xem đáp án
Xem đáp án
Các polime có thể được điều chế bằng phương pháp trùng hợp là: PVC, cao su Buna, PE (trùng hợp các chất tương ứng là và )
Câu 23:
Hiđro hóa hoàn toàn 0,5 mol triolein cần bao nhiêu mol H2 (điều kiện xảy ra phản ứng có đủ)?
 Xem đáp án
Xem đáp án
Chọn B.
0,5…………………….1,5
Câu 24:
Nhúng thanh sắt vào dung dịch hỗn hợp chứa 0,2 mol HCl và 0,2 mol CuCl2 đến khi phản ứng xảy ra hoàn toàn, lấy thanh sắt ra, làm khô, sấy nhẹ. Cho biết khối lượng thanh sắt tăng hay giảm bao nhiêu gam so với ban đầu?
 Xem đáp án
Xem đáp án
Chọn B.
Bảo toàn
phản ứng
phản ứng =
Giảm 4 gam.
Câu 26:
Cho 4,6 gam Na vào nước dư thì thể tích khí H2 thu được ở đktc là:
 Xem đáp án
Xem đáp án
Câu 27:
Dãy gồm các ion cùng tồn tại trong một dung dịch là:
 Xem đáp án
Xem đáp án
Câu 28:
Dãy các ion xếp theo chiều giảm dần tính oxi hóa là:
 Xem đáp án
Xem đáp án
Câu 29:
Đốt cháy hoàn toàn hỗn hợp chứa axit axetic, vinyl fomat, glucozơ và saccarozơ cần vừa đủ 4,48 lít khí O2 (đktc). Hấp thụ toàn bộ sản phẩm cháy bằng dung dịch Ca(OH)2 dư, thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
Quy đổi các chất thành C và
Câu 30:
Nung 8,96 lít (đktc) hỗn hợp X gồm propen, propin và hiđro (tỉ lệ mol 1:1:2) trong bình đựng bột Ni một thời gian thì thu được hỗn hợp khí Y có tỉ khối hơi so với X là 1,6. Dẫn toàn bộ Y qua bình đựng dung dịch AgNO3 trong NH3 dư thì thu được 7,35 gam kết tủa và hỗn hợp khí Z. Hấp thụ hết Z vào bình đựng dung dịch brom dư thì thấy có m gam brom phản ứng. Giá trị của m là:
 Xem đáp án
Xem đáp án
Chọn B.
gồm và
phản ứng
dư
Bảo toàn liên kết pi:
phản ứng dư
gam.
Câu 31:
Cho các phát biểu sau:
(1) Tất cả các nguyên tố nhóm B đều là kim loại.
(2) Trong cùng một chu kì kim loại có bán kính nguyên tử lớn hơn so với nguyên tử phi kim.
(3) Tính dẫn điện của Ag > Cu > Al > Au > Fe.
(4) Tôn là sắt trang thiếc.
(5) Cho Fe vào dung dịch CuCl2 sẽ xảy ra ăn mòn điện hóa.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn A.
(1) Đúng
(2) Đúng
(3) Sai,
(4) Sai, tôn là Fe tráng Zn
(5) Đúng
Câu 32:
Thực hiện các thí nghiệm sau:
(1) Cho hỗn hợp BaO và Al2O3 (tỉ lệ mol tương ứng 1: 1) vào nước (dư).
(2) Cho hỗn hợp Cu và Fe3O4 (tỉ lệ mol tương ứng 2 : 1) vào dung dịch HCl (dư).
(3) Cho hỗn hợp Ba và NaHCO3 (tỉ lệ mol tương ứng 1: 1) vào nước (dư).
(4) Cho hỗn hợp Cu và NaNO3 (tỉ lệ mol tương ứng 1: 2) vào dung dịch HCl (dư).
(5) Cho hỗn hợp MgCO3 và KHSO4 (tỉ lệ mol tương ứng 1: 2) vào nước (dư).
Khi phản ứng trong các thí nghiệm trên kết thúc, có bao nhiêu thí nghiệm không thu được chất rắn?
 Xem đáp án
Xem đáp án
Chọn B.
(1)
(2) (Cu còn dư)
(3)
(4)
(5)Câu 33:
Tiến hành 2 thí nghiệm sau:
- Thí nghiệm 1: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch H2SO4 loãng.
- Thí nghiệm 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau nhưng được nối với nhau bằng dây dẫn điện) vào cốc đựng dung dịch H2SO4 loãng.
Có các nhận xét sau:
(1) Ở cả 2 thí nghiệm thanh Zn đều bị ăn mòn điện hóa.
(2) Thanh Zn ở cả 2 thí nghiệm đều bị ăn mòn với tốc độ như nhau.
(3) Ở thí nghiệm 1 bọt khí H2 thoát ra ở thanh Zn còn ở thí nghiệm 2 bọt khí H2 thoát ra ở cả thanh Zn và thanh Cu.
(4) Ở thí nghiệm 2 thanh Zn sẽ đóng vai trò cực (-) gọi là anot, thanh Cu sẽ đóng vai trò cực (+) gọi là catot.
(5) Ở thí nghiệm 2 cả thanh Zn và thanh Cu đều bị ăn mòn.
Số nhận xét đúng:
 Xem đáp án
Xem đáp án
Chọn A.
TN1: Thanh Zn và Cu không tiếp xúc điện với nhau nên không có ăn mòn điện hóa.
Thanh Zn bị ăn mòn hóa học, thanh Cu không bị ăn mòn.
TN2: Có ăn mòn điện hóa, thanh Zn là cực âm (anot) bị oxi hóa,
thanh Cu là cực dương (catot) xảy ra quá trình khử .
(1) Sai
(2) Sai, thanh Zn ở TN1 ăn mòn chậm hơn thanh Zn ở TN2.
(3) Đúng
(4) Đúng
(5) Sai, chỉ thanh Zn bị ăn mòn.
Câu 34:
Cho các phát biểu sau:
(1) Anbumin của lòng trắng trứng, fibroin của tơ tằm là những protein phức tạp.
(2) Trong mật ong có nhiều glucozơ (khoảng 30%).
(3) Tinh bột và xenlulozơ thủy phân hoàn toàn đều thu được 1 loại monosaccarit.
(4) Xenlulozơ có nhiều trong bông, đay, tre... khi cho tác dụng với hỗn hợp HNO3/H2SO4 đặc, đun nóng sẽ tạo chất hữu cơ dễ cháy, nổ mạnh được dùng làm thuốc súng không khói.
(5) Muối mononatri của axit glutamic dùng làm gia vị thức ăn (gọi là mì chính hay bột ngọt).
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn A.
(1) Sai, chúng đều là protein đơn giản.
(2) Đúng
(3) Đúng, tạo glucozơ.
(4) Đúng
(5) Đúng
Câu 35:
Từ 1 kg nho chứa 18% glucozơ về khối lượng lên men rượu thì có thể thu được bao nhiêu lít rượu vang 10°, biết khối lượng riêng của rượu nguyên chất là 0,8 gam/ml và hiệu suất chuyển hóa là 75%?
 Xem đáp án
Xem đáp án
Chọn D.
V rượu = 0,8625 lít
Câu 36:
Hỗn hợp X gồm Na, Ba, Na2O và BaO. Hòa tan hoàn toàn 20,7 gam X vào nước, thu được 1,12 lít khí H2 (đktc) và dung dịch Y, trong đó có 17,1 gam Ba(OH)2. Hấp thụ hoàn toàn V lít khí CO2 (đktc) vào Y, thu được m gam kết tủa. Quan hệ giữa V và m theo bảng sau:
|
V (lít) |
V1 |
4V1 |
4,5V1 |
|
m (gam) |
x |
x |
y |
Tính y?
 Xem đáp án
Xem đáp án
Chọn A.
Quy đổi X thành Na (a), Ba (0,1) và O (b)
Bảo toàn electron:
Đặt
Lượng tăng từ u lên 4u nhưng kết tủa
không đổi nên lúc dùng u thì kết tủa chưa
bị hòa tan, lúc dùng 4u thì kết tủa đã bị hòa tan.
Khi dùng u mol
và
Bảo toàn
Khi CO2 tăng thì
thì có thêm 0,04 mol đã bị hòa tan
Còn lại mol
Câu 37:
Hòa tan hoàn toàn 13,5 gam hỗn hợp bột gồm Mg, Al, MgO, Mg(OH)2, MgCO3, Al(NO3)3 bằng một lượng vừa đủ 0,97 mol HNO3. Sau khi phản ứng kết thúc thu được dung dịch X và 0,672 lít hỗn hợp khí gồm N2O và CO2. Lấy dung dịch X cho phản ứng với dung dịch NaOH thì lượng NaOH phản ứng tối đa là 1,05 mol vad sau phản ứng thu được 11,6 gam kết tủa màu trắng, dung dịch chứa 88,8 gam muối. Phần trăm khối lượng của Mg(OH)2 trong hỗn hợp đầu gần nhất với:
 Xem đáp án
Xem đáp án
Chọn A.
Dung dịch sau phản ứng với NaOH chứa NaNO3 (a) và NaAlO2 (b)
Và m muối
Dung dịch X chứa
bảo toàn điện tích
m khí
Bảo toàn khối lượng
Bảo toàn
Câu 38:
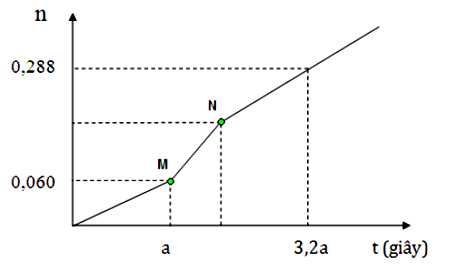
Hòa tan hoàn toàn m gam hỗn hợp CuSO4 và NaCl vào nước, thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được trên cả 2 điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị bên (đồ thị gấp khúc tại các điểm M, N).
Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của H2O. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A.
Đoạn 1:
Trong a giây mỗi điện cực đã trao đổi mol electron.
Đoạn 2: Có độ dốc lớn hơn đoạn 1
nên tốc độ thoát khí nhanh hơn Thoát và
Bảo toàn electron
Đoạn 3: Thoát H2 và O2. Đặt
n khí tổng
anot
và
đoạn 1 = 0,06
tổng = 0,24
gam.
Câu 39:
Hỗn hợp X chứa hai peptit A, B đều mạch hở, tổng số liên kết peptit là 6. Khi thủy phân hoàn toàn hỗn hợp X thu được hỗn hợp gồm glyxin, alanin và valin. Đốt ch|y 19,16 gam X cần dùng 0,78 mol O2, sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua dung dịch KOH đặc, dư thấy khối lượng dung dịch tăng 40,2 gam. Phần trăm khối lượng của peptit có khối lượng phân tử lớn gần nhất với:
 Xem đáp án
Xem đáp án
Chọn C.
Quy đổi X thành
Số N trung bình là đipeptit.
Tổng 6 liên kết peptit nên B là hexapeptit.
(Bấm hệ và )
A dạng và B dạng
Sản phầm thủy phân có Val nên
ít nhất 1 trong 2 giá trị và là nghiệm duy nhất.
Vậy X gồm và
Câu 40:
Cho hỗn hợp X gồm hai este thuần chức, mạch hở, không phân nhánh A, B (MA < MB) và số mol của A gấp 2 lần số mol của B. Khi đốt cháy hoàn toàn A hoặc B thì tỉ lệ số mol O2 đã phản ứng và số mol CO2 thu được đều bằng 1 : 1. Lấy 26,64 gam hỗn hợp X thủy phân hoàn toàn bằng 360ml dung dịch KOH 1M vừa đủ, sau phản ứng thu được hỗn hợp Y chứa 2 ancol và hỗn hợp D chứa 2 muối. Dẫn toàn bộ Y qua bình đựng Na dư thấy khối lượng bình tăng 13,68 gam. Đốt cháy hoàn toàn hỗn hợp D cần dùng 0,33 mol O2. Phần trăm về khối lượng của B trong hỗn hợp gần nhất với:
 Xem đáp án
Xem đáp án
Chọn C
nên A, B đều có số H gấp đôi số O.
đốt đốt
đốt và
Bảo toàn
Bảo toàn (muối)
Các muối đều không có H
n muối
Muối của A là và muối của B là
Các muối đa chức nên ancol đơn chức
Dễ thấy nên Y gồm các ancol no, mạch hở.
(muối)
Với x, y chẵn nên có 2 trường hợp.
TH1: và Muối gồm và
X gồm A là và B là
Các este đều có 8H nên loại vì , trái với giả thiết.
TH2: và Muối gồm và
X gồm ![]() là và B là
là và B là
Các este đều có 8H nên thỏa mãn
