(2023) Đề thi thử Hóa học THPT Nguyễn Trung Trực, Hồ Chí Minh có đáp án
(2023) Đề thi thử Hóa học THPT Nguyễn Trung Trực, Hồ Chí Minh có đáp án
-
194 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 2:
Lên men m gam glucozơ để tạo thành ancol etylic (hiệu suất phản ứng bằng 90%). Hấp thụ hoàn toàn lượng khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 15 gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
nCO2 = nCaCO3 = 0,15
→ nC6H12O6 phản ứng = 0,075
→ mC6H12O6 đã dùng = 0,075.180/90% = 15 gam
Chọn A
Câu 3:
Cho 12,1 gam hỗn hợp kim loại gồm Fe và Zn tan hết trong dung dịch HCl (vừa đủ) thấy thoát ra 4,48 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được chất rắn có khối lượng là
 Xem đáp án
Xem đáp án
nH2 = 0,2 → nCl- = 0,4
m muối = m kim loại + mCl- = 26,3 gam
Chọn B
Câu 6:
Trong các trường hợp sau, trường hợp nào xảy ra ăn mòn điện hóa học?
 Xem đáp án
Xem đáp án
D có ăn mòn điện hóa học do có cặp điện cực Fe-C tiếp xúc với nhau và cùng tiếp xúc với môi trường điện li (không khí ẩm).
Chọn D
Câu 8:
Xà phòng hóa hoàn toàn triolein bằng dung dịch NaOH vừa đủ, ta thu được sản phẩm là
 Xem đáp án
Xem đáp án
Chọn D
Câu 12:
Dãy kim loại nào dưới đây điều chế được bằng cách điện phân nóng chảy muối clorua?
 Xem đáp án
Xem đáp án
Chọn B
Câu 13:
Cho 15 gam hỗn hợp 3 amin đơn chức, bậc 1 tác dụng vừa đủ với V lít dung dịch HCl 1,2M thì thu được 18,504 gam muối. Giá trị của V là
 Xem đáp án
Xem đáp án
nHCl = (18,504 – 15)/36,5 = 0,096
→ V = 0,08 lít
Chọn C
Câu 15:
Etyl fomat là một este có mùi thơm, không độc, được dùng làm chất tạo hương trong công nghiệp thực phẩm. Công thức của etyl fomat là
 Xem đáp án
Xem đáp án
Chọn D
Câu 17:
Một số cơ sở sản xuất thuốc bắc thường đốt một chất bột rắn màu vàng (là một đơn chất) để tạo ra khí X nhằm mục đích tẩy trắng, chống mốc. Tuy nhiên, theo các nhà khoa học thì khí X có ảnh hưởng không tốt đến cơ quan nội tạng và khí X cũng cũng là một trong những nguyên nhân gây ra mưa axit. Khí X là
 Xem đáp án
Xem đáp án
Chọn C
Câu 23:
Cho từ từ dung dịch NaOH vào dung dịch X, thu được kết tủa keo trắng tan trong dung dịch NaOH dư. Chất X là
 Xem đáp án
Xem đáp án
Chất X là AlCl3:
AlCl3 + 3NaOH → 3NaCl + Al(OH)3 (↓ keo trắng)
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Chọn D
Câu 24:
Cho dãy các chất sau: (1) glucozơ, (2) metyl fomat, (3) vinyl axetat, (4) axetanđehit. Số chất trong dãy có phản ứng tráng bạc với dung dịch AgNO3/NH3 là
 Xem đáp án
Xem đáp án
Có 3 chất trong dãy có phản ứng tráng bạc với dung dịch AgNO3/NH3 là (1)(2)(4)
Chọn A
Câu 25:
Este X có công thức phân tử C6H10O4. Xà phòng hóa hoàn toàn X bằng dung dịch NaOH, thu được ba chất hữu cơ Y, Z, T. Biết Y tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam. Nung nóng Z với hỗn hợp rắn gồm NaOH và CaO, thu được CH4. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Y + Cu(OH)2 → Dung dịch xanh lam nên Y là ancol 2 chức có OH kề nhau.
→ Z, T là các muối đơn chức.
Z + NaOH/CaO → CH4 nên Z là CH3COONa
X là CH3COO-CH2-CH(CH3)-OOC-H hoặc HCOO-CH2-CH(CH3)-OOC-CH3.
Y là CH2OH-CH(CH3)OH
T là HCOONa
B. Sai, Y mạch thẳng.
Chọn B
Câu 26:
Cho các thí nghiệm sau:
(a) Cho CaCO3 vào dung dịch CH3COOH dư.
(b) Cho Ag vào dung dịch HCl dư.
(c) Cho Na vào dung dịch CuSO4 dư.
(e) Cho Ba(HCO3)2 vào dung dịch NaHSO4 dư.
Số thí nghiệm có sự hòa tan chất rắn chỉ tạo ra dung dịch trong suốt là
 Xem đáp án
Xem đáp án
(a) CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O
(b) Không phản ứng
(c) Na + CuSO4 + H2O → Na2SO4 + Cu(OH)2 + H2
(d) Ba(HCO3)2 + NaHSO4 → BaSO4 + Na2SO4 + CO2 + H2O
Chọn D
Câu 27:
Hỗn hợp X gồm FeS2 và MS có số mol bằng nhau (M là kim loại có hóa trị không đổi). Cho 6,51 gam X tác dụng hoàn toàn với dung dịch HNO3 đun nóng thu được dung dịch Y và 13,216 lít hỗn khí (đktc) có khối lượng 26,34 gam gồm NO, NO2. Thêm một lượng dung dịch BaCl2 vào dung dịch Y thấy xuất hiện kết tủa trắng. Kim loại M là
 Xem đáp án
Xem đáp án
Khí B gồm NO2 (0,54) và NO (0,05)
Đặt nFeS2 = nMS = a
Bảo toàn electron: 15nFeS2 + 8nMS = nNO2 + 3nNO
→ a = 0,03
→ mX = 120.0,03 + 0,03(M + 32) = 6,51
→ M = 65: Zn
Chọn A
Câu 28:
Cho hỗn hợp X gồm một tetrapeptit và một tripeptit. Để thủy phân hoàn toàn 50,36 gam X cần dung dịch chứa 0,76 mol NaOH, sau phản ứng hoàn toàn cô cạn thu được 76,8 gam hỗn hợp muối chỉ gồm a mol muối glyxin và b mol muối alanin. Mặt khác đốt cháy hoàn toàn 0,11 mol X bằng O2 dư thu được m gam CO2. Giá trị của m là
 Xem đáp án
Xem đáp án
Quy đổi X thành:
C2H3ON: 0,76 mol
CH2: x mol
H2O: y mol
mX = 0,76.57 + 14x + 18y = 50,36
m muối = 0,76.57 + 14x + 0,76.40 = 76,8
→ x = y = 0,22
Nếu đốt 0,22 mol X thu được nCO2 = 0,76.2 + x = 1,74
→ Đốt 0,11 mol X thu được nCO2 = 0,87
→ mCO2 = 38,28
Chọn C
Câu 29:
X, Y, Z là ba hiđrocacbon mạch hở (MX < MY < MZ < 62) có cùng số nguyên tử cacbon trong phân tử và đều phản ứng với dung dịch AgNO3 trong NH3 dư. Cho 11,7 gam hỗn hợp E gồm X, Y, Z (có cùng số mol) tác dụng tối đa với a mol Br2 trong dung dịch. Giá trị của a là:
 Xem đáp án
Xem đáp án
Các chất X, Y, Z thỏa mãn là:
X là CH≡C-C≡CH
Y là CH≡C-CH=CH2
Z là CH≡C-CH2-CH3
nX = nY = nZ = e
→ mE = 50e + 52e + 54e = 11,7
→ e = 0,075
nBr2 = 4nX + 3nY + 2nZ = 0,675
Chọn B
Câu 30:
Cho dãy các chất: CH4, C2H4, CH2=CH-COOH, C6H5NH2 (anilin), C6H6 (benzen). Số chất trong dãy phản ứng được với nước brom là
 Xem đáp án
Xem đáp án
Có 3 chất trong dãy phản ứng được với nước brom là: C2H4, CH2=CH-COOH, C6H5NH2
Chọn A
Câu 31:
Phát biểu đúng là:
 Xem đáp án
Xem đáp án
A. Sai, amino axit là các chất rắn kết tinh, không màu.
B. Sai, isoamyl axetat có mùi chuối chín.
C. Đúng, glucozơ có chức -OH và -COOH, glyxin có chức -NH2 và -COOH.
D. Sai, tơ visco, tơ axetat là tơ nhân rạo, tơ nilon-6,6, tơ enang là tơ tổng hợp.
Chọn C
Câu 32:
Hòa tan hết 11,02 gam hỗn hợp X gồm FeCO3, Fe(NO3)2 và Al vào dung dịch Y chứa KNO3 và 0,4 mol HCl, thu được dung dịch Z và 2,688 lít (đktc) khí T gồm CO2, H2 và NO (có tỉ lệ mol tương ứng là 5 : 2 : 5). Dung dịch Z phản ứng được tối đa với 0,45 mol NaOH. Nếu cho Z tác dụng với dung dịch AgNO3 dư thì thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn và NO là sản phẩm khử duy nhất của N+5 trong các phản ứng trên. Giá trị của m là
 Xem đáp án
Xem đáp án
T gồm CO2 (0,05), H2 (0,02) và NO (0,05)
Trong X chứa FeCO3 (0,05), Fe(NO3)2 (a), Al (b). Đặt nKNO3 = c
mX = 116.0,05 + 180a + 27b = 11,02 (1)
Bảo toàn N: 2a + c = 0,05 (2)
Z + NaOH thu được dung dịch chứa Na+ (0,45), K+ (c), Cl- (0,4) và AlO2- (b)
Bảo toàn điện tích → c + 0,45 = b + 0,4 (3)
(1)(2)(3) → a = 0,02; b = 0,06; c = 0,01
nH+ = 2nCO2 + 2nH2 + 4nNO tổng
→ nNO tổng = 0,065
Bảo toàn electron:
nFeCO3 + nFe(NO3)2 + 3nAl = 2nH2 + 3nNO tổng + nAg
→ nAg = 0,015
Bảo toàn Cl → nAgCl = 0,4
→ m↓ = 59,02 gam
Chọn A
Câu 33:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam mỡ lợn và 10 ml dung dịch NaOH 40%.
Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 30 phút và thỉnh thoảng thêm nước cất để giữ cho thể tích hỗn hợp không đổi rồi để nguội hỗn hợp.
Bước 3: Rót thêm vào hỗn hợp 15 – 20 ml dung dịch NaCl bão hòa nóng, khuấy nhẹ rồi để yên hỗn hợp.
Cho các phát biểu sau:
(a) Sau bước 3 thấy có lớp chất rắn màu trắng nổi lên là glixerol.
(b) Vai trò của dung dịch NaCl bão hòa ở bước 3 là để tách muối natri của axit béo ra khỏi hỗn hợp.
(c) Ở bước 2, nếu không thêm nước cất, hỗn hợp bị cạn khô thì phản ứng thủy phân không xảy ra.
(d) Ở bước 1, nếu thay mỡ lợn bằng dầu mỡ bôi trơn thì hiện tượng thí nghiệm sau bước 3 vẫn xảy ra tương tự.
(e) Trong công nghiệp, phản ứng ở thí nghiệm trên được ứng dụng để sản xuất xà phòng và glixerol.
Số phát biểu sai là
 Xem đáp án
Xem đáp án
(a) Sai, chất rắn màu trắng nổi lên là xà phòng.
(b) Đúng, muối của axit béo khó tan trong dung dịch chứa NaCl nên tách ra, nhẹ hơn và nổi lên.
(c) Đúng, phản ứng thủy phân cần có mặt H2O.
(d) Sai, dầu nhớt là hiđrocacbon, không thể tạo ra xà phòng.
(e) Đúng.
Chọn B
Câu 34:
Thực hiện phản ứng nhiệt nhôm m gam hỗn hợp X gồm Al và Fe3O4 đến khi phản ứng hoàn toàn thu được hỗn hợp Y (biết Fe3O4 chỉ bị khử về Fe). Chia Y thành hai phần:
- Phần 1 cho tác dụng với dung dịch NaOH dư thu được 0,15 mol H2, dung dịch Z và phần không tan T. Cho toàn bộ phần không tan T tác dụng với dung dịch HCl dư thu được 0,45 mol H2.
- Phần 2 cho tác dụng với dung dịch HCl thu được 1,2 mol H2.
Giá trị của m là:
 Xem đáp án
Xem đáp án
Phần 1:
Với NaOH: nH2 = 0,15 → nAl = 0,1
Với HCl: nH2 = 0,45 → nFe = 0,45
8Al + 3Fe3O4 → 4Al2O3 + 9Fe
0,4…….0,15….0,2….← 0,45
Vậy phần 1 chứa: Al (0,1), Fe (0,45), Al2O3 (0,2)
→ Phần 2 chứa Al (0,1k), Fe (0,45k), Al2O3 (0,2k)
→ 0,1k.3 + 0,45k.2 = 1,2.2
→ k = 2
Vậy Phần 2 gấp 2 lần phần 1
→ mX = mY = 3mPhần 1 = 144,9
Chọn B
Câu 35:
Cho 7,3 gam lysin và 15 gam glyxin vào dung dịch chứa 0,3 mol KOH, thu được dung dịch Y. Cho Y tác dụng hoàn toàn với dung dịch HCl dư, thu được m gam muối. Giá trị của m là:
 Xem đáp án
Xem đáp án
Muối gồm có:
Lys(HCl)2: 0,05 mol
GlyHCl: 0,2 mol
KCl: 0,3 mol
→ m muối = 55,6 gam
Chọn C
Câu 36:
Hỗn hợp M gồm 3 este đơn chức X, Y, Z (X và Y là đồng phân của nhau, mạch hở). Đốt cháy hoàn toàn 5,3 gam M thu được 6,272 lít CO2 (đktc) và 3,06 gam H2O. Mặt khác, khi cho 5,3 gam M tác dụng với dung dịch NaOH dư thì thấy khối lượng NaOH phản ứng hết 2,8 gam, thu được ancol T, chất tan hữu cơ no Q cho phản ứng tráng gương và m gam hỗn hợp 2 muối. Giá trị của m gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
nCO2 = 0,28; nH2O = 0,17
Bảo toàn khối lượng → nO2 = 0,315
Bảo toàn O → nM = 0,05
nNaOH = 0,07 > nM → Z là este của phenol
→ nX + nY = 0,03 và nZ = 0,02
X, Y có số C là n và Z có số C là m
→ nC = 0,03n + 0,02m = 0,28
→ 3n + 2m = 28
Xà phòng hóa tạo andehit Q nên n ≥ 3, mặt khác m ≥ 7 nên n = 4 và m = 8 là nghiệm duy nhất.
Sản phẩm có 1 ancol, 1 andehit, 2 muối nên các chất là:
X: HCOO-CH2-CH=CH2
Y: HCOO-CH=CH-CH3
Z: HCOO-C6H4-CH3
Muối gồm HCOONa (0,05) và CH3-C6H4-ONa (0,02)
→ m muối = 6
Chọn B
Câu 37:
Quá trình làm đậu phụ được tiến hành như sau:
+ Xay đậu tương cùng với nước lọc và lọc bỏ bã được “nước đậu”
+ Đun nước đậu “đến sôi” và chế thêm nước chua được “óc đậu”.
+ Cho “óc đậu” vào khuôn và ép, được đậu phụ.
Mục đích chính khi cho thêm nước chua vào “nước đậu”:
 Xem đáp án
Xem đáp án
Mục đích chính khi cho thêm nước chua vào “nước đậu” là làm protein trong nước đậu bị đông tụ.
Chọn D
Câu 38:
Cho 27,6 gam hỗn hợp gồm Na, Na2O, Ba và BaO vào lượng nước dư, thu được a mol khí H2 và dung dịch X. Sục khí CO2 đến dư vào X, phản ứng được biểu diễn theo đồ thị sau
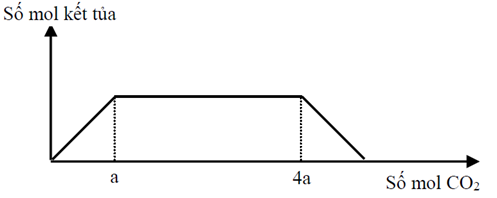
Giá trị của a là.
 Xem đáp án
Xem đáp án
Khi nCO2 = a thì kết tủa đạt max → nBa = nBaCO3 = a
Khi nCO2 = 4a thì kết tủa bắt đầu bị hòa tan → nBaCO3 + nNaHCO3 = 4a
→ nNaHCO3 = 3a → nNa = 3a
Đặt nO = b
→ 137a + 23.3a + 16b = 27,6
Bảo toàn electron → 2a + 3a = 2b + 2a
→ a = 0,12 và b = 0,18
Chọn D
Câu 40:
Cho các phát biểu sau:
(1) Oxi hóa glucozơ, thu được sobitol.
(2) Để chứng minh trong phân tử của glucozơ có nhiều nhóm hiđroxyl, người ta cho dung dịch glucozơ phản ứng tráng bạc.
(3) Saccarozơ và glucozơ đều có phản ứng với Cu(OH)2 ở nhiệt độ thường tạo thành dung dịch màu xanh lam.
(4) Các amin đều không độc được sử dụng để chế biến thực phẩm.
(5) Muối natri hoặc kali của axit béo được dùng để sản xuất xà phòng.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(1) Sai, khử glucozơ bằng H2 thu được sobitol.
(2) Sai, dùng phản ứng với Cu(OH)2 để chứng minh có nhiều -OH (hoặc phản ứng với (CH3CO)2O để chứng minh có cụ thể 5 nhóm -OH)
(3) Đúng
(4) Sai, các amin đều độc.
(5) Đúng
Chọn D
