Thi Online (2023) Đề thi thử Hóa THPT Phan Bội Châu, Nghệ An (Lần 1) có đáp án
Thi Online (2023) Đề thi thử Hóa THPT Phan Bội Châu, Nghệ An (Lần 1) có đáp án
-
525 lượt thi
-
40 câu hỏi
-
45 phút
Danh sách câu hỏi
Câu 1:
X là loại đường có nhiều trong quả nho chín. Số nguyên tử H trong phân tử X là?
 Xem đáp án
Xem đáp án
Chọn B
Câu 3:
Mùa lạnh, đưa lò than vào trong phòng kín dễ gây ngạt thở. Nguyên nhân gây ngạt thở nhanh là do khí nào sau đây?
 Xem đáp án
Xem đáp án
Chọn C
Câu 6:
Thạch cao nung thu được khi đun nóng thạch cao sống ở 160°C, dược dùng để nặn tượng, bó bột. Công thức của thạch cao nung là?
 Xem đáp án
Xem đáp án
Chọn A
Câu 11:
Natri cacbonat được dùng trong công nghiệp thủy tinh, bột giặt, phẩm nhuộm. Công thức của natri cacbonat là
 Xem đáp án
Xem đáp án
Chọn D
Câu 13:
Dữ kiện thực nghiệm nào sau đây chứng tỏ phân tử saccarozơ có nhiều nhóm -OH?
 Xem đáp án
Xem đáp án
Chọn D
Câu 14:
Trong sơ đồ thực nghiệm theo hình vẽ sau đây:
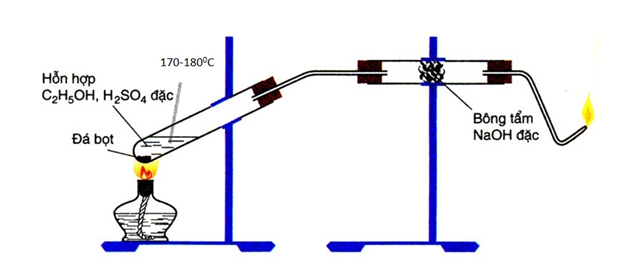
Chọn phát biểu đúng:
 Xem đáp án
Xem đáp án
Hình vẽ là sơ đồ điều chế và thử tính chất của C2H4.
A. Đúng
C2H4 + H2O + KMnO4 —> C2H4(OH)2 + KOH + MnO2
B. Sai. Phản ứng có sản phẩm phụ là SO2, nó được tạo ra do H2SO4 bị khử. Bông tẩm NaOH có tác dụng ngăn SO2 thoát ra cùng sản phẩm chính C2H4.
C. Sai, tại mức nhiệt độ trên 170°C thì phản ứng chính là: C2H5OH —> C2H4 + H2O
D. Sai. H2SO4 có vai trò xúc tác cho phản ứng.
Chọn A
Câu 15:
Cho 3 ion: Fe2+, Ag+, Cu2+. Tính oxi hóa của các ion kim loại này tăng theo thứ tự nào sau đây?
 Xem đáp án
Xem đáp án
Chọn A
Câu 16:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
A. Sai, thu được dung dịch chứa 3 muối CuCl2, FeCl2, FeCl3 dư.
Cu + 2FeCl3 —> 2FeCl2 + CuCl2
B. Đúng, có thể tan hết khi nCu ≤ nFe3O4:
Fe3O4 + 8HCl —> FeCl2 + 2FeCl3 + 4H2O
Cu + 2FeCl3 —> 2FeCl2 + CuCl2
C. Sai, nNO = nFe2+/3 < nNO3- ban đầu = 2nFe2+ nên NO3- còn dư, dung dịch thu được chứa FeCl3, Fe(NO3)3.
D. Sai, Cu khử được ion Fe3+ trong dung dịch.
Chọn B
Câu 17:
Cho Fe dư tác dụng với dung dịch HNO3, sau khi kết thúc phản ứng thu được dung dịch chứa chất nào sau đây?
 Xem đáp án
Xem đáp án
Fe dư + HNO3 —> Fe(NO3)2 + NO + H2O
Dung dịch thu được chứa Fe(NO3)2.
Chọn D
Câu 20:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
A. Sai, điều chế Fe bằng phương pháp nhiệt luyện.
B. Đúng: Mg2+ + 2e —> Mg
C. Sai, Na+ không bị khử trong dung dịch, lúc này H2O bị khử tạo H2.
D. Sai, khi điện phân Al2O3 nóng chảy người ta dùng anot và catot đều bằng than chì.
Chọn B
Câu 21:
Cách nào sau đây không sử dụng để loại bỏ tính cứng tạm thời của nước?
 Xem đáp án
Xem đáp án
Nước cứng tạm thời chứa Mg(HCO3)2, Ca(HCO3)2 (Gọi chung là M(HCO3)2):
A. M(HCO3)2 + Na2CO3 —> MCO3 + NaHCO3
B. M(HCO3)2 + NaOH —> MCO3 + Na2CO3 + H2O
C. Không làm mềm được vì vẫn còn Ca2+ (có trong Ca(OH)2 dư).
D. M(HCO3)2 —> MCO3 + CO2 + H2O
Chọn C
Câu 22:
Nhận định nào sau đây không đúng về amino axit?
 Xem đáp án
Xem đáp án
A. Đúng, amino axit có tính axit ở nhóm -COOH, tính bazơ ở nhóm -NH2.
B. Đúng.
C. Đúng, do sự tồn tại ion lưỡng cực nên amino axit tương đối dễ tan trong nước.
D. Sai, amino axit là chất tạp chức.
Chọn D
Câu 23:
Chất nào sau đây không phải là chất lưỡng tính?
 Xem đáp án
Xem đáp án
HCOOCH3 không phải chất lưỡng tính vì không có phản ứng trao đổi proton với axit, bazơ khác.
Chọn B
Câu 25:
Vai trò nào không phải là của cacbon trong sản xuất gang?
 Xem đáp án
Xem đáp án
Vai trò tạo xỉ không phải của C. Vai trò tạo xỉ là nhờ CaO (tạo ra do CaCO3 bị nhiệt phân):
CaO + SiO2 —> CaSiO3 (xỉ)
Chọn A
Câu 26:
Thí nghiệm nào sau đây không có kết tủa xuất hiện?
 Xem đáp án
Xem đáp án
A. Ca(OH)2 + Ba(HCO3)2 —> CaCO3 + BaCO3 + H2O
B. BaCl2 + NaHSO4 —> BaSO4 + NaCl + HCl
C. KOH + Ca(HCO3)2 —> CaCO3 + K2CO3 + H2O
D. Mg(HCO3)2 + H2SO4 —> MgSO4 + CO2 + H2O
Chọn D
Câu 27:
Hỗn hợp E gồm ba este X, Y, Z đều đa chức, no, mạch hở (MX < MY < MZ). Đốt cháy hoàn toàn 8,55 gam E cần vừa đủ 8,232 lít khí O2, thu được 5,13 gam H2O. Mặt khác, đun nóng 8,55 gam E với dung dịch NaOH (vừa đủ), cô cạn dung dịch sau phản ứng, thu được muối T (có mạch cacbon không phân nhánh) và hỗn hợp hai ancol (đơn chức, kế tiếp trong dãy đồng đẳng). Đốt cháy hoàn toàn T, thu được Na2CO3, CO2 và 1,08 gam H2O. Khối lượng của 0,12 mol Y là
 Xem đáp án
Xem đáp án
Muối T không nhánh nên tối đa 2 chức, mặt khác các ancol đều đơn chức nên T và E đều 2 chức.
nO2 = 0,3675; nH2O = 0,285
Bảo toàn khối lượng —> nCO2 = 0,345
—> nT = nE = nCO2 – nH2O = 0,06
Đốt T —> nH2O = 0,06
—> Số H của T = 2nH2O/nT = 2
—> T là CH2(COONa)2
nAncol = 2nE = 0,12 và nC(ancol) = nC(E) – nC(T) = 0,165
—> Số C = nCO2/nAncol = 1,375 —> CH3OH và C2H5OH
X là CH2(COOCH3)2
Y là CH2(COOCH3)(COOC2H5)
Z là CH2(COOC2H5)2
Khi nY = 0,12 thì mY = 17,52
Chọn C
Câu 28:
Cho các phát biểu sau:
(a) Glucozơ là monosaccarit duy nhất có trong quả nho chín.
(b) Ancol etylic có nhiệt độ sôi cao hơn axit axetic.
(c) Dung dịch valin làm quỳ tím hóa xanh.
(d) Quần áo dệt bằng tơ tằm không nên là ủi ở nhiệt độ cao.
(e) Mặt cắt quả chuối xanh tạo màu xanh tím với iot.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) Sai, nho chín chứa glucozơ, fructozơ.
(b) Sai, C2H5OH có nhiệt độ sôi thấp hơn CH3COOH do C2H5OH có phân tử khối nhỏ hơn, liên kết H liên phân tử kém bền hơn CH3COOH.
(c) Sai, Val có môi trường trung tính.
(d) Đúng, tơ tằm kém bền với nhiệt, nhiệt độ cao sẽ làm tơ tằm bị nhăn, thủng.
(e) Đúng, chuối xanh chứa tinh bột nên tạo màu xanh tím với iot.
Chọn D
Câu 29:
Hòa tan hết hỗn hợp gồm Na và Ba vào nước, thu được dung dịch X và V lít khí (ở đktc). Dung dịch X có thể hòa tan được tối đa 8,1 gam nhôm. Giá trị của V là?
 Xem đáp án
Xem đáp án
2H2O + 2e —> 2OH- + H2
Al + H2O + OH- —> AlO2- + 1,5H2
nAl = 0,3 —> nOH- = 0,3 —> nH2 = 0,15 —> V = 3,36 lít
Chọn A
Câu 30:
Cho hỗn hợp X gồm 6,72 gam Fe và 0,24 mol Cu vào dung dịch AgNO3 đến khi phản ứng hoàn toàn, thu được m gam chất rắn Y và dung dịch Z chứa 3 cation kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
nFe = 0,12
TH1: 3 ion kim loại là Fe3+, Cu2+, Ag+
—> nAg = 3nFe + 2nCu = 0,84 —> mAg = 90,72
—> Chọn B.
TH2: 3 ion kim loại là Fe3+, Fe2+, Cu2+
—> 2nFe + 2nCu < nAg < 3nFe + 2nCu
—> 0,72 < nAg < 0,84 —> 77,76 < mAg < 90,72
—> Không có lựa chọn phù hợp.
Chọn B
Câu 31:
Tiến hành điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi. Kết quả quá trình điện phân được ghi theo bảng sau:
|
Thời gian |
Catot (-) |
Anot (+) |
|
t (giây) |
Khối lượng tăng 15,36 gam |
3,36 lít hỗn hợp khí (đktc) |
|
2t (giây) |
Khối lượng tăng 23,04 gam |
V lít hỗn hợp khí (đktc) |
Nhận định nào sau đây đúng?
 Xem đáp án
Xem đáp án
Sau t giây:
Catot: nCu = 0,24
Anot: nCl2 = a và nO2 = b —> a + b = 0,15
Bảo toàn electron: 2a + 4b = 0,24.2
—> a = 0,06 và b = 0,09
Sau 2t giây, ne trao đổi = 0,24.2.2 = 0,96
Catot: nCu = 0,36, bảo toàn electron —> nH2 = 0,12
Anot: nCl2 = 0,06, bảo toàn electron —> nO2 = 0,21
—> n khí anot lúc 2t = 0,27 —> V = 6,048 (A đúng, D sai)
nCuSO4 = 0,36 và nKCl = 2a = 0,12 —> m = 66,54 (B, C sai)
Chọn A
Câu 32:
Hòa tan hoàn toàn m gam hỗn hợp X chứa FeO, Fe2O3, Fe3O4 và FeCO3 bằng dung dịch chứa HCl (vừa đủ) thu được 0,04 mol CO2 và dung dịch Y có chứa 24,43 gam hỗn hợp muối FeCl3 và FeCl2. Cho NaOH dư vào Y trong điều kiện không có không khí thấy xuất hiện 16,66 gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Y chứa FeCl3 (a) và FeCl2 (b) —> 162,5a + 127b = 24,43
m↓ = 107a + 90b = 16,66
—> a = 0,08; b = 0,09
Bảo toàn Cl —> nHCl = 3a + 2b = 0,42
Bảo toàn H —> nH2O = 0,21
Bảo toàn khối lượng:
mX + mHCl = m muối + mCO2 + mH2O
—> mX = 14,64 gam
Chọn D
Câu 33:
X là hợp chất hữu cơ mạch hở có công thức phân tử C6H8O4. Cho các phản ứng sau (theo đúng tỉ lệ mol phản ứng)
(1) X + 2NaOH → Z + T + H2O
(2) T + H2 → T1
(3) Z + H2SO4 → Z1 + Na2SO4
Biết Z1 và T1 có cùng số nguyên tử cacbon; T là hợp chất hữu cơ đơn chức, no. Có các phát biểu sau:
(a) Nung Z với hỗn hợp với tôi xút thu được ankan đơn giản nhất.
(b) T1 không tác dụng với Na
(c) Tổng số nguyên tử hidro trong Z1 bằng 2.
(d) X không có đồng phân hình học
(c) Số nguyên tử trong một phân tử T bằng 10
Số phát biểu đúng là?
 Xem đáp án
Xem đáp án
Z1 và T1 cùng C —> Z và T cùng C —> Mỗi chất 3C
T là hợp chất hữu cơ đơn chức, no và có phản ứng cộng H2 nên T là anđehit hoặc xeton.
X là:
HOOC-CH2-COO-CH=CH-CH3
HOOC-CH2-COO-C(CH3)=CH2
Z là CH2(COONa)2, Z1 là CH2(COOH)2
T là C2H5CHO hoặc CH3COCH3; T1 là C2H5CH2OH hoặc CH3CHOHCH3
(a) Đúng:
CH2(COONa)2 + NaOH —> CH4 + Na2CO3
(b) Sai, T1 là ancol nên có tác dụng với Na.
(c) Sai, Z1 có 4H
(d) Sai, tùy cấu tạo, cấu tạo đầu của X có đồng phân hình học.
(e) Đúng, T có công thức C3H6O, tổng 10 nguyên tử.
Chọn C
Câu 34:
Hòa tan hết 9,6 gam kim loại Mg trong dung dịch HNO3 loãng, thu được 1,4336 lít khi N2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
nMg(NO3)2 = nMg = 0,4; nN2 = 0,064
Bảo toàn electron: 2nMg = 10nN2 + 8nNH4NO3
—> nNH4NO3 = 0,02
—> m muối = mMg(NO3)2 + mNH4NO3 = 60,8 gam
Chọn C
Câu 35:
Cho các nhân định
- Trong quả nho chín có nhiều đường glucozơ
- Trong mật ong có nhiều đường fructozo (khoảng 40%)
- Fructozơ có trong nhiều loại quả ngọt như dứa, xoài.
- Hàm lượng glucozơ trong máu người khoảng 0,1%
- Trong các loại đường glucozơ, fructozơ, saccarozơ thì đường saccarozơ có vị ngọt nhất.
Số nhận định đúng?
 Xem đáp án
Xem đáp án
4 nhận định đầu đúng. Nhận định cuối sai, fructozơ có vị ngọt nhất trong số 3 đường kể trên.
Chọn C
Câu 36:
A trong sơ đồ phản ứng sau là hợp chất hữu cơ đa chức, có công thức phân tử C4H6O4:
(1) A + 2NaOH → X (muối) + Y (muối) + Z (ancol)
(2) 2X + H2SO4 → 2T + Na2SO4
Biết MX > MY. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
A là HCOO-CH2-COO-CH3
X là HO-CH2-COONa
Y là HCOONa
Z là CH3OH
T là HO-CH2-COOH
A. Đúng, X và Y đều là muối (có COONa) và MX > MY nên nhiệt độ sôi của X lớn hơn Y.
B. Đúng
C. Đúng: T + 2Na —> NaO-CH2-COONa + H2
D. Sai, X và Y không cùng dãy đồng đẳng.
Chọn D
Câu 37:
Đốt cháy hoàn toàn m gam triglixerit X cần vừa đủ 3,465 mol O2, thu được H2O và 2,475 mol CO2. Cho m gam X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và 39,78 gam muối. Mặt khác, m gam X tác dụng được tối đa với a mol Br2 trong dung dịch. Giá trị của a là?
 Xem đáp án
Xem đáp án
Đặt nX = x, nH2O = y.
Bảo toàn O: 6x + 3,465.2 = y + 2,475.2
Bảo toàn khối lượng:
(16.6x + 2y + 2,475.12) + 40.3x = 39,78 + 92x
—> x = 0,045; y = 2,25
nX = x = [2,475 – (y + a)]/2 —> a = 0,135
Chọn C
Câu 38:
Hỗn hợp X gồm 1 axit cacboxylic đơn chức Y, không no, mạch hở có một liên kết đôi C=C và 1 este đơn chức Z no, mạch hở (cùng số mol với Y). Đốt cháy hoàn toàn 0,2 mol X thì thu được 11,2 lít CO2 (dktc) và m gam H2O. Khối lượng của X là
 Xem đáp án
Xem đáp án
Đặt y, z là số C của Y, Z; nY = nZ = 0,1
—> nCO2 = 0,1y + 0,1z = 0,5 —> y + z = 5
y ≥ 3 và z ≥ 2 —> y = 3, z = 2 là nghiệm duy nhất.
Y là C2H3COOH và Z là HCOOCH3 —> mX = 13,2 gam
Chọn C
Câu 39:
Hỗn hợp X có khối lượng 26,28 gam gồm metan, propan, etilen, propen có tổng số mol là 0,78 mol. Đốt cháy hoàn toàn 26,28 gam X cần 2,91 mol O2. Mặt khác 26,28 gam X phản ứng với tối đa a mol Br2 trong dung dịch. Giá trị của a là
 Xem đáp án
Xem đáp án
Đốt X tạo nCO2 = u và nH2O = v
mX = 12u + 2v = 26,28
Bảo toàn O —> 2u + v = 2,91.2
—> u = 1,83; v = 2,16
nX = (a + v) – u = 0,78 —> a = 0,45
Chọn D
Câu 40:
X là muối ngậm nước của kim loại M. Nung nóng m gam X đến khối lượng không đổi được 4,0 gam chất rắn Y và 10,8 gam hỗn hợp khí và hơi Z. Hấp thụ hoàn toàn Z vào 50 gam dung dịch NaOH 8,0% được dung dịch T chỉ chứa một chất tan có nồng độ 13,98%. Biết rằng quá trình nhiệt phân không làm thay đổi số oxi hoá của M. Phần trăm khối lượng của nguyên tố oxi trong X gần nhất với giá trị nào sau đây ?
 Xem đáp án
Xem đáp án
nNaOH = 50.8%/40 = 0,1
mT = mZ + mddNaOH = 60,8
—> m chất tan = 60,8.13,98% = 8,5
Phân tử chất tan có x nguyên tử Na —> Mol chất tan = 0,1/x
—> M chất tan = 8,5x/0,1 = 85x
Chọn x = 1; M = 85: Chất tan là NaNO3 (0,1 mol)
—> 10,8 gam Z gồm NO2 (0,1); O2 (0,1/4 = 0,025) và H2O (0,3)
%O = 16(0,1.3 + 0,3)/(4 + 10,8) = 64,86%
Chọn D
