25 Đề thi thử THPT Quốc Gia môn Hóa năm 2022 (Đề 6)
-
6472 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Trong số các kim loại: Al, Fe, Ag, Cu, kim loại nào có tính khử mạnh nhất?
 Xem đáp án
Xem đáp án
Đáp án C
Thứ tự giảm dần của tính khử: Al, Fe, Cu, Ag.
Câu 2:
Ở nhiệt độ thường, kim loại kali phản ứng với nước tạo thành
 Xem đáp án
Xem đáp án
Đáp án D
PTHH: 2K + 2H2O → 2KOH + H2
Câu 3:
Ion kim loại X khi vào cơ thể vượt mức cho phép sẽ gây nguy hiểm với sự phát triển cả về trí tuệ và thể chất con người. Ở các làng nghề tái chế ắc quy cũ, nhiều người bị ung thư, trẻ em chậm phát triển trí tuệ, còi cọc vì nhiễm độc ion kim loại này. X là
 Xem đáp án
Xem đáp án
Đáp án B
- Chì là một kim loại nặng, độc hại .Chì có màu trắng xanh khi mới cắt nhưng bắt đầu xỉn màu thành xám khi tiếp xúc với không khí. Chỉ dùng trong xây dựng, ắc quy chì, đạn, và là một phần của nhiều hợp kim. - Khi tiếp xúc ở một mức độ nhất định, chỉ là chất độc đối với động vật cũng như con người. Nó gây tổn thương cho hệ thần kinh và gây ra rối loạn não. Tiếp xúc ở mức cao cũng gây ra rối loạn máu ở động vật. Giống với thủy ngân, chì là chất độc thần kinh tích tụ trong mô mềm và trong xương.
Câu 4:
Chất béo nào sau đây là chất rắn ở điều kiện thường?
 Xem đáp án
Xem đáp án
Đáp án D
Chất béo no là chất rắn ở điều kiện thường.
Câu 5:
Kim loại nào sau đây phản ứng được với dung dịch NaOH?
 Xem đáp án
Xem đáp án
Đáp án D
Al phản ứng với nước trong môi trường kiềm.
PTHH: 2Al + 2H2O + 2NaOH → 2NaAlO2 + 3H2.
Câu 6:
Số đồng phân cấu tạo thuộc loại amin bậc 1 có công thức phân tử C3H9N là:
 Xem đáp án
Xem đáp án
Đáp án B
Các đồng phân bậc 1: CH3CH2CH2NH2, CH3CH(CH3)NH2.
Câu 7:
Nhúng 2 đũa thủy tinh vào 2 bình đựng HCl đặc và NH3 đặc, sau đó đưa 2 đũa lại gần thì thấy xuất hiện
 Xem đáp án
Xem đáp án
Đáp án A
NH3 đặc phản ứng với HCl đặc tạo thành NH4Cl tinh thể màu trắng.
PTHH: NH3 + HCl → NH4Cl.
Câu 9:
Polime có cấu trúc mạng không gian là
 Xem đáp án
Xem đáp án
Đáp án D
Tổng hợp nhựa bakelit:
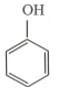 |
+ |
Cấu tạo mạch polime:
- Mạch không phân nhánh: amilozơ, nilon-6,6,..
- Mạch phân nhánh: aminlopectin, glicogen,...
- Mạch không gian: nhựa bakelit, cao su lưu hóa,...
Câu 10:
Nguyên tắc chung để điều chế kim loại là
 Xem đáp án
Xem đáp án
Đáp án A
Nguyên tắc chung để điều chế kim loại là khử cation kim loại: Mn+ + ne → M.
Câu 11:
Để chứng minh trong phân tử glucozơ có nhiều nhóm hiđroxyl, dùng dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Dùng Cu(OH)2 ở nhiệt độ thường để chứng minh chất có từ 2 nhóm -OH liền kề trở lên. Hiện tượng là tạo phức xanh lam.
Câu 12:
Ancol nào sau đây tạo phức xanh lam với Cu(OH)2/NaOH?
 Xem đáp án
Xem đáp án
Đáp án C
Những chất có từ 2 nhóm -OH liền kề trở lên tác dụng được với Cu(OH)2/NaOH tạo phức xanh lam.
Câu 13:
Cho 3,6 gam FeO phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 14:
Hòa tan hoàn toàn 4,6 gam Na vào nước. Để trung hòa dung dịch sau phản ứng cần V ml dung dịch HCl 2M. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 15:
Cho các chất sau: glucozơ, ancol etylic, glixerol, axit axetic. Số chất tác dụng được với Cu(OH)2/NaOH là
 Xem đáp án
Xem đáp án
Đáp án C
Những chất tác dụng được với Cu(OH)2/NaOH: glucozơ, glixerol, axit axetic.
· Những chất hữu cơ tác dụng được với Cu(OH), NaOH:
- Những chất có từ 2 nhóm -OH liền kề trở lên như: glucozơ, fructozơ, saccarozơ, glixerol, etilen glicol,...
- Axit hữu cơ như: axit fomic, axit axetic,...
Câu 16:
Đun nóng 37,5 gam dung dịch glucozơ với lượng dư AgNO3 trong NH3 , thu được 6,48 gam bạc. Nồng độ phần trăm của dung dịch glucozơ là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 17:
Công thức phân tử của amin no, đơn chức, mạch hở chứa 19,178% N về khối lượng là
 Xem đáp án
Xem đáp án
Đáp án A
CT tổng quát của amin no đơn chức mạch hở:
→ Amin là C4H11N
Câu 18:
Trong các chất sau: CH4, CO, CCl4, HCHO, CaC2, CO2, H2CO3, CH3COOH. Số hợp chất hữu cơ là
 Xem đáp án
Xem đáp án
Đáp án B
Các hợp chất hữu cơ là: CH4, CCl4, HCHO, CH3COOH.
Hợp chất hữu cơ là hợp chất của cacbon trừ: CO, CO2, muối cacbonat, xinanua, cacbua,...
Câu 19:
Dãy gồm tất cả các chất điện li mạnh là
 Xem đáp án
Xem đáp án
Đáp án D
Các chất điện li mạnh gồm: axit mạnh, bazơ mạnh và muối tan.
Câu 20:
Cho một số tính chất sau: (1) có dạng sợi, (2) tan trong nước, (3) tan trong nước Svayde, (4) phản ứng với axit nitric đặc (xúc tác axit sunfuric đặc), (5) tham gia phản ứng tráng bạc, (6) bị thuỷ phân trong dung dịch axit đun nóng. Những tính chất nào là của xenlulozơ
 Xem đáp án
Xem đáp án
Đáp án D
Xenlulozơ không tan trong nước và không tham gia phản ứng tráng bạc.
Câu 21:
Cho các dung dịch loãng: CuCl, HNO3, Fe,(SO4)3, HCl. Số dung dịch phản ứng được với Fe là
 Xem đáp án
Xem đáp án
Đáp án D
Các dung dịch phản ứng với Fe: CuCl2, HNO3, Fe2(SO4)3, HCl.
Câu 22:
Cho dãy các chất: phenyl axetat, anlyl axetat, metyl axetat, etyl fomat, tripanmitin. Số chất trong dãy khi thủy phân trong dung dịch NaOH (dư), đun nóng sinh ra ancol là
 Xem đáp án
Xem đáp án
Đáp án A
Các chất khi thủy phân trong dung dịch NaOH (dư), đun nóng sinh ra ancol là: anlyl axetat, metyl axetat, etyl fomat, tripanmitin.
Những chất thủy phân trong NaOH sinh ra ancol gồm:
- Chất béo
- Este: trừ este của phenol, este có dạng RCOOCH=CH-R, RCOOC(R')=CH-R"
Câu 24:
Cấu hình electron của ion Cr3+ là
 Xem đáp án
Xem đáp án
Đáp án C
Cấu hình electron của crom: [Ar]3d54s1.
Cấu hình electron của ion Cr3+:[Ar]3d3.
Câu 25:
Hòa tan hoàn toàn 47,4 gam phèn chua KAl(SO4)2.12H2O vào nước, thu được dung dịch X. Cho toàn bộ X tác dụng với 200 ml dung dịch Ba(OH)2 1M, sau phản ứng thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Các phản ứng xảy ra khi cho X tác dụng với dung dịch Ba(OH)2:
Không có kết tủa Al(OH)3, chỉ có kết tủa BaSO4.
Câu 26:
Cho 10,4 gam hỗn hợp X gồm axit axetic và etyl axetat tác dụng hoàn toàn với 150 gam dung dịch NaOH 5% (dùng dư 25% so với lượng cần vừa đủ cho phản ứng). Phần trăm khối lượng của etyl axetat trong X là
 Xem đáp án
Xem đáp án
Đáp án C
Ta có:
Câu 27:
Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án B
A sai vì mỡ động vật chủ yếu là chất béo rắn, cấu thành từ các gốc axit béo no.
C sai vì chất béo không tan hoặc ít tan trong nước.
D sai vì hiđro hóa chất béo không no thu được chất béo no nhưng không thể hiđro hóa dầu thực vật lỏng thu được mỡ động vật rắn.
Câu 28:
Cho hỗn hợp gồm: CaO, BaO, Al2O3 , Fe3O4 vào nước (dư), thu được dung dịch X và chất rắn Y. Sục khí CO2 đến dư vào dung dịch X, sau phản ứng xảy ra hoàn toàn thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án B
Al(OH)3 không tan trong CO2 dư, còn CaCO3, BaCO3 tan trong CO2 dư tạo muối axit.
Câu 29:
Hòa tan hết một lượng hỗn hợp gồm K và Na vào H2O dư, thu được dung dịch X và 0,672 lít khí H2 (đktc). Cho X vào dung dịch FeCl3 dư, đến khi phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 30:
Hỗn hợp khí X gồm propen, etan, buta-1,3-đien, but-1-in có tỉ khối hơi so với SO2 là 0,75. Đốt cháy hoàn toàn 0,02 mol hỗn hợp X, cho hấp thụ toàn bộ sản phẩm cháy vào bình dung dịch Ca(OH)2 dư thì thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
BT C:
Câu 31:
Cho hỗn hợp gồm Na và Al có tỉ lệ số mol tương ứng là 1: 2 vào nước (dư). Sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Vì nước dư nên Na phản ứng hết, m gam chất rắn không tan là Al dư.
Câu 32:
Cho các phát biểu sau:
(a) Peptit mạch hở phân tử chứa 2 liên kết peptit -CO-NH- được gọi là đipeptit.
(b) Trong dung dịch, glucozơ tồn tại chủ yếu ở dạng mạch vòng 6 cạnh (dạng α và dạng β).
(c) Anilin tham gia phản ứng thế brom vào nhân thơm dễ hơn benzen.
(d) Sản phẩm thủy phân xenlulozơ (xúc tác H+, nhiệt độ) có thể tham gia phản ứng tráng bạc.
(e) Phenyl axetat được điều chế bằng phản ứng giữa phenol và axit axetic.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
Những phát biểu đúng: (b), (c), (d).
(a) sai vì peptit mạch hở phân tử chứa 2 liên kết peptit -CO-NH- được gọi là tripeptit.
(d) đúng vì thủy phân xenlulozơ thu được glucozơ tham gia phản ứng tráng bạc.
(e) sai vì phenyl axetat được điều chế bằng phản ứng giữa phenol và anhiđric axetic (CH3CO)2O)
Câu 33:
Hòa tan hết m gam CuSO4.5H2O vào dung dịch chứa 0,24 mol NaCl, thu được dung dịch X. Điện phân X bằng dòng điện một chiều có cường độ không đổi (điện cực trơ, có màng ngăn, hiệu suất 100%). Sau thời gian t giây, thu được 3,136 lít (đktc) hỗn hợp hai khí ở cả hai điện cực. Sau thời gian 2t giây, khối lượng dung dịch giảm 13,92 gam so với dung dịch ban đầu. Bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Thứ tự điện phân: Sau thời gian t giây, khí cả 2 cực đều xuất hiện, nên H2O đã điện phân ở catot
BT e:
Sau thời gian 2t giây:
Khối lượng dung dịch giảm 13,92 gam bằng khối lượng kim loại tạo thành và khối lượng khí thoát ra.
Câu 34:
Hỗn hợp X gồm hai este, trong phân tử chỉ chứa một loại nhóm chức gồm este Y (CnHmO2) và este Z (CnH2n-4O4). Đốt cháy hoàn toàn 12,98 gam X cần dùng 0,815 mol O2 thu được 7,38 gam nước. Mặt khác đun nóng 12,98 gam X với dung dịch NaOH vừa đủ, thu được ancol etylic duy nhất có khối lượng 2,76 gam và hỗn hợp T gồm ba muối. Trị số của m là
 Xem đáp án
Xem đáp án
Đáp án C
nên chỉ có 1 trong 2 este tạo C2H5OH, este còn lại là este của phenol.
TH1: Nếu Y là este của phenol
BTKL:
TH2: Nếu Z là este của phenol
(loại).
Câu 35:
Cho từ từ dung dịch Ba(OH)2 đến dư vào dung dịch chứa AlCl3 x (mol/l) và Al2(SO4)3 y (mol/l). Phản ứng được biểu diễn theo đồ thị sau:
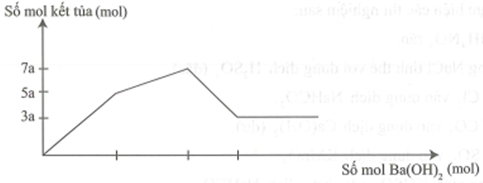
Tỉ lệ x : y là
 Xem đáp án
Xem đáp án
Đáp án B
Giai đoạn 1: Đồ thị dốc chứng tỏ lượng kết tủa tăng nhanh: Al2(SO4)3 tác dụng với Ba(OH)2
Al2(SO4)3 + 3Ba(OH)2 →3BaSO4 + 2Al(OH)2 +H2O
y → 3y 3y 2y
Giai đoạn 2: AlCl3 tác dụng với Ba(OH)2
2A1C13 + 3Ba(OH)2 → 2Al(OH)2 +3BaCl2
x 1,5x x
Lúc kết tủa 5a: giai đoạn 1:
Lúc kết tủa 7a: giai đoạn 1 + 2:
Câu 36:
Cho các phát biểu sau:
(a) Este là hợp chất hữu cơ trong phân tử có nhóm (COO-)
(b) Trong công nghiệp, glucozơ được chuyển hoá từ saccarozơ dùng để tráng gương, tráng ruột phích.
(c) Các amino axit thiên nhiên (hầu hết là α-amino axit) là những hợp chất cơ sở để kiến tạo nên các loại protein của cơ thể sống.
(d) Polietilen, poli(vinyl clorua),... có tính cách điện, cách nhiệt.
(e) Do có khả năng hoà tan tốt nhiều chất nên một số este được dùng làm dung môi để tách, chiết chất hữu cơ (etyl axetat), pha sơn (butyl axetat).
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
Những phát biểu đúng: (b), (c), (d), (e).
(a) sai vì có nhóm (COO-) là muối.
Câu 37:
Hòa tan hết 8,72 gam hỗn hợp FeS2, FeS và Cu vào 400 ml dung dịch HNO3 4M, sản phẩm thu được gồm dung dịch X và một chất khí thoát ra. Nếu cho dung dịch BaCl2 dư vào dung dịch X thì thu được 27,96 gam kết tủa, còn nếu cho dung dịch Ba(OH)2 dư vào dung dịch X thì thu được 36,92 gam kết tủa. Mặt khác, dung dịch X có khả năng hòa tan tối đa m gam Cu. Biết trong các quá trình trên, sản phẩm khử duy nhất của N+5 đều là NO. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
BT
Câu 38:
Hỗn hợp X gồm metyl aminoaxetat (NH-CH2-COOCH3), axit glutamic và vinyl fomat. Hỗn hợp Y gồm etilen và metylamin. Để đốt cháy hoàn toàn x mol X và y mol Y thì tổng số mol O2 cần dùng vừa đủ là 2,28 mol; thu được H2O, 0,2 mol N2 và 1,82 mol CO2. Mặt khác, để phản ứng hết với x mol X cần vừa đủ V ml dung dịch KOH 2M, đun nóng. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án A
Xem hỗn hợp X và Y gồm:
Cơ sở của phương pháp quy đổi này:
Metyl aminoaxetat: 1 COO, 2CH2 , 1 NH3.
Axit glutamic: 2COO, 3 CH3, 1 NH3.
Vinyl fomat: 1 COO, 2 CH2.
Etilen: 2 CH2 .
Metylamin: 1 NH3, 1 CH2.
Câu 39:
Thực hiện các thí nghiệm sau:
(a) Nung NH4NO3 rắn.
(b) Đun nóng NaCl tinh thể với dung dịch H2SO4 (đặc).
(c) Sục khí Cl2 vào dung dịch NaHCO3.
(d) Sục khí CO2 vào dung dịch Ca(OH)2 (dư).
(e) Sục khí SO2 vào dung dịch KMnO4.
(g) Cho dung dịch KHSO4 vào dung dịch NaHCO3.
(h) Cho PbS vào dung dịch HCl (loãng).
(i) Cho Na2CO3 vào dung dịch H2SO4 (dư), đun nóng.
Số thí nghiệm sinh ra chất khí là
 Xem đáp án
Xem đáp án
Đáp án B
(a) NH4NO3 → NO↑ + 2H2O
(b) H2SO3 + 2NaCl → Na2SO4 + 2HCl↑
(c) Cl2 + 2NaHCO3 → H2O + NaCl + 2CO3↑ + NaClO
(d) CO2 + Ca(OH)2 dư → CaCO3 + H2O
(e) 5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
(g) 2KHSO4 + 2NaHCO3 → Na2SO3 + K2SO4 + 2CO2↑ + 2H2O
(i) 3Na2CO3 + Fe2(SO4)3 + 3H2O → 2Fe(OH)2 + 3Na2SO4 + 3CO2↑
- Ở phản ứng (b), cần lưu ý là HCl tạo thành ở trạng thái khí, được gọi là hiđroclorua.
- Ở phản ứng (i), ban đầu phản ứng tạo thành Fe2(CO3)3 nhưng chất này không bền bị phân hủy tạo khí CO2. Tương tự với Al2(CO3)3.
Câu 40:
Chia m gam hỗn hợp T gồm các peptit mạch hở thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một bằng một lượng oxi vừa đủ thu được N2, CO2 và H2O (trong đó tổng số mol O2 và H2O là 0,885 mol). Thủy phân hoàn toàn phần hai, thu được hỗn hợp X gồm Ala, Gly, Val. Cho X tác dụng với 200ml dung dịch KOH 1M, thu được dung dịch Y chứa 20,86 gam chất tan. Để tác dụng vừa đủ với Y cần 340ml dung dịch HCl 1M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Xem giai đoạn hỗn hợp X tác dụng với KOH thu được Y, sau đó Y tác dụng vừa đủ với HCl là hỗn hợp X và KOH cùng tác dụng với HCl
Vậy khi amino axit tác dụng với KOH, số mol KOH dư là: 0,2 - 0,14 = 0,06
