20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án ( Đề 5)
-
4519 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại Al không tan trong dung dịch nào sau đây?
 Xem đáp án
Xem đáp án
Các phương trình phản ứng:
Dung dịch NH3 có tính bazơ yếu nên không thể hòa tan với Al
Chọn đáp án D.
Câu 2:
Kim loại nào sau đây thuộc nhóm VIIIB trong bảng tuần hoàn hóa học?
 Xem đáp án
Xem đáp án
Cấu hình electron của Fe là , nguyên tử Fe có tổng số electron phân lớp là 8, electron cuối cùng điền vào phân lớp 3d, vậy Fe sẽ thuộc nhóm VIIIB
Chọn đáp án C.
Câu 3:
Thuốc nổ đen chứa cacbon, lưu huỳnh và kali nitrat. Công thức hóa học của kali nitrat là
 Xem đáp án
Xem đáp án
Gốc nitrat là gốc axit của axit nitric HNO3. Vậy KNO3 có tên là: Kali nitrat.
Chọn đáp án B.
Câu 4:
Axit béo X có 3 liên kết trong phân tử, X là?
 Xem đáp án
Xem đáp án
Axit linoleic có công thức là C17H31COOH, có (2 liên kết trong gốc hidrocacbon và 1 liên kết trong nhóm COOH)
Chọn đáp án D.
Câu 5:
Chất nào sau đây là chất điện ly mạnh?
 Xem đáp án
Xem đáp án
Chất điện ly mạnh bao gồm:
- Các axit mạnh: HCl, H2SO4, HNO3, HBr, HI, HClO3, HClO4.
- Các bazo mạnh: NaOH, KOH, Ba(OH)2, Ca(OH)2
- Hầu hết các muối (kể cả muối kết tủa)
Chọn đáp án C.
Câu 6:
Cho các dung dịch sau: C6H5NH2 (anilin), , , C2H5NH2, . Số dung dịch làm đổi màu quỳ tím là
 Xem đáp án
Xem đáp án
Ta có:
C6H5NH2 (anilin): amin có tính bazo yếu do nhóm phenyl hút e trên nguyên tử Nitơ nên không làm quỳ chuyển màu
: aminnoaxit có số nhóm nên không làm quỳ chuyển màu vì môi trường gần như trung tính
: làm quỳ chuyển đỏ vì số nhóm nhiều hơn số nhóm
C2H5NH2: làm quỳ chuyển xanh
: làm quỳ chuyển xanh vì số nhóm nhiều hơn số nhóm .
Chọn đáp án D.
Câu 7:
Cho dung dịch NaHSO4 dư vào dung dịch chất X, thu được kết tủa màu trắng. Chất X là
 Xem đáp án
Xem đáp án
Ta có phương trình phản ứng
Chọn đáp án B.
Câu 8:
X là chất rắn màu trắng, dễ nghiền thành bột mịn, tạo được loại bột nhão có khả năng đông cứng nhanh khi nhào bột với nước; thường dùng để nặn tượng, đúc khuôn, bó bột khi gãy xương. Công thức hóa học của X là
 Xem đáp án
Xem đáp án
Ứng dụng của thạch cao nung, công thức là
Chọn đáp án C.
Câu 9:
Cao su Buna - N có tính chống dầu khá cao, được điều chế từ phản ứng đồng trùng hợp buta-1,3-đien với
 Xem đáp án
Xem đáp án
Điều chế cao su Buna - N
Chú ý: tên gọi Buna-N có ý nghĩa: điều chế từ đồng trùng Butadien (Bu), có xúc tác Na (Na), và đồng trùng hợp acrilonitrin (có chứa N)
Chọn đáp án C.
Câu 10:
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy oxit tương ứng?
 Xem đáp án
Xem đáp án
Các kim loại có tính khử mạnh: kim loại kiềm, kiềm thổ và Al thì chỉ có 1 cách duy nhất điều chế là điện phân nóng chảy.
Thường hay điện phân nóng chảy muối clorua, riêng trường hợp AlCl3 có tính chất dễ thăng hoa (chuyển từ trạng thái rắn sang trạng thái hơi mà không qua trạng thái lỏng) nên không thể điện phân nóng chảy, thay vào đó người ta điện phân Al2O3
Chọn đáp án B.
Câu 11:
Cho các chất: xenlulozơ, amilozơ, saccarozơ, amilopectin. Số chất chỉ được tạo nên từ các mắt xích -glucozơ là
 Xem đáp án
Xem đáp án
Chất chỉ được tạo nên từ các mắt xích -glucozơ là amilozơ và amilopectin.
Chọn đáp án A.
Câu 12:
Trong số hợp chất của crom, chất nào sau đây là chất rắn, màu lục thẫm, không tan trong nước (ở điều kiện thường)?
 Xem đáp án
Xem đáp án
Cr2O3: màu lục thẫm, Cr(OH)3 màu lục xám, CrO3 màu đỏ thẫm, Cr(OH)2 màu vàng.
Chọn đáp án C.
Câu 13:
Cho 16,25 gam Zn vào 200 ml dung dịch FeSO4 1M, sau phản ứng thu được m gam hỗn hợp kim loại X. Hòa tan m gam X bằng dung dịch HCl dư thấy thoát ra V lít H2 (đktc). Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
 Xem đáp án
Xem đáp án
Bảo toàn mol electron:
Câu 14:
Cho V ml dung dịch HCl 1M vào 300ml dung dịch NaAlO2 0,5M, sau khi các phản ứng xảy ra hoàn toàn thu được 5,85 gam kết tủa. Giá trị lớn nhất của V là
 Xem đáp án
Xem đáp án
Công thức tính nhanh
trong đó
Chọn đáp án A.
Câu 15:
Cho các chất sau: anilin, phenylamoni clorua, alanin, lysin, metyl butirat. Số chất trong dãy tác dụng được với dung dịch H2SO4 loãng (ở điều kiện thích hợp) là
 Xem đáp án
Xem đáp án
Chất trong dãy tác dụng được với dung dịch H2SO4 loãng là anilin, alamin, lysin.
Chọn đáp án A.
Câu 16:
Thủy phân hoàn toàn 3,42 gam saccarozơ trong môi trường axit, thu được dung dịch X. Cho toàn bộ dung dịch X phản ứng hết với lượng dư dung dịch AgNO3 trong NH3, đun nóng, thì thu được m gam Ag. Giá trị của m là
 Xem đáp án
Xem đáp án
Ta có:
(do cả Glucozơ và Fructozo đều tham gia tráng bạc với tỷ lệ 1 mol Glucozơ/Fructozơ tạo 2 mol Ag)
Chọn đáp án C.
Câu 17:
Cho 0,1 mol tác dụng với 150 ml dung dịch HCl 2M, thu được dung dịch X. Cho dung dịch X tác dụng với dung dịch NaOH dư, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Quy đổi: .
có
Bảo toàn khối lượng có:Câu 18:
Cho các phát biểu sau:
(1) Thành phần chính của tinh bột là amilozơ.
(2) Các gốc -glucozơ trong mạch Amilopectin liên kết với nhau bởi liên kết 1,4-glicozit và 1,6-glicozit.
(3) Tinh bột và xenlulozơ đều là polime có cấu trúc không phân nhánh.
(4). Tinh bột và xenlulozơ đều tan trong dung dịch H2SO4 khi đun nóng và tan trong nước svayde.
(5) Xenlulozơ được dùng để điều chế thuốc súng không khói, sản xuất tơ visco và tơ axetat.
(6) Nhỏ vài giọt dung dịch iot vào nhúm bông sẽ thấy nhúm bông chuyển thành màu xanh.
(7) Các hợp chất glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ đều chứa nhóm -OH trong phân tử.
Số phát biểu không đúng là
 Xem đáp án
Xem đáp án
Ta có:
(1) Thành phần chính của tinh bột là amilozơ (sai, thành phần chính là amilopectin).
(2) Các gốc -glucozơ trong mạch Amilopectin liên kết với nhau bởi liên kết 1,4-glicozit và 1,6-glicozit (đúng).
(3) Tinh bột và xenlulozơ đều là polime có cấu trúc không phân nhánh (sai, dạng amylopectin của tinh bột là polime có nhánh).
(4). Tinh bột và xenlulozơ đều tan trong dung dịch H2SO4 khi đun nóng và tan trong nước svayde (sai, tinh bột không tan trong nước Svayde).
(5) Xenlulozơ được dùng để điều chế thuốc súng không khói, sản xuất tơ visco và tơ axetat (đúng).
(6) Nhỏ vài giọt dung dịch iot vào nhúm bông sẽ thấy nhúm bông chuyển thành màu xanh (sai, dung dịch Iot chỉ chuyển xanh khi tiếp xúc với tinh bột).
(7) Các hợp chất glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ đều chứa nhóm -OH trong phân tử (đúng).
Chọn đáp án D.
Câu 19:
Dãy các ion nào sau đây đồng thời tồn tại trong một dung dịch?
 Xem đáp án
Xem đáp án
Điều kiện để các ion cùng tồn tại trong dung dịch là chúng không được phản ứng với nhau.
A.
B.
C.
Chọn đáp án C.
Câu 20:
Cho vào một ống nghiệm khoảng 2 ml etyl axetat, sau đó thêm vào 1 ml dung dịch H2SO4 20% và đun nhẹ (hoặc đun cách thủy). Sau một thời gian, kết quả thu đựơc là
 Xem đáp án
Xem đáp án
Phản ứng thủy phân Este trong môi trường axit là phản ứng thuận nghịch
Vậy sau phản ứng dung dịch có: CH3COOH, C2H5OH sinh ra và H2SO4 là chất xúc tác còn lại, riêng CH3COOC2H5 còn dư và không tan trong dung môi nước nên bị tách lớp.
Chọn đáp án C.
Câu 21:
Cho các phương pháp sau:
(a) Gắn kim loại kẽm vào kim loại sắt.
(b) Gắn kim loại đồng vào kim loại sắt.
(c) Phủ một lớp sơn lên bề mặt sắt.
(d) Tráng thiếc lên bề mặt sắt.
Số phương pháp điện hóa được sử dụng để bảo vệ kim loại sắt không bị ăn mòn là
 Xem đáp án
Xem đáp án
Phương pháp điện hóa sử dụng bảo vệ kim loại là (a), (b) nhưng trong đó chỉ có (a) là bảo vệ sắt không bị ăn mòn.
Chọn đáp án C.
Câu 22:
Cho các chất rắn sau: CrO3, Cr, Cr2O3, Cr(OH)3, K2Cr2O7, K2CrO4. Số chất tan hoàn toàn trong dung dịch NaOH loãng, dư là
 Xem đáp án
Xem đáp án
Chất tan hoàn toàn trong dung dịch NaOH loãng, dư là CrO3, Cr(OH)3, K2Cr2O7, K2CrO4.
Chọn đáp án A.
Câu 23:
Đốt cháy hoàn toàn m1 gam triglixerit X (mạch hở) cần dùng 1,55 mol O2 thu được 1,10 mol CO2 và 1,02 mol H2O. Cho 25,74 gam X tác dụng vừa đủ với dung dịch KOH thu được m2 gam muối. Giá trị của m2 là
 Xem đáp án
Xem đáp án
Ta có:
→ trong 25,74 (g) X thì
Khi cho X tác dụng với KOH thì:
Chọn đáp án C.
Câu 24:
Cho các loại tơ sau: tơ enang, tơ visco, tơ axetat, tơ nilon-6, tơ olon, tơ lapsan, tơ tằm, tơ nilon-6,6. Số tơ trong dãy thuộc loại tơ tổng hợp là
 Xem đáp án
Xem đáp án
Tơ thuộc loại tơ tổng hợp là tơ enang, tơ nilon-6, tơ lapsan, tơ nilon-6,6.
Chọn đáp án D.
Câu 25:
Hấp thụ hoàn toàn 0,5 mol CO2 vào dung dịch chứa Ba(OH)2 và 0,3 mol NaOH, thu được m gam kết tủa và dung dịch X chứa các muối. Cho từ từ dung dịch chứa HCl 0,3M và H2SO4 0,1M vào dung dịch X thấy thoát ra 3,36 lít CO2 (đktc) đồng thời thu được dung dịch Y. Cho dung dịch Ba(OH)2 dư vào dung dịch Y, thu được 29,02 gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Dung dịch X chứa Na+ (0,3 mol),
Khi cho từ từ axit vào muối thì:
Dung dịch Y có chứa
Khi cho Ba(OH)2 dư vào Y, thu được kết tủa
Từ (1), (2), (3) suy ra:
Chọn đáp án B.
Câu 26:
Este X hai chức, phân tử có chứa vòng benzen. Thủy phân hoàn toàn 0,1 mol X trong 300 ml dung dịch NaOH 1M đun nóng (phản ứng vừa đủ). Cô cạn dung dịch sau phản ứng, thu được 3,2 gam metanol và 25 gam hỗn hợp Y gồm hai muối khan. Số công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Vì X phản với NaOH theo tỉ lệ mol và có dạng
Hỗn hợp muối gồm R(COONa)2 và
Số công thức cấu tạo có thể có thỏa mãn là
Chọn đáp án D.
Câu 27:
Cho các sơ đồ phản ứng sau (theo đúng tỉ lệ mol)
 Xem đáp án
Xem đáp án
Vậy X có CTPT là C8H14O5
Chọn đáp án C.
Câu 28:
Cho các thí nghiệm sau:
(1) Sục khí CO2 dư vào dung dịch chứa Ba(OH)2.
(2) Cho dung dịch Ba(OH)2 dư vào dung dịch chứa phèn chua.
(3) Sục khí NH3 dư vào dung dịch chứa AlCl3.
(4) Cho từ từ dung dịch HCl dư vào dung dịch chứa NaAlO2.
(5) Sục khí HCl dư vào dung dịch chứa AgNO3.
(6) Cho từ từ đến dư dung dịch Al(NO3)3 vào dung dịch KOH và khuấy đều.
Số thí nghiệm có kết tủa xuất hiện, sau đó kết tủa tan hết là
 Xem đáp án
Xem đáp án
(1) Ban đầu xuất hiện kết tủa trắng BaCO3 sau đó kết tủa tan tạo dung dịch trong suốt.
(2) Xuất hiện kết tủa trắng BaSO4 không tan.
(3) Xuất hiện kết tủa trắng Al(OH)3 không tan.
(4) Ban đầu xuất hiện kết tủa trắng Al(OH)3 sau đó kết tủa tan tạo dung dịch trong suốt.
(5) Xuất hiện kết tủa trắng AgCl không tan.
(6) Xuất hiện kết tủa trắng nhưng tan ngay, sau đó xuất hiện kết tủa lại và không tan.
Chọn đáp án A.
Câu 29:
Cho phát biểu sau:
(1) Phèn chua được dùng trong ngành thuộc da, công nghiệp giấy, chất cầm màu trong ngành nhuộm vải, chất làm trong nước…có công thức là KAl(SO4)2.24H2O.
(2) Dùng Ca(OH)2 với lượng dư để làm mất tính cứng tạm thời của nước.
(3) Khi nghiền clanhke, người ta trộn thêm 5-10% thạch cao để điều chỉnh tốc độ đông cứng của xi măng.
(4) NaHCO3 được dùng trong công nghiệp dược phẩm (chế thuốc đau dạ dày) và công nghiệp thực phẩm (làm bột nở,…).
(5) Xesi được dùng làm tế bào quang điện.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Ta có:
(1) Sai, Phèn chua có công thức là KAl(SO4)2.12H2O.
(2) Sai, Dùng Ca(OH)2 với lượng vừa đủ để làm mất tính cứng tạm thời của nước.
Chọn đáp án D.
Câu 30:
Hỗn hợp X gồm axetilen và etan có tỉ lệ mol tương ứng qua ống đựng xúc tác thích hợp, nung nóng ở nhiệt độ cao thu được hỗn hợp Y gồm etan, etilen, axetilen và H2. Tỉ khối của hỗn hợp Y so với hidro là . Nếu cho 0,65 mol Y qua dung dịch brom dư thì số mol Br2 phản ứng tối đa là
 Xem đáp án
Xem đáp án
Giả sử có 1mol C2H2 và 2 mol C2H6
mà
Ta có:
Vậy trong 0,65 mol Y có 0,5 mol brom tham gia phản ứng
Chọn đáp án B.
Câu 31:
Cho a gam hỗn hợp X gồm BaO và Al2O3 vào nước, thu được dung dịch Y. Cho dung dịch H2SO4 vào Y, khối lượng kết tủa (m, gam) theo số mol H2SO4 được biểu diễn theo đồ thị sau. Giá trị của a là
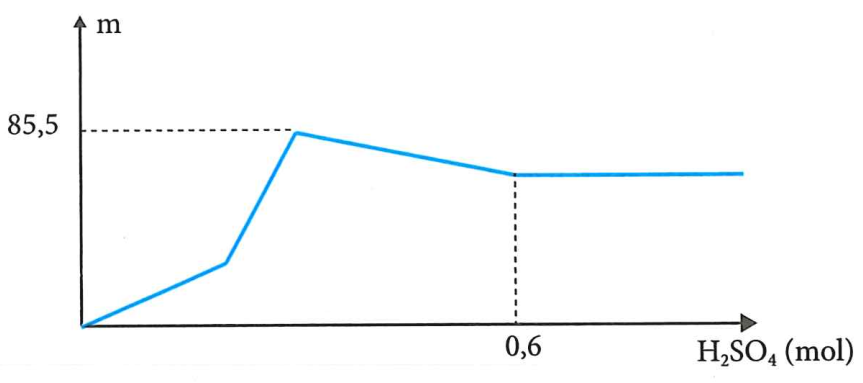
 Xem đáp án
Xem đáp án
Dung dịch Y chứa Ba(OH)2 (x mol) và Ba(AlO2)2 (y mol)
Tại
Tại
Từ (1), (2) suy ra: X gồm BaO (0,3 mol) và .
Chọn đáp án B.
Câu 32:
Cho các phát biểu sau:
(1) Tơ nilon-6,6 có thể điều chế bằng phản ứng trùng hợp hoặc trùng ngưng.
(2) Ở điều kiện thường metylamin, đimetylamin, trimetylamin là các chất khí, mùi khai, tan nhiều trong nước.
(3) Saccarozơ, tinh bột, xenlulozơ bị thủy phân trong môi trường kiềm cho -glucozơ.
(4) Oligopeptit gồm các peptit có từ 2 đến 10 liên kết peptit trong phân tử.
(5) Metyl metacrylat, glycozơ, triolein đều tham gia phản ứng với nước brom.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Ta có:
(1) Sai, Tơ nilon-6,6 điều chế bằng phản ứng trùng ngưng.
(3) Sai, Saccarozơ, tinh bột, xenlulozơ bị thủy phân trong môi trường axit thu được sản phẩm có chứa glucozơ.
(4) Sai, Oligopeptit gồm các peptit có từ 2 đến 10 gốc -amino axit trong phân tử.
Chọn đáp án D.
Câu 33:
Điện phân dung dịch chứa 14,28 gam hỗn hợp CuSO4 và NaCl bằng dòng điện một chiều có cường độ 4A (điện cực trơ, có màng ngăn, hiệu suất 100%). Sau thời gian t giây thì ngừng điện phân, thu được dung dịch X (có ) và 4,48 lít (đktc) hỗn hợp khí thoát ra ở cả hai điện cực, có tỉ khối so với He là 6,2. Bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của t là
 Xem đáp án
Xem đáp án
Đặt:
Chọn đáp án C.
Câu 34:
Đun nóng 29,84 gam hỗn hợp E chứa X (C4H14O3N2) và Y (C5H14O4N2) với 500ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng thu được hỗn hợp Z gồm 2 amin là đồng đẳng kế tiếp nhau có tỉ khối so với hiđro là 17,6 và hỗn hợp rắn T. Phần trăm khối lượng của muối có phân tử khối lớn nhất trong T là
 Xem đáp án
Xem đáp án
Nhận xét: X có công thức phân tử là C4H14O3N2 nên X là muối amonicacbonat có dạng , Y có công thức phân tử là C5H14O4N2 nên Y là muối amoni của axit cacboxylic 2 chức có dạng
Hoặc có thể biện luận theo công thức
Trong đó k: là độ bất bão hòa tính theo phân tử, : là số liên kết pi trong phân tử, i: là số liên kết ion trong phân tử.
Nếu muối amoni có 3 nguyên tử O thì có thể là 1 trong 3 muối: , , .
Nếu muối amoni có 2, 4 nguyên tử O thì là muối của axit cacboxylic đơn chức hoặc 2 chức.
Muối thu được gồm Na2CO3 (0,12 mol); CH2(COONa)2 (0,08 mol); NaOH dư (0,1 mol)
Chọn đáp án C.
Câu 35:
Hòa tan hoàn toàn 21,24 gam hỗn hợp gồm muối hiđrocacbonat (X) và muối cacbonat (Y) vào nước thu được 200 ml dung dịch Z. Cho từ từ 200 ml dung dịch KHSO4 0,3M và HCl 0,45M vào 200 ml dung dịch X, thu được 1,344 lít khí CO2 (đktc) và dung dịch T. Cho dung dịch Ba(OH)2 dư vào T, thu được 49,44 gam kết tủa. Biết X là muối của kim loại kiềm. Nhận định nào sau đây là sai?
 Xem đáp án
Xem đáp án
Ta có:
- Khi cho dung dịch Z tác dụng với dung dịch chứa 0,06 mol KHSO4 và 0,09 mol HCl thì:
- Khi cho dung dịch T tác dụng với Ba(OH)2 ta được:
,
Vậy trong T chứa 0,18 mol
- Vậy trong Z chứa 0,15 mol và 0,09 mol
- Giả sử X là muối NaHCO3, gọi muối của Y là A2(CO3)n ta có:
Vậy muối X là NaHCO3 và Y là (NH4)2CO3.
- Không xét tiếp các trường hợp còn lại vì trường hợp trên đã thỏa mãn.
A. Đúng, NaHCO3 (X) là muối natri hiđrocacbonat chiếm 59,32% về khối lượng hỗn hợp.
B. Đúng, (X) NaHCO3 và (Y) (NH4)2CO3 đều có tính lưỡng tính.
C. Sai, (Y) (NH4)2CO3 là muối amoni cacbonat chiếm 40,67% về khối lượng hỗn hợp.
D. Đúng (X) NaHCO3 và (Y) (NH4)2CO3 đều bị phân hủy bởi nhiệt.
Chọn đáp án C.
Câu 36:
Bộ dụng cụ kết tinh (được mô tả như hình vẽ dưới) dùng để
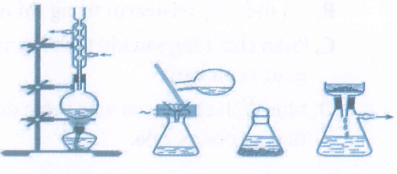
 Xem đáp án
Xem đáp án
Hai chất rắn có độ tan khác nhau, khi pha thành dung dịch và cho kết tinh trở lại ở các nhiệt độ khác nhau.
Chọn đáp án C.
Câu 37:
Có ba dung dịch riêng biệt: H2SO4 1M; Al2(SO4)3 1M; AlCl3 1M được đánh số ngẫu nhiên là (1), (2), (3). Tiến hành các thí nghiệm sau:
TN1: Trộn V ml (1) với V ml (2) và 3V ml dung dịch NaOH 1M thu được a mol kết tủa.
TN2: Trộn V ml (1) với V ml (3) và 3V ml dung dịch Ba(OH)2 1M thu được 5a mol kết tủa.
TN3: Trộn V ml (2) với V ml (3) và 4V ml dung dịch Ba(OH)2 1M thu được b mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn. So sánh nào sau đây đúng?
 Xem đáp án
Xem đáp án
Các dung dịch lần lượt là (1), (2), (3) lần lượt là AlCl3, H2SO4, Al2(SO4)3
Khi cho 1 mol H2SO4 và 1 mol .
Chọn đáp án A.
Câu 38:
 Xem đáp án
Xem đáp án
Dẫn toàn bộ ancol T qua bình đựng Na dư thì:
Ta có
Khi đốt F thì ta thu đựơc: mà
Xét hỗn hợp F ta có:
Vậy hai muối A và B lần lượt là HCOONa và C2H5COONa
→ X, Y và Z lần lượt là C2H4(OOCH)2HCOOCH2CH2OOCC2H5 và C2H4(OOCC2H5)2.
Vậy
Chọn đáp án D.
Câu 39:
Hòa tan hết 30,56 gam hỗn hợp gồm Mg, Fe3O4 và FeCO3 trong dung dịch chứa HCl và 0,24 mol HNO3, thấy thoát ra hỗn hợp khí X gồm CO2, No và 0,08 mol N2O; đồng thời thu được dung dịch Y có khối lượng tăng 22,60 gam so với dung dịch ban đầu. Tỉ khối hơi của X so với He bằng 9,95. Cho dung dịch AgNO3 đến dư vào dung dịch Y, thu được 0,03 mol khí NO (sản phẩm khử duy nhất của N+5) và 239,66 gam kết tủa. Phần trăm khối lượng của Fe3O4 có trong hỗn hợp ban đầu là
 Xem đáp án
Xem đáp án
Khối lượng dung dịch tăng:
và
Từ (1), (2) có:
Khi đó:
Ta có:
Kết tủa thu được gồm và
Từ (1), (2), (3) suy ra:
Chọn đáp án D.
Câu 40:
Tiến hành thí nghiệm xà phòng hóa tristearin theo các bước sau:
Bước 1: Cho vào bát sứ khoảng 1 gam tristearin và 2 – 2,5 ml dung dịch NaOH nồng độ 40%
Bước 2: Đun sôi nhẹ hỗn hợp khoảng 30 phút và khuấy liên tục bằng đũa thủy tinh, thỉnh thoảng thêm vài giọt nước cất.
Bước 3: Rót thêm vào hỗn hợp 4 – 5ml dung dịch NaCl bão hòa nóng, khuấy nhẹ rồi để nguội.
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Mục đích chính của việc thêm dung dịch NaCl bão hòa để thu lấy xà phòng một cách dễ dàng hơn vì xà phòng sẽ ở bên trên bề mặt chất lỏng sau khi thêm dung dịch NaCl bão hòa.
=> Phát biểu sai: “Mục đích chính của việc thêm dung dịch NaCl bão hòa là làm tăng tốc độ cho phản ứng xà phòng hóa”
Chọn đáp án D.
