20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
20 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án ( Đề 15)
-
4523 lượt thi
-
42 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây có tính khử yếu nhất?
 Xem đáp án
Xem đáp án
Tính khử theo dãy điện hóa Al > Cr > Fe > Cu.
Chọn đáp án D.
Câu 2:
Dung dịch nào sau đây không tác dụng với Al2O3?
 Xem đáp án
Xem đáp án
Al2O3 là chất lưỡng tính nên phản ứng được với axit, kiềm.
Chọn đáp án B.
Câu 3:
Trong các chất sau, chất không tác dụng với khí oxi là
 Xem đáp án
Xem đáp án
CO2 không thể phản ứng với O2 vì C đã đạt mức OXH cao nhất là +4.
Chọn đáp án C.
Câu 4:
Este nào sau đây có phản ứng tráng bạc?
 Xem đáp án
Xem đáp án
Những chất có phản ứng tráng bạc:
- Andehit.
- Tất cả các chất có dạng HCOOR (R có thể là H, gốc hiđrocacbon, Na+, …)
- Glucozơ, fructozơ.
Chọn đáp án C.
Câu 5:
Công thức của Natri cromat là
 Xem đáp án
Xem đáp án
Chú ý: natricromat là Na2CrO4 (dung dịch màu vàng) và natriđicromat là Na2Cr2O7 (dung dịch màu da cam), natricromit là NaCrO2.
Chọn đáp án B.
Câu 6:
Polime nào sau đây không được dùng làm chất dẻo?
 Xem đáp án
Xem đáp án
Poli acrilonitrin hay còn gọi là tơ olon, tơ nitron (nên thuộc loại tơ).
Chọn đáp án D.
Câu 7:
Chất nào sau đây vừa phản ứng với dung dịch NaOH vừa phản ứng với dung dịch HCl?
 Xem đáp án
Xem đáp án
Muối axit của axit yếu là chất lưỡng tính nên phản ứng với cả axit và kiềm.
Chọn đáp án D.
Câu 8:
Chất nào sau đây là chất lưỡng tính?
 Xem đáp án
Xem đáp án
Các hiđroxit lưỡng tính hay gặp là Cr(OH)3; Al(OH)3, Zn(OH)2, Be(OH)2
Cr(OH)2 là bazơ, CrO là oxit bazơ, CrO3 là oxit axit.
Chọn đáp án A.
Câu 9:
Chất nào sau đây không phải là chất điện ly?
 Xem đáp án
Xem đáp án
Các chất không chứa liên kết ion (chỉ có các liên kết cộng hóa trị) và không phản ứng với H2O (ở điều kiện thường) là các chất không điện ly.
Ví dụ: glucozơ, fructozơ, saccarozơ, các ancol…
Chọn đáp án B.
Câu 10:
Phản ứng giữa NH3 với chất nào sau đây chứng minh NH3 thể hiện tính bazơ.
 Xem đáp án
Xem đáp án
HCl phản ứng axit – bazơ với NH3 tạo muối amoni clorua.
Chọn đáp án C.
Câu 11:
Hợp chất nào sau đây không chứa Nitơ?
 Xem đáp án
Xem đáp án
Tripanmitin là chất béo (trieste) có công thức (C15H31COO)3C3H5 phân tử chỉ chứa 3 nguyên tố C, H, O.
Chọn đáp án B.
Câu 12:
Phản ứng nào sau đây không có kết tủa xuất hiện?
 Xem đáp án
Xem đáp án
(natriphenolat là muối và tan tốt trong nước)
Chọn đáp án C.
Câu 13:
Cho 10,4 gam hỗn hợp Mg và Fe tan hết trong dung dịch HCl dư thu được 6,72 lít khí (đktc). Phần trăm khối lượng của Fe trong hỗn hợp ban đầu là
 Xem đáp án
Xem đáp án
Đặt ẩn và giải hệ cơ bản:
Chọn đáp án A.
Câu 14:
Lượng kết tủa tạo thành khi trộn lẫn dung dịch chứa 0,0075 mol NaHCO3 với dung dịch chứa 0,01 mol Ba(OH)2 là
 Xem đáp án
Xem đáp án
0,0075 0,02 (dư) = 0,0075 mol
0,01 0,0075 0,0075
Chọn đáp án B.
Câu 15:
Trong phòng thí nghiệm quá trình điều chế etilen thường có lẫn khí CO2 và SO2. Để loại bỏ CO2 và SO2 người ta cho hỗn hợp khí đi qua dung dịch dư nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án D.
Câu 16:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Phenol là C6H5OH (có 6 nguyên tử H), anilin là C6H5NH2 (có 7 nguyên tử H)
Chọn đáp án C.
Câu 17:
Xà phòng hóa hoàn toàn 0,2 mol hỗn hợp gồm etyl axetat và vinyl axetat bằng 300ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng thu được m gam chất rắn. Giá trị của m là:
 Xem đáp án
Xem đáp án
Nhận thấy 2 este đều được tạo từ axit axetic.
Sau phản ứng ta có
Chú ý: có = 0,3 – 0,2 = 0,1 mol
mrắn = = 0,2.82 + 0,1.40 = 20,4 (g)
Chọn đáp án C.
Câu 18:
Cho 11,8 gam amin đơn chức X tác dụng vừa đủ với dung dịch HCl, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Làm bay hơi dung dịch Y thu được 19,1 gam muối khan. Số amin bậc I ứng với công thức phân tử của X là
 Xem đáp án
Xem đáp án
Bảo toàn khối lượng
Do amin đơn chức nên ta có Mamin =
C3H9N có 2 đồng phân amin bậc I: CH3 – CH2 – CH2 – NH2 và CH3 – CH(CH3) – NH2.
Chọn đáp án B.
Câu 19:
Cho HNO3 đặc nóng, dư tác dụng với các chất sau. S, FeCO3, CaCO3, Cu, Al2O3, FeS2, CrO. Số phản ứng HNO3 đóng vai trò chất oxi hóa là
 Xem đáp án
Xem đáp án
Các chất S, FeCO3, Cu, FeS2, CrO đóng vai trò là chất khử trong phản ứng với HNO3 do các nguyên tố chưa đạt số OXH cao nhất
.
Chọn đáp án A.
Câu 20:
Cho dãy các chất sau: Glucozơ, Saccarozơ, Ala – Gly – Glu, Ala – Gly, Glixerol. Số chất trong dãy có phản ứng với Cu(OH)2 tạo ra dung dịch màu xanh lam là
 Xem đáp án
Xem đáp án
Đáp án gồm: glucozơ, saccarozơ, glixerol
Các chất hữu cơ phản ứng với Cu(OH)2 tạo dung dịch xanh lam là:
- Ancol đa chức có ít nhất 2 nhóm –OH kề nhau.
- Axit cacboxylic
Chú ý: tripeptit cũng phản ứng với Cu(OH)2 nhưng tạo phức tím (phản ứng màu buire)
Chọn đáp án C.
Câu 21:
Cho các phát biểu sau:
1. Các chất Al, Al2O3, Al(OH)3 là những hợp chất lưỡng tính.
2. Phương pháp trao đổi ion làm mềm được nước cứng toàn phần.
3. Dung dịch HCl có pH lớn hơn dung dịch H2SO4 có cùng nồng độ mol.
4. Hàm lượng cacbon trong gang cao hơn trong thép.
5. Điện phân hỗn hợp dung dịch CuSO4 và NaCl có khí màu vàng lục thoát ra ở catot.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Số phát biểu đúng gồm (2) (3) và (4)
(1) Sai vì không có khái niệm “Kim loại lưỡng tính”.
(5) Sai vì khí Cl2 thoát ra ở anot.
Chọn đáp án B.
Câu 22:
Xà phòng hóa hoàn toàn este X (chỉ chứa nhóm chức este) trong dung dịch NaOH, thu được hỗn hợp các chất hữu cơ gồm. CH3COONa, NaO – C6H4CH2OH và H2O. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Kết hợp dữ kiện X chỉ chứa nhóm chức Este X là
Chọn đáp án A.
Câu 23:
Xà phòng hóa hoàn toàn este X (chỉ chứa nhóm chức este) trong dung dịch NaOH, thu được hỗn hợp các chất hữu cơ gồm. CH3COONa, NaO – C6H4CH2OH và H2O. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Kết hợp dữ kiện X chỉ chứa nhóm chức Este X là
Chọn đáp án A.
Câu 24:
Cho V lít CO2 (đktc) hấp thụ hết trong dung dịch chứa 0,2 mol Ba(OH)2 và 0,1 mol NaOH. Sau phản ứng hoàn toàn thu được kết tủa và dung dịch chỉ chứa 21,35 gam muối. V có giá trị là
 Xem đáp án
Xem đáp án
Nhận xét: kết tủa là BaCO3, dung dịch có thể chứa muối Na2CO3, NaHCO3 và Ba(HCO3)2
- Biện luận: nếu dung dịch chỉ có muối Na2CO3 và NaHCO3 thì (khoảng giá trị khi coi muối chỉ có Na2CO3 và NaHCO3), điều này vô lý theo đề bài. Vậy muối sẽ gồm (đã có thì không thể có trong dung dịch)
Câu 25:
Chất hữu cơ X có công thức phân tử C4H11NO2. Cho 15,75 gam X tác dụng được với dung dịch NaOH vừa đủ. Cô cạn dung dịch sau phản ứng thu được 10,2 gam chất rắn. Số công thức cấu tạo phù hợp với X là
 Xem đáp án
Xem đáp án
chắc chắn X là muối amoni (Nếu X chỉ là hợp chất có liên kết cộng hóa trị, trong phân tử có 2 nguyên tử O, lại phản ứng với NaOH nên chỉ có thể là nhóm este , vô lí).
X có 2O, nên X là muối amoni của axit cacboxylic mô hình của X là
các công thức cấu tạo của X thỏa mãn là:
Chọn đáp án B.
Câu 26:
Hòa tan hoàn toàn a mol Al2O3 vào dung dịch chứa 2a mol Ba(OH)2 thu được dung dịch X. Trong các chất NaOH, CO2, Fe(NO3)2, NH4Cl, NaHCO3, HCl, Al, Na2CO3. Số chất phản ứng được với dung dịch X là
 Xem đáp án
Xem đáp án
Sau khi hòa tan a mol Al2O3 vào 2a mol Ba(OH)2:
+ Vậy số chất có thể tác dụng với dung dịch X gồm:
CO2, Fe(NO3)2, NH4Cl, NaHCO3, HCl, Al và Na2CO3
Các phương trình phản ứng:
Câu 27:
Chia một lượng xenlulozơ thành hai phần bằng nhau. Cho phần một tác dụng với lượng dư dung dịch hỗn hợp HNO3/H2SO4, đun nóng, tách thu được 35,64 kg xenlulozơ trinitrat với hiệu suất 75%. Thủy phân phần hai với hiệu suất 80%, trung hòa dung dịch sau thủy phân rồi cho toàn bộ lượng sản phẩm sinh ra tác dụng với một lượng H2 dư (Ni, to) đến khi phản ứng xảy ra hoàn toàn thu được m kg sobitol. Giá trị của m là
 Xem đáp án
Xem đáp án
Ở phần 1 ta có phản ứng:
Phần 2 thủy phân xenlulozơ ta có phản ứng
Câu 29:
Tiến hành các thí nghiệm sau:
(a) Cho từ từ a mol HCl vào dung dịch chứa a mol Na2CO3.
(b) Sục khí Cl2 vào dung dịch NaOH loãng.
(c) Cho Fe3O4 vào dung dịch HNO3 loãng, dư.
(d) Cho Fe3O4 vào dung dịch H2SO4 loãng, dư.
(e) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2 dư.
(g) Cho dung dịch Al2(SO4)3 vào dung dịch Ba(OH)2 dư.
Sau khi kết thúc các phản ứng, số thí nghiệm tạo ra hai muối là
 Xem đáp án
Xem đáp án
Ta có các phản ứng sau:
Sau đó:
Thí nghiệm (a) (b) (d) (e) và (g) tạo 4 muối
Chọn đáp án D.
Câu 30:
Kết quả thí nghiệm của các chất X, Y, Z, T với một số thuốc thử được ghi ở bảng sau:
|
Chất |
X |
Y |
Z |
T |
|
Dung dịch nước brom |
|
Dung dịch mất màu |
Kết tủa trắng |
Dung dịch mất màu |
|
Kim loại Na |
Có khí thoát ra |
|
Có khí thoát ra |
Có khí thoát ra |
Các chất X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Vì Y làm mất màu nước brom Loại C.
Z có tạo kết tủa với nước brom Loại B và D
Chọn đáp án A.
Câu 31:
Kết quả thí nghiệm của các chất X, Y, Z, T với một số thuốc thử được ghi ở bảng sau:
|
Chất |
X |
Y |
Z |
T |
|
Dung dịch nước brom |
|
Dung dịch mất màu |
Kết tủa trắng |
Dung dịch mất màu |
|
Kim loại Na |
Có khí thoát ra |
|
Có khí thoát ra |
Có khí thoát ra |
Các chất X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Vì Y làm mất màu nước brom Loại C.
Z có tạo kết tủa với nước brom Loại B và D
Chọn đáp án A.
Câu 32:
 Xem đáp án
Xem đáp án
Sơ đồ ta có
Bảo toàn khối lượng:
Bảo toàn mol
Câu 33:
Nhỏ từ từ dung dịch Ba(OH)2 đến dư vào dung dịch chứa a mol Na2SO4 và b mol Al2(SO4)3. Lượng kết tủa tạo ra được biểu diễn bằng đồ thị bên:
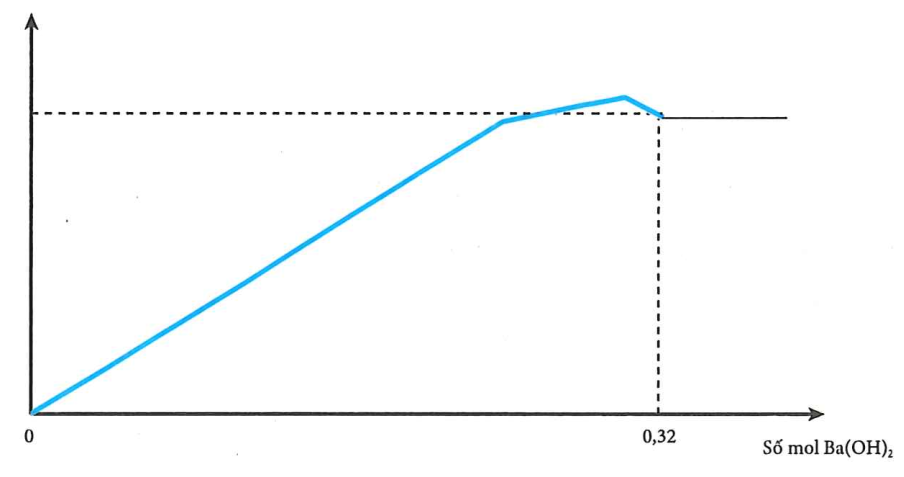
Giá trị của a là
 Xem đáp án
Xem đáp án
Ta có sơ đồ phản ứng sau
+ Từ sơ đồ trên ta có hệ phương trình:
- Biểu diễn phương trình theo số mol của
- Biểu diễn phương trình bằng định luật bảo toàn Ba: a + 3b + b = a + 4b = 0,32 (2)
+ Giải hệ (1) và (2) ta có
Chọn đáp án B
Câu 34:
Cho các chất Etilen, vinylaxetilen, benzen, toluen, triolein, anilin, stiren, isopren. Số chất tác dụng với dung dịch brom ở điều kiện thường là:
 Xem đáp án
Xem đáp án
Số chất tác dụng với dung dịch brom ở điều kiện thường gồm:
Eliten, vinylaxetilen, triolein, anilin, stiren và isopren.
Chọn đáp án A.
Câu 35:
Tiến hành điện phân (với điện cực trơ, hiệu suất 100%, dòng điện có cường độ không đổi) với dung dịch X gồm 0,2 mol CuSO4 và 0,15 mol HCl, sau một thời gian điện phân thu được dung dịch Y có khối lượng giảm 14,125 gam so với khối lượng dung dịch X. Cho 15 gam bột Fe vào Y đến khi kết thúc các phản ứng thu được m gam chất rắn. Biết các khí sinh ra hòa tan không đáng kể trong nước. Giá trị của m là
 Xem đáp án
Xem đáp án
Khối lượng dung dịch giảm gồm:
Dung dịch Y chứa CuSO4: 0,2 – 0,075 – 0,05 = 0,075 mol; H2SO4: 0,125 mol (bảo toàn nhóm )
Khi cho 15 gam bột Fe thì xảy ra phản ứng
Khối lượng chất rắn thu được gồm Cu: 0,075 mol và Fe dư: 15 – 0,075.56 – 0,125.56 = 3,8 gam
m = 0,075.64 + 3,8 = 8,6 (gam)
Chọn đáp án A.
Câu 36:
Đốt cháy hoàn toàn 14,24 gam hỗn hợp X chứa 2 este đều no, đơn chức, mạch hở thu được CO2 và H2O có tổng khối lượng là 34,72 gam. Mặt khác đun nóng 14,24 gam X với dung dịch NaOH vừa đủ, thu được hỗn hợp Y chứa 2 ancol kế tiếp và hỗn hợp Z chứa 2 muối của 2 axit cacboxylic kế tiếp, trong đó có a gam muối A và b gam muối B (MA < MB). Tỉ lệ gần nhất của a : b là
 Xem đáp án
Xem đáp án
X chứa 2 este đều no, đơn chức, mạch hở thu được CO2 bằng số mol H2O
X chứa este HCOOCH3 (x mol) và CH3COOC2H5 (y mol)
Ta có hệ
Câu 37:
Cho 86,3 gam hỗn hợp X gồm Na, K, B và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết vào nước, thu được dung dịch Y và 13,44 lít khí H2 (đktc). Cho 3,2 lít dung dịch HCl 0,75M vào dung dịch Y. Sau khi các phản ứng xảy ra hoàn toàn, thu được gam kết tủa Z. Nung Z đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Sơ đồ tổng số mol điện tích âm trong dung dịch Y.
sau phản ứng trung hòa bị hòa tan
Công thức tính nhanh:
Câu 38:
Hỗn hợp X gồm một số amino axit (chỉ chứa nhóm chức –COOH và –NH2 trong phân tử), trong đó tỉ lệ . Để tác dụng vừa đủ với 10,36 gam hỗn hợp X cần dùng đủ 120ml dung dịch HCl 1M. Mặt khác cho 10,36 gam hỗn hợp X tác dụng với 250ml dung dịch NaOH 1M rồi cô cạn thu được m gam rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Ta có: số nguyên tử O gấp đôi số nguyên tử N nên X gồm các a.a có 1 nhóm và 1 nhóm (tạo thành)
ta có: mrắn = 10,36 + 0,25.40 – 0,12.18 =18,2 gam.
Chọn đáp án D.
Câu 39:
Cho m gam bột Fe vào bình kín chứa đồng thời 0,06 mol O2 và 0,03 mol Cl2, rồi đốt nóng. Sau khi các phản ứng xảy ra hoàn toàn chỉ thu được hỗn hợp chất rắn chứa các oxit sắt và muối sắt. Hòa tan hết hỗn hợp này trong một lượng dung dịch HCl (lấy dư 25% so với lượng cần phản ứng) thu được dung dịch X. Cho dung dịch AgNO3 dư vào X, sau khi kết thúc các phản ứng thì thu được 53,28 gam kết tủa (biết sản phẩm khử của N+5 là khí NO duy nhất). Giá trị của m là
 Xem đáp án
Xem đáp án
O trong 0,06 mol sẽ chạy hết vào trong H2O
đã dùng (dư 25%) = 1,25.0,24 = 0,3 mol.
Quá trình:
Sơ đồ:
(cả quá trình)
đi vào hết AgCl
Câu 40:
X, Y (MX < MY) là hai peptit mạch hở, hơn kém nhau một liên kết peptit. Đun nóng 36,58 gam hỗn hợp E chứa X, Y và este Z (C5H11O2N) với dung dịch NaOH vừa đủ, chưng cất dung dịch sau phản ứng, thu được 0,05 mol ancol etylic và hỗn hợp chứa 2 muối của 2 -aminoaxit thuộc cùng dãy đồng đẳng. Đốt cháy toàn bộ muối cần dùng 1,59 mol O2, thu được CO2, H2O, N2 và 26,5 gam Na2CO3. Phần trăm khối lượng X trong hỗn hợp E là
 Xem đáp án
Xem đáp án
Thủy phân E gồm 2 peptit và 1 este ancol C2H5OH và các muối của aminoaxit
Z chắc chắn là este của ancol etylic với aminoaxi
Z có mô hình là H2N–R–COOC2H5
R là C2H4 (– CH(CH3) –) Z là este của Ala với ancol etylic: H2N– CH(CH3) – COOC2H5
Đốt muối bằng O2:
Chú ý: nằm hết trong peptit X, Y nhưng nằm trong cả X, Y, Z
Câu 41:
 Xem đáp án
Xem đáp án
(bị khử) = 0,15 mol
Chú ý: Các công thức tính nhanh cho bài toán HNO3 là vũ khí cực kì lợi hại
(số e nhận + số nguyên tử N (trong sản phẩm khử)). nsản phẩm khử
mmuối = mkim loại
Chọn đáp án B.
Câu 42:
X, Y là hai axit cacboxylic đều đơn chức, mạch hở (trong phân tử X, Y chứa không quá 2 liên kết và ); Z là este được tạo bởi X, Y và etylen glicol. Đốt cháy 13,12 gam hỗn hợp E chứa X, Y, Z cần dùng 0,50 mol O2. Mặt khác 0,36 mol E làm mất màu vừa đủ dung dịch chứa 0,1 mol Br2. Nếu đun nóng 13,12 gam E với 200 ml dung dịch KOH 1M (vừa đủ), cô cạn dung dịch sau phản ứng thu được hỗn hợp F gồm a gam muối A và b gam muối B (MA < MB).Tỉ lệ của a : b gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
X không thể là HCOOH
muối ghép chất
Chú ý: khi ghép chất dễ thấy giá trị số mol nhóm CH2 = giá trị số mol nhóm H2, nên ta ghép cùng một nhóm CH2 và bớt 1 nhóm H2 (số mol âm) vào 1 phân tử axit nền CH3COOH, thì ta sẽ được CH2=CH-COOH
Chọn đáp án B.
