Đề thi thử THPT môn Hóa năm 2022 có đáp án (Mới nhất) - Đề 12
-
3460 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Hợp chất nào sau đây có tính lưỡng tính
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Al(OH)3 là hiđroxit lưỡng tính.
Al(OH)3 là hiđroxit lưỡng tính.
Câu 2:
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của P2O5
Độ dinh dưỡng của phân lân được đánh giá bằng hàm lượng % của P2O5
Câu 3:
Chất nào sau đây là amin bậc hai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Đimetylamin (CH3)2NH là amin bậc 2
Đimetylamin (CH3)2NH là amin bậc 2
Câu 4:
Phản ứng xảy ra giữa 2 cặp Fe2+/Fe và Cu2+/Cu là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
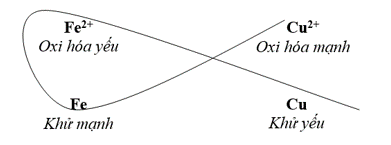
Phương trình: Cu2+ + Fe → Cu + Fe2+.

Phương trình: Cu2+ + Fe → Cu + Fe2+.
Câu 5:
Cho dung dịch Fe(NO3)3 tác dụng với dung dịch NaOH tạo thành kết tủa có màu
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ + 3NaNO3
Fe(OH)3 là kết tủa màu nâu đỏ
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ + 3NaNO3
Fe(OH)3 là kết tủa màu nâu đỏ
Câu 6:
Dung dịch NaOH không phản ứng với chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
2NaOH + SO2 → Na2SO3 + H2O
H2S + 2NaOH → Na2S + 2H2O
2NaOH + CO2 → Na2CO3 + H2O
2NaOH + SO2 → Na2SO3 + H2O
H2S + 2NaOH → Na2S + 2H2O
2NaOH + CO2 → Na2CO3 + H2O
Câu 7:
Để điều chế CO2 trong phòng thí nghiệm người ta cho dung dịch HCl tác dụng với CaCO3 trong bình kíp. Do đó CO2 thu được thường có lẫn một ít hiđroclorua và hơi nước. Có thể dùng hoá chất theo thứ tự nào sau đây để thu được CO2 tinh khiết ?
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Có thể dùng theo thứ tự NaHCO3 (loại HCl) và H2SO4 đặc (loại H2O) để thu được CO2 tinh khiết.
NaHCO3 + HCl → NaCl + CO2 + H2O
Có thể dùng theo thứ tự NaHCO3 (loại HCl) và H2SO4 đặc (loại H2O) để thu được CO2 tinh khiết.
NaHCO3 + HCl → NaCl + CO2 + H2O
Câu 8:
Saccarozơ có nhiều trong mía, củ cải đường, hoa thốt nốt,… Công thức phân tử của saccarozơ là
 Xem đáp án
Xem đáp án
Đáp án đúng là: B
Công thức phân tử của saccarozơ là C12H22O11.
Công thức phân tử của saccarozơ là C12H22O11.
Câu 9:
Một trong những nguyên nhân gây tử vong của nhiều vụ cháy là do nhiễm độc khí X. Khi vào cơ thể, khí X kết hợp với hemoglobin, làm giảm khả năng vận chuyển oxi của máu. Khí X là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Khí X là CO.
Khí X là CO.
Câu 10:
Crom có số oxi hóa +6 trong hợp chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Crom có số oxi hóa +6 trong hợp chất CrO3.
Crom có số oxi hóa +6 trong hợp chất CrO3.
Câu 11:
Xà phòng hóa triolein trong dung dịch NaOH đun nóng, thu được muối có công thức là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
(C17H33COO)3C3H5 + 3NaOH → 3C17H33COONa + C3H5(OH)3
(C17H33COO)3C3H5 + 3NaOH → 3C17H33COONa + C3H5(OH)3
Câu 12:
Chất ứng với công thức cấu tạo nào sau đây là đipeptit?
 Xem đáp án
Xem đáp án
Đáp án đúng là: D
H2NCH(CH3)CONHCH2COOH là đipeptit
H2NCH(CH3)CONHCH2COOH là đipeptit
Câu 15:
Chất X tác dụng với dung dịch NaOH vừa đủ thu được dung dịch chứa hai muối. X là chất nào trong các chất sau:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
HCOOC6H5 + 2NaOH → HCOONa + C6H5ONa + H2O
HCOOC6H5 + 2NaOH → HCOONa + C6H5ONa + H2O
Câu 16:
Trường hợp nào sau đây kim loại bị ăn mòn điện hóa?
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Trường hợp thép cacbon để trong không khí ẩm, kim loại bị ăn mòn điện hóa
Trường hợp thép cacbon để trong không khí ẩm, kim loại bị ăn mòn điện hóa
Câu 17:
Hiện tượng xảy ra khi nhỏ vài giọt dung dịch H2SO4 vào dung dịch Na2CrO4 là:
 Xem đáp án
Xem đáp án
Đáp án đúng là C
Hiện tượng xảy ra là dung dịch chuyển từ màu vàng sang màu da cam.
Hiện tượng xảy ra là dung dịch chuyển từ màu vàng sang màu da cam.
Câu 18:
Tổng số chất hữu cơ mạch hở, đơn chức có cùng công thức phân tử C2H4O2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
HCOOCH3
CH3COOH
HCOOCH3
CH3COOH
Câu 19:
Thủy phân hoàn toàn este X có công thức cấu tạo CH3-COO-CH2-CH2-OOC-C2H5 trong dung dịch NaOH đun nóng, sản phẩm hữu cơ thu được gồm
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
CH3COOCH2CH2OOCC2H5 + 2NaOH → CH3COONa + C2H5COONa + HOCH2CH2OH
CH3COOCH2CH2OOCC2H5 + 2NaOH → CH3COONa + C2H5COONa + HOCH2CH2OH
Câu 20:
Khi làm thí nghiệm với dung dịch HNO3 đặc thường sinh ra khí nitơ đioxit gây ô nhiễm không khí. Công thức của nitơ đioxit là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Công thức của nitơ đioxit là NO2.
Công thức của nitơ đioxit là NO2.
Câu 22:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
C sai, vì Na không khử được ion Cu2+
2Na + 2H2O → 2NaOH + H2
Cu2+ + 2OH- → Cu(OH)2↓
C sai, vì Na không khử được ion Cu2+
2Na + 2H2O → 2NaOH + H2
Cu2+ + 2OH- → Cu(OH)2↓
Câu 24:
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
X, Y, Z, T lần lượt là
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X, Y |
Cu(OH)2 |
Dung dịch xanh lam |
|
Y |
AgNO3/NH3, t° |
Kết tủa Ag trắng sáng |
|
Z |
Dung dịch Br2 |
Kết tủa trắng |
|
T |
Quỳ tím |
Chuyển màu xanh |
X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Vì X, Y phản ứng với Cu(OH)2 sinh ra dung dịch màu xanh lam → chọn đáp án C
Vì X, Y phản ứng với Cu(OH)2 sinh ra dung dịch màu xanh lam → chọn đáp án C
Câu 28:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch BaCl2 vào dung dịch KHSO4.
(b) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(c) Cho dung dịch NH3 tới dư vào dung dịch Fe(NO3)3.
(d) Cho dung dịch NaOH tới dư vào dung dịch AlCl3.
(e) Cho kim loại Cu vào dịch FeCl3 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kết tủa là
(a) Cho dung dịch BaCl2 vào dung dịch KHSO4.
(b) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(c) Cho dung dịch NH3 tới dư vào dung dịch Fe(NO3)3.
(d) Cho dung dịch NaOH tới dư vào dung dịch AlCl3.
(e) Cho kim loại Cu vào dịch FeCl3 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án đúng là: C
Các thí nghiệm thu được kết tủa là: (a), (b), (c).
Các thí nghiệm thu được kết tủa là: (a), (b), (c).
Câu 29:
Cho dãy các chất: Fe2O3, FeS, Fe(OH)2, Fe3O4, FeCO3, Fe(OH)3. Số chất trong dãy tác dụng với H2SO4 đặc, nóng, dư không tạo khí SO2 là
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Chất tác dụng với H2SO4 đặc, nóng, dư không tạo khí SO2 là: Fe2O3, Fe(OH)3
Chất tác dụng với H2SO4 đặc, nóng, dư không tạo khí SO2 là: Fe2O3, Fe(OH)3
Câu 30:
Cho các phát biểu sau:
(a) Mỡ lợn hoặc dầu dừa có thể dùng làm nguyên liệu sản xuất xà phòng.
(b) Nước ép của quả nho chín có khả năng tham gia phản ứng tráng bạc.
(c) Trong tơ tằm có các gốc α-amino axit.
(d) Cao su lưu hóa có tính đàn hồi, lâu mòn và khó tan hơn cao su thường.
(e) Một số este có mùi thơm được dùng làm chất tạo hương cho thực phẩm và mỹ phẩm.
Số phát biểu đúng là:
(a) Mỡ lợn hoặc dầu dừa có thể dùng làm nguyên liệu sản xuất xà phòng.
(b) Nước ép của quả nho chín có khả năng tham gia phản ứng tráng bạc.
(c) Trong tơ tằm có các gốc α-amino axit.
(d) Cao su lưu hóa có tính đàn hồi, lâu mòn và khó tan hơn cao su thường.
(e) Một số este có mùi thơm được dùng làm chất tạo hương cho thực phẩm và mỹ phẩm.
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
Đáp án đúng là: A
Các phát biểu đúng là: (a), (b), (c), (d), (e).
Các phát biểu đúng là: (a), (b), (c), (d), (e).