Bộ đề thi môn Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi môn Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) (Đề số 4)
-
26370 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Đốt cháy 1 mol este C4H8O2 thì thu được khối lượng nước là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Bảo toàn nguyên tố H.
Giải chi tiết:
Bảo toàn nguyên tố H:
C4H8O2 H2O
1 mol → 4 mol
⟹ mH2O = 4.18 = 72 gam.
Câu 2:
Anđehit được điều chế bằng phản ứng oxi hóa ancol nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Lý thuyết về phản ứng oxi hóa ancol.
Giải chi tiết:
Phản ứng oxi hóa ancol:
+ Ancol bậc 1 tạo anđehit.
+ Ancol bậc 2 tạo xeton.
+ Ancol bậc 3 không bị oxi hóa.
Câu 3:
Công thức phân tử của fructozơ là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Lý thuyết về fructozơ.
Giải chi tiết:
Công thức phân tử của fructozơ là C6H12O6.
Câu 4:
Axit axetic CH3COOH không phản ứng với chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Tính chất hóa học của axit cacboxylic.
Giải chi tiết:
CH3COOH không phản ứng với NaCl.
PTHH:
CH3COOH + NaOH → CH3COONa + H2O
2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O
2CH3COOH + 2Na → 2CH3COONa + H2
Câu 5:
Chất X là một khí rất độc, có trong thành phần của khí than. Chất X là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Giải chi tiết:
Khí độc có trong thành phần của khí than là CO.
Câu 6:
Chất béo nào sau đây ở dạng lỏng trong điều kiện thường?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Chất béo không no có trạng thái lỏng trong điều kiện thường.
Giải chi tiết:
Chất béo không no có trạng thái lỏng trong điều kiện thường.
⟹ (C17H33COO)3C3H5
Câu 7:
Etyl butirat là tên của este có công thức nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Từ tên gọi suy ra CTHH.
Giải chi tiết:
Etyl butirat là CH3CH2CH2COOCH2CH3.
Câu 8:
Tripanmitin có công thức cấu tạo là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về chất béo.
Giải chi tiết:
Tripanmitin có công thức cấu tạo là (C15H31COO)3C3H5 hay C3H5(OCOC15H31)3.
Câu 9:
Cacbohiđrat nào sau đây có tính khử?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Chất khử là chất nhường e (có số oxi hóa tăng).
Giải chi tiết:
Trong 4 cacbohiđrat trên, glucozơ có tính khử.
Câu 10:
Ancol X hòa tan Cu(OH)2 thành dung dịch màu xanh lam. X là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Ancol hòa tan Cu(OH)2 thành dung dịch màu xanh lam là ancol đa chức có nhiều nhóm OH gắn vào các nguyên tử C cạnh nhau.
Giải chi tiết:
Ancol X hòa tan Cu(OH)2 thành dung dịch màu xanh lam nên X là ancol đa chức có nhiều nhóm OH gắn vào các nguyên tử C cạnh nhau.
⟹ X là C3H5(OH)3.
Câu 11:
Chất nào sau đây không phải este?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Khi thay nhóm -OH của axit cacboxylic bằng nhóm -OR' ta được este.
Giải chi tiết:
HOOCCH3 viết lại là CH3COOH, là một axit cacboxylic, không phải este.
Câu 12:
Chất nào sau đây có 1 liên kết pi (π) trong phân tử?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Liên kết đôi (C=C) = 1π + 1σ
Liên kết ba (C≡C) = 2π + 1σ
Giải chi tiết:
- CH2=CH2 ⟹ có 1π
- ⟹ có 3π
- CH≡CH ⟹ có 2π
- CH4 ⟹ không có liên kết π
Câu 13:
Khi có 1 mol anđehit nào sau đây tham gia phản ứng tráng bạc tạo thành 4 mol Ag?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Lý thuyết về anđehit.
Giải chi tiết:
1 mol anđehit fomic (HCHO) tham gia tráng bạc sinh ra 4 mol Ag.
PTHH: HCHO + 4AgNO3 + 6NH3 + 2H2O (NH4)2CO3 + 4Ag + 4NH4NO3
Câu 14:
Mệnh đề nào sau đây sai khi nói về este?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về este.
Giải chi tiết:
- và B đúng, do este không tạo được liên kết H với nước. C. đúng. D. sai, este của phenol không được điều chế trực tiếp từ axit và phenol mà phải điều chế từ phenol và anhiđrit của axit.
PTHH: (CH3CO)2O + C6H5OH CH3COOC6H5 + CH3COOH
Câu 15:
Cacbohiđrat X có các tính chất sau:
|
Tính chất |
Hòa tan Cu(OH)2 ở nhiệt độ thường |
Tác dụng với dung dịch AgNO3/NH3 |
Tác dụng với dung dịch brom |
Lên men khi có enzim xúc tác |
|
Hiện tượng |
Tạo dung dịch màu xanh lam |
Tạo kết tủa trắng bạc |
Làm mất màu dung dịch brom |
Có khí thoát ra làm đục nước vôi trong |
X là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về cacbohiđrat.
Giải chi tiết:
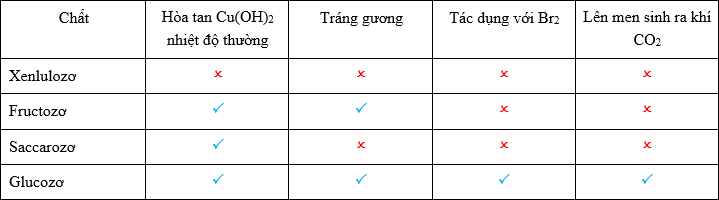
Vậy X là glucozơ.
Câu 16:
Chọn mệnh đề sai về cacbohiđrat?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về cacbohiđrat.
Giải chi tiết: D. sai, vì saccarozơ là một đisaccarit chứ không phải polisaccarit.
Câu 17:
Phản ứng nào sau đây không được dùng để điều chế CH3COOH?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Lý thuyết về phản ứng điều chế axit cacboxylic.
Giải chi tiết:
A: C2H5OH + O2 CH3COOH + H2O.
B: CH4 + O2 HCHO + H2O.
C: CH3OH + CO CH3COOH.
D: 2CH3CHO + O2 2CH3COOH.
Câu 18:
Chất nào sau đây làm mất màu dung dịch brom?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Hiđrocacbon làm mất màu dung dịch Br2 chứa liên kết bội kém bền hoặc xicloankan có vòng 3 cạnh, …
Giải chi tiết:
But-1-en có CTCT là CH2=CH-CH2-CH3 có chứa liên kết C=C kém bền nên làm mất màu dung dịch Br2.
PTHH: CH2=CH-CH2-CH3 + Br2 → CH2Br-CHBr-CH2-CH3.
Câu 19:
Ure là một loại phân bón hóa học được sử dụng rộng rãi trong nông nghiệp. Ure thuộc loại phân bón hóa học nào?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Giải chi tiết:
Ure có công thức (NH2)2CO, khi hòa tan vào nước sinh ra (NH4)2CO3 cung cấp N dưới dạng ion NH4+
⟹ Ure là một loại phân đạm.
PTHH: (NH2)2CO + 2H2O → (NH4)2CO3
Câu 20:
Thủy phân este C4H6O2 trong môi trường axit thu được hỗn hợp gồm 2 chất hữu cơ đều có khả năng tráng gương. Công thức cấu tạo của este đó là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Thủy phân este thu được 2 chất đều tráng gương ⟹ Este có dạng HCOOCH=CH-R' (R' là H hoặc gốc hiđrocacbon).
Giải chi tiết:
Thủy phân este thu được 2 chất đều tráng gương ⟹ Este có dạng HCOOCH=CH-R' (R' là H hoặc gốc hiđrocacbon).
⟹ Chất thỏa mãn là HCOOCH=CH-CH3.
PTHH: HCOOCH=CH-CH3 + H2O HCOOH + CH3-CH2-CHO.
Câu 21:
Một este no, đơn chức, mạch hở có 48,65% cacbon về khối lượng trong phân tử thì số đồng phân este là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Este no, đơn chức, mạch hở có dạng CnH2nO2 (n ≥ 2).
Từ phần trăm khối lượng C suy ra giá trị của n ⟹ CTPT.
Từ CTPT viết các đồng phân este.
Giải chi tiết:
Đặt công thức este là CnH2nO2 (n ≥ 2).
Ta có:
⟹ CTPT este là C3H6O2.
Có 2 đồng phân este có CTPT C3H6O2 là:
HCOOCH2CH3
CH3COOCH3.
Câu 22:
Tính chất nào sau đây không phải của triolein?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về chất béo.
Giải chi tiết:
Triolein không có phản ứng este hóa (Lưu ý: Phản ứng este hóa là phản ứng điều chế este).
Câu 23:
Mệnh đề nào sau đây đúng khi nói về chất béo?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Lý thuyết về chất béo.
Giải chi tiết:
- đúng.
- sai, trong công nghiệp chất béo được dùng để sản xuất xà phòng và glixerol.
- sai, dầu mỡ bị ôi là do phản ứng oxi hóa ở liên kết C=C.
- sai, dầu ăn là các chất béo chứa C, H, O (ngoài ra còn có tạp chất); còn dầu hỏa là các hiđrocacbon có thành phần C, H.
Câu 24:
Cho phản ứng hóa học: CaCO3 (r) + 2HCl → CaCl2 + CO2↑ + H2O.
Phương trình ion thu gọn của phản ứng trên là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Cách chuyển đổi các phương trình phân tử sang phương trình ion rút gọn:
+ Chuyển tất cả các chất vừa dễ tan, vừa điện li mạnh thành ion, các chất khí, kết tủa, điện li yếu để nguyên dưới dạng phân tử thu được phương trình ion đầy đủ.
+ Lược bỏ những ion không tham gia phản ứng ta được phương trình ion rút gọn.
Giải chi tiết:
PT ion thu gọn của phản ứng trên là: CaCO3 (r) + 2H+ → Ca2+ + CO2↑ + H2O.
Câu 25:
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 4,83 mol O2, thu được 3,42 mol CO2 và 3,18 mol H2O. Mặt khác, cho a gam X phản ứng vừa đủ với dung dịch brom. Khối lượng Br2 đã phản ứng là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
- Bảo toàn nguyên tố O tính được số mol của chất béo.
- Khi đốt cháy chất béo ta có công thức tính nhanh:
(với k là số liên kết π trong toàn phân tử).
Từ đó xác định được k.
- Khi chất béo tác dụng với dung dịch Br2:
CB + (k-3) Br2 → Sản phẩm cộng
Giải chi tiết:
- Khi đốt cháy chất béo:
+) BTNT O → 6nCB + 2nO2 = 2nCO2 + nH2O
+) Ta có công thức tính nhanh: (với k là số liên kết π trong toàn phân tử).
⟹ ⟹ k = 5.
Chất béo chứa 3 π trong 3 gốc COO nên còn lại 2 π ở ngoài gốc hiđrocacbon.
- Khi X tác dụng với Br2 thì chỉ có 2 π ngoài gốc hiđrocacbon tác dụng:
X + 2Br2 → Sản phẩm
0,06 → 0,12 mol
⟹ mBr2 = 0,12.160 = 19,2 gam.
Câu 26:
Đốt cháy hoàn toàn 7,4 gam hỗn hợp hai este đồng phân, thu được 6,72 lít CO2 (đktc) và 5,4 gam H2O. CTPT của hai este là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Ta thấy nCO2 = nH2O ⟹ 2 este no, đơn chức, mạch hở.
Giả sử 2 este có cùng CTPT là CnH2nO2.
Áp dụng bảo toàn nguyên tố C ⟹ ⟹ giá trị của n ⟹ CTPT.
Giải chi tiết:
Ta thấy nCO2 = nH2O = 0,3 mol ⟹ 2 este no, đơn chức, mạch hở.
Giả sử 2 este có cùng CTPT là CnH2nO2.
⟹ CTPT của 2 este là C3H6O2.
Câu 27:
Cho khí CO qua ống chứa 15,2 gam hỗn hợp (A) gồm CuO và FeO nung nóng. Sau một thời gian thu được hỗn hợp khí (B) và 13,6 gam chất rắn (C). Cho B tác dụng với dung dịch Ca(OH)2 dư thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Khối lượng chất rắn giảm chính là khối lượng O phản ứng ⟹ nO(pư).
Phản ứng khử oxit kim loại bằng CO có thể viết là: CO + O → CO2 ⟹ nCO2.
Khi cho khí tác dụng với Ca(OH)2 dư: CO2 + Ca(OH)2 → CaCO3 ↓ + H2O ⟹ nCaCO3 ⟹ m ↓.
Giải chi tiết:
mO(pư) = mchất rắn giảm = 15,2 - 13,6 = 1,6 gam
→ nO(pư) = 1,6 : 16 = 0,1 mol
Phản ứng khử oxit kim loại bằng CO có thể viết là:
CO + O → CO2
0,1 → 0,1 (mol)
Khi cho khí tác dụng với Ca(OH)2 dư:
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
0,1 → 0,1 (mol)
→ m = mCaCO3 = 0,1.100 = 10 gam.
Câu 28:
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch NaI vào dung dịch AgNO3;
(b) Sục khí Cl2 vào dung dịch FeCl2;
(c) Dẫn khí CO dư qua bột CuO nung nóng;
(d) Nhiệt phân AgNO3;
(e) Đốt FeS2 trong không khí.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Giải chi tiết:
(a) NaI + AgNO3 → NaNO3 + AgI ↓
(b) Cl2 + 2FeCl2 → 2FeCl3
(c) CO dư + CuO Cu + CO2
(d) 2AgNO3 2Ag + 2NO2 + O2
(e) 4FeS2 + 11O2 2Fe2O3 + 8SO2
Vậy có 2 thí nghiệm thu được kim loại là (c), (d).
Câu 29:
Đốt cháy hoàn toàn m gam hỗn hợp gồm xenlulozơ, tinh bột, glucozơ và saccarozơ cần 2,52 lít khí O2 (đktc), thu được 1,8 gam nước. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Khi đốt cacbohiđrat luôn có nCO2 = nO2(pư) (HS tự chứng minh bằng cách viết PTHH).
Giải chi tiết:
Khi đốt cacbohiđrat luôn có nCO2 = nO2(pư) = 2,52/22,4 = 0,1125 mol.
BTKL: m = mCO2 + mH2O - mO2 = 0,1125.44 + 1,8 - 0,1125.32 = 3,15 gam.
Câu 30:
Cho 5,1 gam Y tác dụng với dung dịch NaOH dư, thu được 4,80 gam muối và 1 ancol. Công thức cấu tạo của Y là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Giải chi tiết:
Quan sát thấy các este đều no, đơn chức, mạch hở.
RCOOR' → RCOONa
Ta thấy meste > mmuối ⟹ R' > 23 ⟹ R' là -C2H5 (quan sát 4 đáp án A, B, C, D).
RCOOC2H5 → RCOONa
Ta có: neste = nmuối ⟹
Vậy este có công thức là C2H5COOC2H5.
Câu 31:
Đun nóng 37,5 gam dung dịch glucozơ với lượng AgNO3/dung dịch NH3 dư, thu được 6,48 gam bạc. Nồng độ % của dung dịch glucozơ là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Glucozơ 2Ag
Từ số mol Ag ⟹ số mol glucozơ ⟹ khối lượng glucozơ.
Tính C% dung dịch glucozơ:
Giải chi tiết:
Glucozơ 2Ag
→ nGlu = ½ nAg = ½.6,48/108 = 0,03 mol
→ mGlu = 0,03.180 = 5,4 gam
→ C%dd glucozơ = (5,4/37,5).100% = 14,4%.
Câu 32:
Cho các mệnh đề sau:
(1) Công thức phân tử của tristearin là C54H110O6.
(2) Polime thiên nhiên khi I2 hấp phụ tạo thành màu xanh tím là tinh bột.
(3) Fructozơ được gọi là đường nho.
(4) Thủy phân hoàn toàn chất béo luôn thu được glixerol.
(5) Xenlulozơ và tinh bột là đồng phân của nhau.
(6) Xenlulozơ trinitrat được dùng làm thuốc súng không khói.
Số mệnh đề đúng là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết tổng hợp về este, cacbohiđrat.
Giải chi tiết:
(1) sai, tristearin là (C17H35COO)3C3H5 có CTPT là C57H110O6.
(2) đúng.
(3) sai, glucozơ được gọi là đường nho.
(4) đúng.
(5) sai.
(6) đúng.
Vậy có 3 mệnh đề đúng.
Câu 33:
Hỗn hợp khí X gồm 0,3 mol H2 và 0,1 mol vinyl axetilen. Nung X một thời gian với xúc tác Ni thu được hỗn hợp Y có tỉ khối so với không khí là 1. Dẫn hỗn hợp Y qua dung dịch brom dư, phản ứng hoàn toàn. Tính khối lượng brom đã phản ứng?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Tính được MY = 29 g/mol; vinyl axetilen là CH≡C-CH=CH2 có chứa 3 π.
BTKL: mX = mY ⟹ nY.
Tính được nH2(pư) = ngiảm = nX - nY.
Bảo toàn liên kết π: n π (bđ) = n π (bị phá bởi H2) + n π (bị phá bởi Br2) ⟹ 3nC2H2(bđ) = nH2(pư) + nBr2 ⟹ nBr2.
Giải chi tiết:
Ta có: MY = 29 g/mol; vinyl axetilen là CH≡C-CH=CH2 có chứa 3 π.
BTKL: mX = mY ⟹ 0,3.2 + 0,1.52 = nY.29 ⟹ nY = 0,2 mol.
nH2(pư) = ngiảm = 0,3 + 0,1 - 0,2 = 0,2 mol.
Bảo toàn liên kết π: n π (bđ) = n π (bị phá bởi H2) + n π (bị phá bởi Br2)
⟹ 3nC2H2(bđ) = nH2(pư) + nBr2
⟹ 3.0,1 = 0,2 + nBr2
⟹ nBr2 = 0,1 mol.
⟹ mBr2 = 16 gam.
Câu 34:
Cho 6 gam một ancol đơn chức mạch hở tác dụng Na vừa đủ thu được 1,12 lít khí H2 (đkc). Số CTCT của X là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
ROH + Na → RONa + ½ H2
⟹ nancol = 2nH2 ⟹ Mancol ⟹ CTPT ⟹ Các CTCT.
Giải chi tiết:
nH2 = 0,05 mol
ROH + Na → RONa + ½ H2
0,1 ← 0,05 (mol)
⟹ Mancol = 6 : 0,1 = 60 g/mol
⟹ R + 17 = 60
⟹ R = 43 (-C3H7)
Các công thức cấu tạo thỏa mãn là:
CH3-CH2-CH2-OH
CH3-CH(OH)-CH3
Câu 35:
Xà phòng hóa hoàn toàn 17,24 gam chất béo cần vừa đủ 0,06 mol NaOH. Cô cạn dung dịch sau phản ứng thu được khối lượng xà phòng là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Phản ứng xà phòng hóa chất béo: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Vậy trong phản ứng xà phòng hóa chất béo ta luôn có: nglixerol = 1/3.nNaOH.
BTKL: mmuối = mchất béo + mNaOH - mglixerol.
Giải chi tiết:
Phản ứng xà phòng hóa chất béo: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Vậy trong phản ứng xà phòng hóa chất béo ta luôn có: nglixerol = 1/3.nNaOH = 0,02 mol.
BTKL: mmuối = mchất béo + mNaOH - mglixerol = 17,24 + 0,06.40 - 0,02.92 = 17,8 gam.
Câu 36:
Thực hiện phản ứng este hóa giữa 4,6 gam ancol etylic với lượng dư axit axetic, thu được 4,4 gam este. Hiệu suất phản ứng este hóa là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Tính số mol C2H5OH ban đầu.
Tính số mol C2H5OH phản ứng dựa vào PTHH.
Tính hiệu suất phản ứng:
Giải chi tiết:
CH3COOH + C2H5OH CH3COOC2H5 + H2O
nC2H5OH(bđ) = 4,6/46 = 0,1 mol.
nC2H5OH(pư) = nCH3COOC2H5 = 4,4/88 = 0,05 mol.
Câu 37:
Đốt cháy hoàn toàn 10,58 gam hỗn hợp X chứa ba este đều đơn chức, mạch hở bằng lượng oxi vừa đủ, thu được 8,96 lít khí CO2 (đktc). Mặt khác, hiđro hóa hoàn toàn 10,58 gam X cần dùng 0,07 mol H2 (xúc tác, to), thu được hỗn hợp Y. Đun nóng toàn bộ Y với 250 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được một ancol Z duy nhất và m gam rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Sử dụng phương pháp ankan hóa.
Giải chi tiết:
Sử dụng phương pháp ankan hóa X thành các este no Y:
+) mY = mX + mH2 = 10,58 + 0,07.2 = 10,72 (g).
+) Khi đốt Y:
nCO2(đốt Y) = nCO2(đốt X) = 0,4 mol = nH2O(đốt Y) (do Y là các este no, đơn chức).
+) Khi đốt X:
nC(X) = nCO2(đốt Y) = 0,4 mol
nH2O(đốt X) = nH2O(đốt Y) - nH2 = 0,4 - 0,07 = 0,33 mol → nH(X) = 0,66 mol.
BTKL: nO(X) = (10,58 - 0,4.12 - 0,66)/16 = 0,32 mol
→ nX = ½ nO = 0,16 mol (do các este đều đơn chức)
→ Số C trung bình = 0,4 : 0,16 = 2,5
→ Có 1 este là HCOOCH3
→ Ancol Z là CH3OH; nCH3OH = nX = 0,16 mol
+) Khi cho Y + dd NaOH:
BTKL: mchất rắn = mY + mNaOH - mCH3OH = 10,72 + 0,25.40 - 0,16.32 = 15,6 gam.
Câu 38:
Cho m gam hỗn X gồm Fe và Al tan hoàn toàn trong 1,2 lít dung dịch HCl 1M (dư), thu được dung dịch Y và thoát ra 10,752 lít H2 (đktc). Mặt khác cho m gam hỗn hợp X vào dung dịch H2SO4 đặc nóng, dư, khi phản ứng xảy ra hoàn toàn, thu được 14,112 lít SO2 (đktc, sản phẩm khử duy nhất của S+6). Thêm 0,1 mol NaNO3 vào dung dịch Y, khi phản ứng xảy ra hoàn toàn thu được dung dịch Z và thoát ra V lít khí NO (đktc, sản phẩm khử duy nhất của N+5). Khối lượng muối có trong Z là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
*TN1: Fe và Al phản ứng với HCl dư tạo Fe2+ và Al3+:
Bảo toàn e ta có: 2nFe + 3nAl = 2nH2 (1)
*TN2: Fe và Al phản ứng với H2SO4 đặc nóng dư tạo Fe3+ và Al3+:
Bảo toàn e ta có: 3nFe + 3nAl = 2nSO2 (2)
Từ (1) và (2) suy ra nFe và nAl.
Xác định thành phần của dd Y.
Khi cho NaNO3 vào Y: 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
Tính theo PT ion xác định được thành phần dung dịch Z.
Giải chi tiết:
*TN1: Fe và Al phản ứng với HCl dư tạo Fe2+ và Al3+ sinh ra nH2 = 0,48 mol
Bảo toàn e ta có: 2nFe + 3nAl = 2nH2 = 0,96 (1)
nHCl pư = 2nH2 = 0,96 mol ⟹ nHCl dư = 1,2 - 0,96 = 0,24 mol
*TN2: Fe và Al phản ứng với H2SO4 đặc nóng dư tạo Fe3+ và Al3+ thu được nSO2 = 0,63 mol
Bảo toàn e ta có: 3nFe + 3nAl = 2nSO2 = 1,26 (2)
Từ (1) và (2) suy ra nFe = 0,3 và nAl = 0,12
Vậy Y gồm: Fe2+ (0,3 mol); Al3+ (0,12 mol); H+ (0,24); Cl- (1,2)
Khi cho 0,1 mol NaNO3 vào Y:
3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O
0,18 ← 0,24 → 0,06 → 0,18
Vậy Z gồm:
Fe3+: 0,18 mol
Fe2+: 0,3 - 0,18 = 0,12 mol
Al3+: 0,12 mol
Na+: 0,1
Cl-: 1,2 mol
NO3-: 0,1 - 0,06 = 0,04 mol
⟹ m muối = ∑m ion = 67,42 gam
Câu 39:
Hỗn hợp X gồm một este, một axit cacboxylic và một ancol (đều no, đơn chức, mạch hở). Thủy phân hoàn toàn 6,18 gam X bằng lượng vừa đủ dung dịch chứa 0,1 mol NaOH thu được 3,2 gam một ancol. Cô cạn dung dịch sau thủy phân rồi đem lượng muối khan thu được đốt cháy hoàn toàn thu được 0,05 mol H2O. Hỏi phần trăm khối lượng của este trong X là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Bảo toàn nguyên tố, bảo toàn khối lượng
Giải chi tiết:
nmuối = nNaOH = 0,1 mol
⟹ Số H trong muối = 2nH2O : n muối = 2.0,05 : 0,1 = 1
⟹ Muối chỉ chứa HCOONa
BTKL: mX + mNaOH = mHCOONa + m ancol + mH2O
⟹ 6,18 + 0,1.40 = 0,1.68 + 3,2 + mH2O
⟹ mH2O = 0,18 gam ⟹ nH2O = 0,01 mol
Mà n axit = nH2O ⟹ n este = nHCOONa - naxit = 0,1 - 0,01 = 0,09 mol
Ta có n ancol > n este = 0,09 ⟹ M ancol < 3,2 : 0,09 = 35,55 ⟹ ancol là CH3OH
⟹ Este là HCOOCH3
mHCOOCH3 = 0,09.60 = 5,4 gam
⟹ %m este = (5,4 : 6,18). 100% = 87,38%.
Câu 40:
Chất hữu cơ Z có công thức phân tử C17H16O4, không làm mất màu dung dịch brom, Z tác dụng với NaOH theo phương trình hóa học: Z + 2NaOH → 2X + Y; trong đó Y hòa tan Cu(OH)2 tạo thành dung dịch màu xanh lam. Phát biểu nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Ta có Z + 2NaOH → 2X + Y ⟹ Z là este 2 chức tạo bởi 1 axit đơn chức và ancol hai chức (1)
Z không làm mất màu dung dịch nên không chứa liên kết π kém bền hoặc nhóm chức anđehit (2)
CTPT của Z (3)
Từ (1) (2) (3) ⟹ CTCT của X, Y, Z.
Giải chi tiết:
Ta có Z + 2NaOH → 2X + Y ⟹ Z là este 2 chức tạo bởi 1 axit đơn chức và ancol hai chức (1)
Z không làm mất màu dung dịch nên không chứa liên kết π kém bền hoặc nhóm chức anđehit (2)
Mà theo đề bài Z có CTPT C17H16O4 (3)
Từ (1) (2) (3) ⟹ CTCT của Z chỉ có thể là C6H5COO-CH(CH3)-CH2-OOCC6H5.
⟹ X: C6H5COONa; Y: CH3-CH(OH)-CH2OH.
- A đúng, vì X có CTPT C7H5O2Na có .
- B sai, Y có thể được tạo từ CH2=CH-CH3 bằng 1 phản ứng:
CH2=CH-CH3 + H2O CH3-CH(OH)-CH (spc)
- C sai, chỉ có 1 đồng phân thỏa mãn Z.
- D sai, vì:
CH3-CH(OH)-CH2OH + Na → CH3-CH(ONa)-CH2ONa + H2
→ nH2 = nY = 15,2/76 = 0,2 mol
→ VH2 = 4,48 lít.
