Bộ đề thi môn Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi môn Hóa học THPT Quốc gia năm 2022 có lời giải (30 đề) (Đề số 12)
-
26368 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Chất nào sau đây có nhiệt độ sôi cao nhất?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Nhiệt độ sôi theo chiều giảm dần các chất là axit > ancol > este (cùng loại hợp chất, chất nào có phân tử khối lớn hơn sẽ có nhiệt độ sôi cao hơn).
Giải chi tiết:
Sắp xếp các chất theo chiều nhiệt độ sôi giảm dần là CH3COOH > HCOOH > C2H5OH > HCOOCH3.
Vậy chất có nhiệt độ sôi cao nhất là CH3COOH.
Câu 2:
Cho thí nghiệm như hình vẽ:
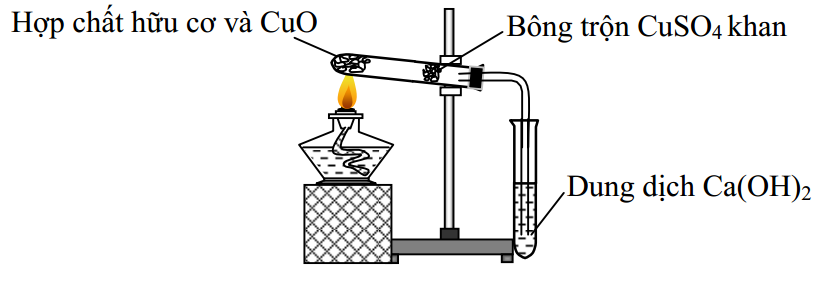
Cho biết CuSO4 khan có vai trò định tính nguyên tố nào?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Dựa vào phương pháp phân tích định tính hợp chất hữu cơ.
Giải chi tiết:
CuSO4 khan có vai trò định tính nguyên tố H.
Hợp chất hữu cơ → CO2 + H2O
Bông trộn CuSO4 khan gặp H2O: chất rắn chuyển từ màu trắng → màu xanh (CuSO4.5H2O).
Câu 3:
Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất X, Y, Z, T ở dạng dung dịch (hoặc chất lỏng):
|
Chất Thuốc thử |
X |
Y |
Z |
T |
|
Quỳ tím |
Xanh |
Tím |
Tím |
Đỏ |
|
Dung dịch Br2 |
Không hiện tượng |
Kết tủa trắng |
Mất màu |
Không hiện tượng |
Chất X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào tính chất hóa học của các hợp chất X, Y, Z, T và kết hợp đáp án ⟹ Hợp chất X, Y, Z, T.
Giải chi tiết:
Chất X, Y, Z, T lần lượt là metyl amin, anilin, glucozơ, axit glutamic.
* Quỳ tím:
- metyl amin làm quỳ tím hóa xanh do mang tính bazơ.
- axit glutamic làm quỳ tím hóa đỏ do mang tính axit.
- anilin và glucozơ không làm quỳ tím đổi màu.
* Dung dịch Br2.
- Anilin tạo kết tủa trắng.
C6H5NH2 + 3Br2 → C6H2(Br3)NH2 ↓trắng + 3HBr.
- Glucozơ làm mất màu dung dịch brom.
HOCH2[CHOH]4CHO + 2AgNO3 + 3NH3 + H2O HOCH2[CHOH]4COONH4 + 2Ag ↓ + 2NH4NO3.
Câu 4:
Chất nào sau đây có tính lưỡng tính?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Hợp chất mang tính lưỡng tính: vừa mang tính axit, vừa mang tính bazơ.
Giải chi tiết:
H2NCH2COOH vừa mang tính axit (-COOH), vừa mang tính bazơ (-NH2) là chất có tính lưỡng tính.
Câu 5:
Cho các phát biểu sau:
(a) Có thể dùng giấm ăn để giảm mùi tanh của cá.
(b) Thủy phân hoàn toàn các triglixerit đều thu được glixerol.
(c) Cao su lưu hóa có tính đàn hồi tốt hơn cao su chưa lưu hóa.
(d) Khi nấu canh cua, riêu cua nổi lên trên là hiện tượng đông tụ protein.
(e) Vải làm từ tơ nilon-6,6 kém bền trong nước xà phòng có tính kiềm.
(g) Muối mononatri glutamat được sử dụng làm mì chính (bột ngọt).
Số nhận xét đúng là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào kiến thức tổng hợp về các hợp chất thuộc chương 2,3,4 (Hóa 12).
Giải chi tiết:
(a) đúng vì giấm ăn mang tính axit, mùi tanh của cá là do các amin (mang tính bazơ).
(b) đúng vì triglixerit là este của glixerol và axit béo.
(c) đúng.
(d) đúng.
(e) đúng vì vải làm từ nilon - 6,6 có nhóm CONH kém bền trong môi trường kiềm.
(g) đúng.
Câu 6:
Cho m gam alanin phản ứng vừa đủ với dung dịch NaOH thu được dung dịch chứa 27,75 gam muối tan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
PTHH: H2N – CH(CH3) – COOH + NaOH → H2N – CH(CH3) – COONa + H2O.
Dựa vào PTHH ⟹ nalanin ⟹ m.
Giải chi tiết:
nmuối = 27,75/111 = 0,25 (mol).
PTHH: H2N – CH(CH3) – COOH + NaOH → H2N – CH(CH3) – COONa + H2O.
Theo PTHH ⟹ nalanin = nmuối = 0,25 (mol).
Vậy m = 0,25.89 = 22,25 gam.
Câu 7:
Đốt cháy hoàn toàn 0,15 mol este mạch hở, no, đơn chức thu được CO2 và H2O có tổng khối lượng là 27,9 gam. Công thức phân tử của X là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Este no, đơn chức, mạch hở khi đốt cháy ⟹ nCO2 = nH2O.
Dựa vào tổng khối lượng CO2 và H2O ⟹ nCO2.
Gọi CTPT của este là CnH2nO2 (n ≥ 2)
Bảo toàn nguyên tố C ⟹ n ⟹ CTPT của X.
Giải chi tiết:
Este no, đơn chức, mạch hở khi đốt cháy ⟹ nCO2 = nH2O.
Ta có mCO2 + mH2O = 27,9 ⟹ 44.nCO2 + 18.nCO2 = 27,9 ⟹ nCO2 = 0,45 (mol).
Gọi CTPT của este là CnH2nO2 (n ≥ 2) có số mol 0,15 (mol).
Bảo toàn nguyên tố C ⟹ 0,15n = 0,45 ⟹ n = 3.
Vậy CTPT của este là C3H6O2.
Câu 8:
Khi bị ốm, mất sức, nhiều người bệnh thường được truyền dịch đường để bổ sung nhanh năng lượng. Chất đường trong dịch truyền trên là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Dựa vào kiến thức lý thuyết tổng hợp về tính chất của các hợp chất cacbohiđrat.
Giải chi tiết:
Chất đường trong dịch truyền trên là glucozơ.
Câu 9:
Phát biểu nào sai về tripeptit Gly-Ala-Val?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào kiến thức về tính chất hóa học của peptit và protein.
Giải chi tiết:
A sai vì tripeptit Gly-Ala-Val không phản ứng với HNO3 đặc tạo kết tủa vàng.
Kết tủa vàng xuất hiện khi cho dung dịch HNO3(đ) phản ứng chủ yếu do phản ứng nitro hóa vòng benzen ở các gốc amino axit Phe, Tyr,…
Câu 10:
Polime nào sau đây có cấu trúc mạng lưới không gian?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Dựa vào kiến thức về vật liệu polime.
Giải chi tiết:
Cao su lưu hóa có cấu trúc mạng lưới không gian.
Câu 11:
Lên men rượu m gam tinh bột thu được V lít CO2 (đktc). Toàn bộ lượng CO2 sinh ra được hấp thụ vào dung dịch Ca(OH)2 dư thu được 12 gam kết tủa. Biết hiệu suất quá trình lên men là 90%. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
(C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2
Dựa vào PTHH ⟹ nC6H12O6 (LT) = nCO2/2 = nCaCO3/2 (mol) ⟹ ntinh bột (LT) = nC6H12O6 (LT)/n (mol).
Do H = 90% ⟹ ntinh bột (TT) ⟹ m.
Giải chi tiết:
nCaCO3 = 12/100 = 0,12 (mol).
(C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2
Theo PTHH ⟹ nC6H12O6 (LT) = nCO2/2 = nCaCO3/2 = 0,06 (mol)
⟹ ntinh bột (LT) = nC6H12O6 (LT)/n = 0,06/n (mol).
Do H = 90% ⟹ ntinh bột (TT) = (0,06/n).(100%/90%) = 1/15n (mol).
Vậy m = 162n.1/15n = 10,8 (gam).
Câu 12:
Polime được điều chế từ phản ứng trùng ngưng là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào kiến thức về vật liệu polime.
Giải chi tiết:
Tơ lapsan được điều chế từ phản ứng trùng ngưng giữa axit terephtalic và etilen glicol.
Câu 13:
Tơ nào sau đây thuộc loại tơ nhân tạo?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Dựa vào kiến thức về vật liệu polime.
Giải chi tiết:
Tơ axetat thuộc loại tơ nhân tạo (tơ bán tổng hợp).
Câu 14:
Cho dãy chuyển hóa: Glyxin X1 X2. Vậy X2 là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào tính chất hóa học của glyxin.
Giải chi tiết:
H2N – CH2 – COOH ClH3N – CH2 – COOH H2N – CH2 – COONa.
PTHH:
H2N – CH2 – COOH + HCl → ClH3N – CH2 – COOH (X1)
ClH3N – CH2 – COOH + 2NaOH → H2N – CH2 – COONa (X2) + NaCl + 2H2O
Vậy X2 là H2NCH2COONa.
Câu 15:
Hiđro hóa hoàn toàn triolein thu được triglixerit X. Đun X với dung dịch NaOH dư, thu được muối nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Triolein có công thức là (C17H33COO)3C3H5 khi hiđro hóa sẽ tạo thành (C17H35COO)3C3H5 (X).
Dựa vào phản ứng hóa học giữa X và dung dịch NaOH ⟹ muối.
Giải chi tiết:
Triolein có công thức là (C17H33COO)3C3H5 khi hiđro hóa sẽ tạo thành (C17H35COO)3C3H5 (X).
PTHH: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3.
Vậy muối thu được là natri stearat.
Câu 16:
Thủy tinh hữu cơ plexiglas là loại chất dẻo rất bền, trong suốt, có thể cho gần 90% ánh sáng truyền qua nên được sử dụng làm kính chống đạn, kính ô tô, kính máy bay, răng giả, ... Monome dùng sản xuất thủy tinh hữu cơ có tên gọi là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào kiến thức về vật liệu polime.
Giải chi tiết:
Monome trùng hợp ra thủy tinh hữu cơ plexiglas là metyl metacrylat (CH2 = C(CH3) – COOCH3).
Câu 17:
Khi thủy phân este metyl benzoat trong dung dịch NaOH dư, đun nóng thu được sản phẩm hữu cơ gồm
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Este metyl benzoat có công thức là C6H5COOCH3.
Dựa vào phản ứng hóa học giữa este và dung dịch NaOH ⟹ sản phảm hữu cơ.
Giải chi tiết:
Este metyl benzoat có công thức là C6H5COOCH3.
PTHH: C6H5COOCH3 + NaOH → C6H5COONa + CH3OH.
Câu 18:
Phân tử khối trung bình của một loại cao su thiên nhiên là 98600. Số mắt xích trung bình của loại cao su trên là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Cao su thiên nhiên có công thức phân tử là (C5H8)n (với n là số mắt xích trung bình).
Ta có Mtb = 68n = 98600 ⟹ n (số mắt xích trung bình).
Giải chi tiết:
Cao su thiên nhiên có công thức phân tử là (C5H8)n (với n là số mắt xích trung bình).
Ta có Mtb = 68n = 98600 ⟹ n = 1450.
Vậy số mắt xích trung bình của loại cao su thiên nhiên trên là 1450.
Câu 19:
Cho 4,5 gam amin X no, đơn chức, mạch hở tác dụng với dung dịch HCl dư thu được 8,15 gam muối. Số nguyên tử hiđro trong phân tử X là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Gọi công thức phân tử của X là CnH2n+3N (n ≥ 1).
PTHH: CnH2n+3N + HCl → CnH2n+4NCl
Bảo toàn khối lượng ⟹ mHCl ⟹ nHCl ⟹ nX ⟹ n ⟹ CTPT của X.
Giải chi tiết:
Gọi công thức phân tử của X là CnH2n+3N (n ≥ 1).
PTHH: CnH2n+3N + HCl → CnH2n+4NCl
Bảo toàn khối lượng ⟹ mHCl = mmuối – mX = 3,65 (g) ⟹ nHCl = 3,65/36,5 = 0,1 (mol).
Theo PTHH ⟹ nX = nHCl = 0,1 (mol).
⟹ MX = 14n + 17 = 4,5/0,1 = 45 ⟹ n = 2.
Vậy CTPT của X là C2H7N (số H là 7).
Câu 20:
Este etyl butirat có mùi dứa. Công thức cấu tạo của etyl butirat là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào kiến thức tổng hợp về công thức của một số este thường gặp.
Giải chi tiết:
Công thức cấu tạo của etyl butirat là CH3CH2CH2COOCH2CH3.
Câu 21:
Anilin (C6H5NH2) và phenol (C6H5OH) đều có phản ứng với
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào tính chất hóa học của anilin và phenol.
Giải chi tiết:
Anilin (C6H5NH2) và phenol (C6H5OH) đều có phản ứng với dung dịch Br2 tạo kết tủa trắng.
PTHH:
C6H5NH2 + 3Br2 → C6H2(Br3)NH2 ↓trắng + 3HBr
C6H5OH + 3Br2 → C6H2(Br3)OH ↓trắng + 3HBr
Câu 22:
Cho các phát biểu sau về cacbohiđrat:
(a) Hồ tinh bột phản ứng với I2 cho dung dịch màu xanh tím.
(b) Tinh bột và xenlulozơ đều là polisaccarit.
(c) Fructozơ và saccarozơ đều không làm mất màu dung dịch Br2.
(d) Thủy phân hoàn saccarozơ trong môi trường axit chỉ thu được một loại monosaccarit duy nhất.
(e) Cacbohiđrat thường có công thức phân tử chung là Cn(H2O)m.
(f) Glucozơ và saccarozơ đều tác dụng với H2 (xúc tác Ni, đun nóng) tạo sobitol.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Dựa vào kiến thức tổng hợp về các hợp chất cacbohiđrat.
Giải chi tiết:
(a), (b), (c), (e) đúng.
(d) sai vì thủy phân hoàn saccarozơ trong môi trường axit thu được glucozơ và fructozơ.
(f) sai vì glucozơ và fructozơ (không phải saccarozơ) tác dụng với H2 (xúc tác Ni, đun nóng) tạo sobitol.
Câu 23:
Số đồng phân amin bậc II của C4H11N là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào cách viết đồng phân amin (amin bậc 2 có dạng là R – NH – R’).
Giải chi tiết:
Các đồng phân amin bậc II của C4H11N là
CH3 – NH – CH2 – CH2 – CH3
CH3 – NH – CH(CH3) – CH3
CH3 – CH2 – NH – CH2 – CH3
Câu 24:
Từ chất X thực hiện các phản ứng hóa học sau:
(1) X + KOH Y + Z;
(2) Y + Br2 + H2O → T + 2HBr;
(3) T + KOH → Z + H2O.
Chất X có thể là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào đáp án và phản ứng (2) ⟹ Y là CH3CHO ⟹ T là CH3COOH và X có dạng RCOOCH=CH2.
Dựa vào phản ứng (3) ⟹ Z ⟹ X (dựa vào phản ứng (1)).
Giải chi tiết:
Dựa vào đáp án và phản ứng (2) ⟹ Y là CH3CHO ⟹ T là CH3COOH và X có dạng RCOOCH=CH2.
(2) CH3CHO (Y) + Br2 + H2O → CH3COOH (T) + 2HBr
(3) CH3COOH (T) + KOH → CH3COOK (Z) + H2O
(1) CH3COOCH=CH2 (X) + KOH CH3COOK (Z) + CH3CHO (Y)
Vậy X có thể là CH3COOCH=CH2.
Câu 25:
Nhận xét nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết chung về polime.
Giải chi tiết:
A sai, ví dụ các polime thuộc loại poliamit chứa nhóm CONH sẽ kém bền trong axit và bazo.
B sai, đa số polime không tan trong các dung môi thông thường.
C sai, hầu hết polime là các chất rắn không bay hơi.
D đúng.
Câu 26:
Đun hỗn hợp X gồm 12 gam axit axetic và 11,5 gam ancol etylic với xúc tác H2SO4 đặc trong điều kiện thích hợp thu được 12,32 gam este. Hiệu suất phản ứng este hóa là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Cách xác định hiệu suất tính theo chất nào?
Tương tự như cách xác định chất phản ứng hết.
PTHH: aA + bB → cC + dD
Đề bài cho biết nA và nB. Để biết được hiệu suất tính theo chất nào ta so sánh tỉ số và .
Tỉ số nào nhỏ hơn thì hiệu suất tính theo chất đó.
Giải chi tiết:
nCH3COOH = 12/60 = 0,2 mol
nC2H5OH = 11,5/46 = 0,25 mol
nCH3COOC2H5 = 12,32/88 = 0,14 mol
PTHH: CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O (H2SO4 đặc, to)
Bđ: 0,2 0,25 (do 0,2/1 < 0,25/1 ⟹ H% tính theo CH3COOH)
Pư: 0,14 ← 0,14 ← 0,14
⟹ H% = = 70%.
Câu 27:
Số tripeptit mạch hở có công thức phân tử C7H13O4N3 là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Ta thấy tripeptit có 7C ⟹ Tripeptit này được tạo bởi 2Gly và 1Ala.
Từ đó viết công thức các peptit thỏa mãn.
Giải chi tiết:
Ta thấy tripeptit có 7C ⟹ Tripeptit này được tạo bởi 2Gly và 1Ala.
Vậy có 3 peptit thỏa mãn là: Gly-Gly-Ala; Gly-Ala-Gly; Ala-Gly-Gly.
Câu 28:
Cho 13 gam C2H2 phản ứng với nước xúc tác HgCl2, đun nóng (hiệu suất phản ứng là 60%) thu được hỗn hợp A gồm CH3CHO và C2H2 dư. Cho A tác dụng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được m gam kết tủa. Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
- Tính được nC2H2(bđ) ⟹ nC2H2(pư) = nC2H2(bđ).H%.
- Tính theo PTHH để xác định thành phần của A:
C2H2 + H2O → CH3CHO (xt: Hg2+)
- Khi cho A + dd AgNO3:
C2H2 → Ag2C2 ↓
CH3CHO → 2Ag ↓
⟹ mkết tủa = mAg2C2 + mAg.
Giải chi tiết:
nC2H2(bđ) = 0,5 mol ⟹ nC2H2(pư) = 0,5.60% = 0,3 mol.
C2H2 + H2O → CH3CHO (xt: Hg2+)
Bđ: 0,5 (mol)
Pư: 0,3 → 0,3 (mol)
Sau: 0,2 0,3 (mol)
⟹ A gồm C2H2 dư (0,2 mol) và CH3CHO (0,3 mol).
- Khi cho A + dd AgNO3:
C2H2 → Ag2C2 ↓
0,2 → 0,2 (mol)
CH3CHO → 2Ag ↓
0,3 → 0,6 (mol)
⟹ mkết tủa = mAg2C2 + mAg = 0,2.240 + 0,6.108 = 112,8 gam.
Câu 29:
Chất nào sau đây không phải là este?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Khi thay nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm OR (R ≠ H) thì được este.
Giải chi tiết:
Chất C2H5COOH thuộc loại axit cacboxylic, không phải este.
Câu 30:
Cho dãy các dung dịch: saccarozơ, etyl axetat, glixerol, ancol etylic, axit axetic, Gly-Ala, anbumin. Số chất phản ứng với Cu(OH)2 ở điều kiện thường là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Một số loại chất thường gặp phản ứng với Cu(OH)2 ở điều kiện thường là:
- Axit cacboxylic.
- Chất có nhiều nhóm -OH gắn vào các nguyên tử C cạnh nhau.
- Peptit có từ 2 liên kết peptit trở lên (tripeptit trở lên).
Giải chi tiết:
Các chất phản ứng với Cu(OH)2 ở điều kiện thường: saccarozơ, glixerol, axit axetic, anbumin (4 chất).
Câu 31:
Cho hỗn hợp X gồm 3 este (chỉ chứa chức este) tạo bởi axit fomic với các ancol metylic, etylen glicol và glixerol. Đốt cháy hoàn toàn m gam X cần 3,584 lít O2 (đktc) thu được CO2 và 2,52 gam nước. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Các este trong X là HCOOCH3, (HCOO)2C2H4, (HCOO)3C3H5 đều có đặc điểm chung là số nguyên tử C bằng số nguyên tử O.
Như vậy ta đặt nO(X) = nC(X) = a mol.
BTNT C ⟹ nCO2 = nC(X) = a mol.
BTNT O ⟹ nO(X) + 2nO2 = 2nCO2 + nH2O ⟹ giá trị của a.
BTKL ⟹ mX = mCO2 + mH2O - mO2.
Giải chi tiết:
Tính được nO2 = 0,16 mol; nH2O = 0,14 mol.
Các este trong X là HCOOCH3, (HCOO)2C2H4, (HCOO)3C3H5 đều có đặc điểm chung là số nguyên tử C bằng số nguyên tử O.
Như vậy ta đặt nO(X) = nC(X) = a mol.
BTNT C ⟹ nCO2 = nC(X) = a mol.
BTNT O ⟹ nO(X) + 2nO2 = 2nCO2 + nH2O
⟹ a + 2.0,16 = 2a + 0,14
⟹ a = 0,18.
BTKL: mX = mCO2 + mH2O - mO2 = 0,18.44 + 0,14.18 - 0,16.32 = 5,32 gam.
Câu 32:
Đốt cháy hoàn toàn m gam hỗn hợp X gồm xenlulozơ, tinh bột, glucozơ và sacarozơ cần 13,44 lít O2 (đktc). Mặt khác thủy phân hoàn toàn m gam X trong môi trường axit thu được dung dịch Y. Lấy toàn bộ lượng glucozơ và fructozơ trong Y cho tác dụng với lượng dư dung dịch AgNO3/NH3 thu được a gam Ag. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
- Khi đốt cacbohiđrat luôn có: nCO2 = nO2(pư).
BTNT C ⟹ nC(X) = nCO2.
- Khi thủy phân hoàn toàn hỗn hợp X ta thu được glucozơ và fructozo đều có CTPT C6H12O6. Gọi công thức chung của chúng là C6H12O6.
BTNT C ⟹ nC6H12O6 = 1/6.nC(X).
- Khi cho glucozơ và fructozơ tráng gương:
C6H12O6 → 2Ag
⟹ nAg = 2nC6H12O6 ⟹ mAg.
Giải chi tiết:
- Khi đốt cacbohiđrat luôn có: nCO2 = nO2(pư) = 0,6 mol.
BTNT C ⟹ nC(X) = nCO2 = 0,6 mol.
- Khi thủy phân hoàn toàn hỗn hợp X ta thu được glucozơ và fructozo đều có CTPT C6H12O6. Gọi công thức chung của chúng là C6H12O6.
BTNT C ⟹ nC6H12O6 = 1/6.nC(X) = 0,1 mol.
- Khi cho glucozơ và fructozơ tráng gương:
C6H12O6 → 2Ag
0,1 → 0,2 (mol)
⟹ mAg = 0,2.108 = 21,6 gam.
Câu 33:
Đốt cháy hoàn toàn một lượng triglixerit X cần dùng 1,61 mol O2, thu được 1,14 mol CO2 và 1,06 mol H2O. Cho 26,58 gam X tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
*X + O2 → CO2 + H2O:
+) Áp dụng BTKL ⟹ mX.
+) BTNT O: 6nX + 2nO2 = 2nCO2 + nH2O ⟹ nX.
Tính số mol X trong 26,58 gam X dựa vào tỷ lệ tương ứng.
*26,58 gam X + NaOH vừa đủ:
X + 3NaOH → Muối + C3H5(OH)3
BTKL: mmuối = mX + mNaOH - mglixerol.
Giải chi tiết:
*X + O2: 1,61 → CO2: 1,14 + H2O: 1,06
+) BTKL: mX = 44.1,14 + 18.1,06 - 32.1,61 = 17,72 gam.
+) BTNT O: 6nX + 2nO2 = 2nCO2 + nH2O
⟹ 6nX + 2.1,61 = 2.1,14 + 1,06
⟹ nX = 0,02 mol.
Tỷ lệ: 17,72 gam X tương ứng với 0,02 mol X.
⟹ 26,58 gam …………………0,03 mol.
*26,58 gam X + NaOH vừa đủ:
X + 3NaOH → Muối + C3H5(OH)3
0,03 → 0,09 → 0,03 (mol)
BTKL: mmuối = mX + mNaOH - mglixerol = 26,58 + 0,09.40 - 0,03.92 = 27,42 gam.
Câu 34:
Hỗn hợp A gồm 1 amin đơn chức, 1 anken và 1 ankan. Đốt cháy hoàn toàn 12,95 gam hỗn hợp A cần V lít O2 thu được 19,04 lít CO2; 0,56 lít N2 và m gam nước. Biết các thể tích khí đo ở đktc. Tính V?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Sơ đồ:
+) BTKL: mhh A + mO2 = mCO2 + mH2O + mN2 ⟹ phương trình (1)
+) BTNT O: 2nO2 = 2nCO2 + nH2O ⟹ phương trình (2)
Giải hệ (1) (2) được a và b ⟹ giá trị của V.
Giải chi tiết:
Sơ đồ:
+) BTKL: mhh A + mO2 = mCO2 + mH2O + mN2
⟹ 12,95 + 32a = 44.0,85 + 18b + 28.0,025
⟹ 32a - 18b = 25,15 (1)
+) BTNT O: 2nO2 = 2nCO2 + nH2O
⟹ 2a = 2.0,85 + b
⟹ 2a - b = 1,7 (2)
Giải hệ (1) (2) được a = 1,3625; b = 1,025.
⟹ V = 22,4.1,3625 = 30,52 lít.
Câu 35:
Cho hỗn hợp A gồm 0,1 mol alanin và 0,15 mol axit glutamic tác dụng với 300 ml dung dịch NaOH 1M, sau phản ứng thu được dung dịch B. Cho B phản ứng vừa đủ với dung dịch HCl thu được dung dịch D chứa m gam hỗn hợp muối tan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Để đơn giản ta coi B gồm Ala, Glu, NaOH.
Ala + HCl → Muối
Glu + HCl → Muối
NaOH + HCl → NaCl + H2O
BTKL: mmuối = mAla + mGlu + mNaOH + mHCl - mH2O
Giải chi tiết:
Để đơn giản ta coi B gồm Ala, Glu, NaOH.
Ala + HCl → Muối
0,1 → 0,1 (mol)
Glu + HCl → Muối
0,15 → 0,15 (mol)
NaOH + HCl → NaCl + H2O
0,3 → 0,3 → 0,3 (mol)
BTKL: mmuối = mAla + mGlu + mNaOH + mHCl - mH2O
= 0,1.89 + 0,15.147 + 0,3.40 + 36,5.(0,1 + 0,15 + 0,3) - 0,3.18
= 57,625 gam.
Câu 36:
Đun nóng 13,6 gam hỗn hợp gồm benzyl fomat và phenyl axetat với dung dịch KOH dư, thấy lượng KOH phản ứng là 0,16 mol, thu được m gam muối. Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
- Đặt ẩn là số mol mỗi chất.
- Đặt số mol mỗi chất vào các PTHH:
HCOOCH2C6H5 + KOH → HCOOK + C6H5CH2OH
CH3COOC6H5 + 2KOH → CH3COOK + C6H5OK + H2O
- Lập hệ phương trình về khối lượng hỗn hợp và số mol KOH. Giải hệ tìm được số mol các chất.
- Xác định thành phần của muối ⟹ giá trị của m.
Giải chi tiết:
HCOOCH2C6H5 + KOH → HCOOK + C6H5CH2OH
x → x → x (mol)
CH3COOC6H5 + 2KOH → CH3COOK + C6H5OK + H2O
y → 2y → y → y (mol)
Ta có hệ phương trình
Muối chứa HCOOK (0,04 mol); CH3COOK (0,06 mol) và C6H5OK (0,06 mol).
⟹ m = mmuối = 17,16 gam.
Câu 37:
Tiến hành các bước thí nghiệm như sau:
Bước 1: Cho một nhúm bông vào cốc đựng dung dịch H2SO4 70%, đun nóng đồng thời khuấy đều đến khi thu được dung dịch đồng nhất.
Bước 2: Trung hòa dung dịch thu được bằng dung dịch NaOH 10%.
Bước 3: Lấy dung dịch sau khi trung hòa cho vào ống nghiệm đựng dung dịch AgNO3 trong NH3 dư, sau đó đun nóng.
Nhận định nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Lý thuyết về xenlulozo.
Giải chi tiết:
(C6H10O5)n (xenlulozơ) + nH2O nC6H12O6 (glucozơ)
A sai, dung dịch I2 chỉ tạo được dung dịch màu xanh tím với hồ tinh bột.
B sai, trong cốc chỉ thu được 1 loại saccarit là glucozơ.
C đúng, vì glucozơ có phản ứng tráng gương.
D sai, phản ứng trên chứng minh xenlulozơ thủy phân sinh ra glucozơ.
Câu 38:
Hỗn hợp E gồm tripeptit X (Gly-Ala-Lys) và chất hữu cơ Y (C4H12O2N2) đều mạch hở. Cho m gam E phản ứng vừa đủ với 400 ml dung dịch NaOH 1M, đun nóng, thu được 2,24 lít khí Z (đktc) và dung dịch chứa 3 muối. Đốt cháy Z bằng oxi rồi cho sản phẩm cháy qua dung dịch H2SO4 đặc dư thì khối lượng dung dịch tăng 4,5 gam và thoát 0,15 mol hỗn hợp khí CO2 và N2. Mặt khác, cho m gam E phản ứng với dung dịch HCl dư thu được a gam muối. Các phản ứng xảy ra hoàn toàn. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Biện luận tìm được công thức Z là CH3NH2 ⟹ Y: CH3CH(NH2)COONH3CH3.
*E + NaOH:
Gly-Ala-Lys + 3NaOH → GlyNa + AlaNa + LysNa + H2O
CH3CH(NH2)COONH3CH3 + NaOH → CH3CH(NH2)COONa + CH3NH2 + H2O
Từ nZ ⟹ nY ⟹ nX.
*E + HCl:
Gly-Ala-Lys + 2H2O + 4HCl → Muối
CH3CH(NH2)COONH3CH3 + 2HCl → CH3CH(NH3Cl)COOH + CH3NH3Cl
Áp dụng BTKL: mmuối = mE + mH2O + mHCl.
Giải chi tiết:
3 muối là GlyNa, AlaNa, LysNa ⟹ Y tạo ra 1 trong 3 muối này.
Nhưng do Y chỉ có 4C nên không tạo được LysNa ⟹ Y tạo GlyNa hoặc AlaNa.
Theo đề đốt khí Z thu được H2O, CO2, N2 ⟹ Z là amin ⟹ Y là muối của amino axit và amin ⟹ Z là amin đơn chức.
nZ = 0,1 mol ⟹ nN2(do Z) = 0,05 mol ⟹ nCO2(do Z) = 0,15 - 0,05 = 0,1 mol.
⟹ CZ = nCO2(do Z) : nZ = 0,1 : 0,1 = 1 ⟹ Z là CH3NH2
⟹ Y là CH3CH(NH2)COONH3CH3.
*E + NaOH:
Gly-Ala-Lys + 3NaOH → GlyNa + AlaNa + LysNa + H2O
0,1 ← 0,4 - 0,1 (mol)
CH3CH(NH2)COONH3CH3 + NaOH → CH3CH(NH2)COONa + CH3NH2 + H2O
0,1 ← 0,1 ← 0,1 (mol)
*E + HCl:
Gly-Ala-Lys + 2H2O + 4HCl → Muối
0,1 → 0,2 → 0,4 (mol)
CH3CH(NH2)COONH3CH3 + 2HCl → CH3CH(NH3Cl)COOH + CH3NH3Cl
0,1 → 0,2 (mol)
BTKL: mmuối = mE + mH2O + mHCl = 0,1.274 + 0,1.120 + 0,2.18 + 0,6.36,5 = 64,9 gam.
Câu 39:
Hỗn hợp X chứa butan, đietylamin, etyl propionat và valin. Đốt cháy hoàn toàn 0,4 mol X cần dùng 2,66 mol O2, thu được CO2, H2O và N2. Toàn bộ sản phẩm cháy được dẫn vào dung dịch Ca(OH)2 dư thì thấy có a mol khí không bị hấp thụ. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Butan: C4H10
Đietylamin: C4H11N = C4H10 + NH
Etyl propionat: C5H10O2
Valin: C5H11O2N = C5H10O2 + NH
⟹ Quy đổi hỗn hợp thành C4H10, C5H10O2, NH
Giải chi tiết:
Butan: C4H10
Đietylamin: C4H11N = C4H10 + NH
Etyl propionat: C5H10O2
Valin: C5H11O2N = C5H10O2 + NH
⟹ Quy đổi hỗn hợp thành C4H10, C5H10O2, NH
Sơ đồ:
+) nhh X = x + y = 0,4 (1)
+) BTNT O ⟹ 2nC5H10O2 + 2nO2 = 2nCO2 + nH2O
⟹ 2y + 2.2,66 = 2.(4x + 5y) + 5x + 5y + 0,5z
⟹ 13(x + y) + 0,5z = 5,32 (2)
Thay (1) vào (2) ⟹ z = 0,24.
Khí không bị hấp thụ là N2 ⟹ nN2 = 0,5z = 0,12 mol.
Câu 40:
Cho hỗn hợp E gồm các oligopeptit đều được tạo thành từ Gly; Ala và Val. Thủy phân hoàn toàn 0,12 mol E trong NaOH dư thì thấy có 0,72 mol NaOH tham gia phản ứng. Toàn bộ lượng muối thu được đem đốt cháy thì cần dùng vừa đủ 3,24 mol O2. Khối lượng (gam) của 0,12 mol E là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Do các peptit đều được tạo nên từ các a.a có 1 nhóm NH2 và 1 nhóm COOH
⟹ Quy đổi hỗn hợp thành CONH, CH2, H2O (với số mol H2O bằng số mol peptit).
Giải chi tiết:
Do các peptit đều được tạo nên từ các a.a có 1 nhóm NH2 và 1 nhóm COOH
⟹ Quy đổi hỗn hợp thành CONH, CH2, H2O (với số mol H2O bằng số mol peptit).
⟹ nCONH = nNaOH = 0,72 mol; nH2O = npeptit = 0,12 mol.
Bảo toàn O cho phản ứng đốt muối ⟹ 2nCOONa + 2nO2 = 3nNa2CO3 + 2nCO2 + nH2O
⟹ 2.0,72 + 2.3,24 = 3.0,36 + 2.(x + 0,36) + (x + 0,72)
⟹ x = 1,8.
⟹ mE = mCONH + mCH2 + mH2O = 0,72.43 + 1,8.14 + 0,12.18 = 58,32 gam.
