[Năm 2022] Đề thi thử môn Hóa THPT Quốc gia có lời giải (30 đề)
[Năm 2022] Đề thi thử môn Hóa THPT Quốc gia có lời giải (Đề 9)
-
12927 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Để có 297 kg xenlulozơ trinitrat, cần dùng a gam xenlulozơ và dung dịch chứa m kg axit nitric. Biết hiệu suất phản ứng đạt 90%. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
(C6H10O5)n + 3nHNO3 → [C6H7O2(ONO2)3]n + 3nH2O
Giải chi tiết:
(C6H10O5)n + 3nHNO3 → [C6H7O2(ONO2)3]n + 3nH2O
162n 3n.63 297n (kg)
x 297 (kg)
⟹ kg.
Do H = 90% ⟹ mHNO3 (thực tế) = m = x/90% = 210 kg.
Câu 2:
Cho các phát biểu sau:
(1) Hiđro hóa hoàn toàn glucozơ cũng như fructozơ thu được axit gluconic.
(2) Glucozơ, fructozơ là nhóm cacbohiđrat đơn giản nhất, không thủy phân được.
(3) Thủy phân đến cùng xenlulozơ trong môi trường axit tạo ra nhiều phân tử monosaccarit.
(4) Trong phân tử saccarozơ gốc α-glucozơ và gốc β-glucozơ liên kết với nhau qua nguyên tử oxi.
(5) Tinh bột là chất rắn vô định hình, màu trắng, ở điều kiện thường không tan trong nước.
(6) Phân tử amilozơ và amilopectin có cấu trúc mạch phân nhánh.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào lý thuyết liên quan tới cacbohiđrat.
Giải chi tiết:
(1) sai: Hiđro hóa hoàn toàn glucozơ cũng như fructozơ thu được sobitol.
(4) sai: Trong phân tử saccarozơ gốc α-glucozơ và gốc β-fructozơ liên kết với nhau qua nguyên tử oxi.
(6) sai: Phân tử amilozơ có cấu trúc mạch không phân nhánh.
Câu 3:
Chất hữu cơ X mạch hở, có công thức phân tử C4H6O4, không tham gia phản ứng tráng bạc. Cho a mol X phản ứng với dung dịch KOH dư, thu được ancol Y và m gam một muối. Đốt cháy hoàn toàn Y, thu được 0,2 mol CO2 và 0,3 mol H2O. Giá trị của a và m lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
X + KOH → ancol Y và một muối
⟹ X là este no, 2 chức, mạch hở
⟹ Y là ancol no, mạch hở (1 chức hoặc 2 chức)
Giải chi tiết:
X + KOH → ancol Y và một muối
⟹ X là este no, 2 chức, mạch hở
⟹ Y là ancol no, mạch hở (1 chức hoặc 2 chức)
Y + O2 → CO2 + H2O
⟹ nY = nH2O – nCO2 = 0,1 mol.
BTNT C ⟹ số C (Y) = nCO2/nY = 2
Do X không tráng bạc ⟹ X chỉ có thể là HOOC-COOC2H5
HOOC-COOC2H5 + 2KOH → (COOK)2 + C2H5OH + H2O
0,1 0,1 ← 0,1 (mol)
Vậy a = 0,1 mol và m = m(COOK)2 = 16,6 g.
Câu 4:
Trong sơ đồ phản ứng sau:
(1) Xenlulozơ → glucozơ → X + CO2
(2) X + O2 → Y + H2O
Các chất X và Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Dựa vào tính chất hóa học của glucozơ.
Giải chi tiết:
C6H12O6 → 2C2H5OH + 2CO2
C2H5OH + O2 → CH3COOH + H2O
Vậy X và Y lần lượt là ancol etylic, axit axetic.
Câu 5:
Hỗn hợp gồm 0,1 mol một axit cacboxylic đơn chức và 0,1 mol muối của axit đó với kim loại kiềm có tổng khối lượng 15,8 gam. Tên của axit là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Gọi axit có dạng là RCOOH và muối có dạng RCOOA
Dựa vào số liệu đề bài cho ⟹ Phương trình liên hệ giữa R và A.
Giải chi tiết:
Gọi axit có dạng là RCOOH và muối có dạng RCOOA
Ta có m = 0,1(R + 45) + 0,1(R + 44 + A) = 15,8. ⟹ 2R + A = 69
Nhận thấy đáp án cho axit là axit no, đơn chức, mạch hở ⟹ A = 39 (K) và R = 15 (–CH3)
Vậy axit là CH3COOH (axit etanoic).
Câu 6:
Đốt cháy hoàn toàn m gam hỗn hợp X chứa tripanmitin, triolein, axit stearic, axit panmitic (trong đó số mol các chất béo bằng nhau). Sau phản ứng thu được 83,776 lít CO2 (đktc) và 57,24 gam nước. Mặt khác, đun nóng m gam X với dung dịch NaOH (dư) đến khi các phản ứng hoàn toàn thì thu được a gam glixerol. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Khi đốt cháy một hợp chất hữu cơ X bất kì có k liên kết π trong phân tử
⟹ nX = (k – 1).(nCO2 – nH2O)
Giải chi tiết:
* X gồm (C15H31COO)3C3H5 (x mol); (C17H33COO)3C3H5 (x mol); C17H35COOH ; C15H31COOH
Nhận thấy trong X có:
+ 2 axit chỉ có 1 liên kết π trong phân tử⟹ Khi đốt cháy cho nCO2 = nH2O.
+ (C15H31COO)3C3H5 có 3 liên kết π trong phân tử.
+ (C17H33COO)3C3H5 có 6 liên kết π trong phân tử.
X + O2 → CO2 + H2O
3,74 3,18 (mol)
⟹ nCO2 – nH2O = 2ntripanmitin + 5ntriolein = 7x = 0,56. ⟹ x = 0,08 mol.
* X + NaOH → C3H5(OH)3
⟹ nC3H5(OH)3 = ntripanmitin + ntriolein = 2x = 0,16 mol.
⟹ a = 0,16.92 = 14,72 g.
Câu 7:
X, Y, Z là 3 este mạch hở (trong đó X, Y đơn chức, Z hai chức). Đun nóng 19,28 gam hỗn hợp E chứa X, Y, Z với dung dịch NaOH vừa đủ, thu được hỗn hợp F chỉ chứa 2 muối có tỉ lệ số mol 1 : 1 và hỗn hợp 2 ancol no, có cùng số nguyên tử cacbon. Dẫn toàn bộ hỗn hợp 2 ancol này qua bình đựng Na dư thấy khối lượng bình tăng 8,1 gam. Đốt cháy toàn bộ F thu được CO2, 0,39 mol H2O và 0,13 mol Na2CO3. Các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của este có khối lượng phân tử nhỏ nhất trong E là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Đặt ancol là R(OH)n (0,26/n mol)
⟹ m tăng = (R + 16n).0,26/n = 8,1
⟹ R = 197n/13
Do 1 < n < 2 (este trong E là đơn chức và hai chức) ⟹ 15,2 < R < 30,4
⟹ Hai ancol là C2H5OH (x mol) và C2H4(OH)2 (y mol).
Dựa vào các dữ kiện tiếp theo xác định các muối ⟹ các este.
Giải chi tiết:
nNa2CO3 = 0,13 mol ⟹ nNaOH = 0,26 mol (BTNT Na).
Đặt ancol là R(OH)n (0,26/n mol)
⟹ m tăng = (R + 16n).0,26/n = 8,1
⟹ R = 197n/13
Do 1 < n < 2 (este trong E là đơn chức và hai chức) ⟹ 15,2 < R < 30,4
⟹ Hai ancol là C2H5OH (x mol) và C2H4(OH)2 (y mol)
⟹ x + 2y = 0,26 và 45x + 60y = 8,1
⟹ x = 0,02 và y = 0,12
Bảo toàn khối lượng:
⟹ mE + mNaOH = mmuối + mancol
⟹ mmuối = 21,32 gam
Trong muối có nNa = nNaOH = 0,26 mol ⟹ nO = 2nNa = 0,52 mol.
nH2O = 0,39 mol ⟹ nH = 0,78 mol.
mF = mC + mNa + mO + mH ⟹ mC = 6,24 g. ⟹ nC = 0,52 mol.
BTNT C ⟹ nCO2 = nC(muối) - nNa2CO3 = 0,39 mol
Vì nCO2 = nH2O ⟹ Các muối no, đơn chức, mạch hở.
⟹ nmuối = nNaOH = 0,26 ⟹ Số C(muối) = nC/nmuối = 0,52/0,26 = 2
Do 2 muối có số mol bằng nhau ⟹ Hai muối là HCOONa và C2H5COONa
Vậy các este trong E gồm
X: HCOOC2H5 (0,01 mol )
Y: C2H5COOC2H5 (0,01 mol)
Z: HCOO-CH2-CH2-OOC-C2H5 (0,12 mol)
⟹ %mX = 3,84%
Câu 8:
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Nhiệt độ sôi của những hợp chất có liên kết hiđro sẽ lớn hơn nhiệt độ sôi của những hợp chất không có liên kết hiđro ⟹ nhiệt độ sôi: axit > ancol > este.
Với những hợp chất cùng dãy đồng đằng thì hợp chất có khối lượng mol lớn hơn sẽ có nhiệt độ sôi lớn hơn.
Giải chi tiết:
Nhiệt độ sôi của các chất sắp xếp theo chiều tăng dần là (2) < (4) < (5) < (1) < (3).
Câu 9:
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Hỗn hợp m gồm tất cả các chất đều là cacbohiđrat có dạng Cn(H2O)m
PTHH: Cn(H2O)m + nO2 → nCO2 + mH2O
Theo PTHH ⟹ nCO2 = nO2
Giải chi tiết:
Hỗn hợp m gồm tất cả các chất đều là cacbohiđrat có dạng Cn(H2O)m
PTHH: Cn(H2O)m + nO2 → nCO2 + mH2O
Theo PTHH ⟹ nCO2 = nO2 = 0,24 mol.
Áp dụng ĐLBTKL ⟹ m + mO2 = mCO2 + mH2O ⟹ m = 6,84 g.
Câu 10:
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Dựa vào cách gọi tên của este.
Giải chi tiết:
CH3COOCH3 có tên gọi là metyl axetat.
Câu 11:
X là một triglixerit. Xà phòng hóa hoàn toàn m gam bằng một lượng KOH vừa đủ, cô cạn dung dịch thu được hỗn hợp muối khan Y. Đốt cháy hoàn toàn Y cần vừa đủ 4,41 mol O2, thu được K2CO3; 3,03 mol CO2 và 2,85 mol H2O. Mặt khác m gam X tác dụng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
X được tạo bởi axit béo và C3H5(OH)3
X phản ứng với Br2 do liên kết π có trong của axit béo
⟹ (với (k – 1) là số liên kết π có trong của axit béo ).
Giải chi tiết:
X được tạo bởi axit béo và C3H5(OH)3
(1)
Gọi số mol của muối Y là x mol.
BTNT K ⟹ nK2CO3 = 0,5x (mol)
BTNT O ⟹ 2nY + 2nO2 = 2nCO2 + nH2O + 3nK2CO3
⟹ 2x + 4,41.2 = 2.3,03 + 2,85 + 3.0,5x ⟹ x = 0,18 mol.
Giả sử Y có k liên kết π có trong axit béo.
⟹ nCO2 – nH2O = (k – 1)nY
⟹ 3,03 – 2,85 = (k – 1).0,18 mol
⟹ k = 2
⟹
Câu 12:
Cho các este: vinyl axetat, vinyl benzoat, etyl axetat, isoamyl axetat, phenyl axetat, anlyl axetat. Số este có thể điều chế trực tiếp bằng phản ứng của axit và ancol tương ứng (có H2SO4 đặc làm xúc tác) là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Xác định những este được điều chế trực tiếp từ axit và ancol tương ứng.
Giải chi tiết:
Este có thể điều chế trực tiếp bằng phản ứng của axit với ancol tương ứng (có H2SO4 đặc làm xúc tác) là etyl axetat, isoamyl axetat, anlyl axetat. ⟹ Có 3 chất.
Câu 13:
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Xác định CTCT hoặc CTPT của etylfomat để tìm ra PTK
Giải chi tiết:
Etylfomat có công thức cấu tạo là HCOOC2H5 ⟹ PTK = 74.
Câu 14:
Este nào sau đây khi đun nóng với lượng dư dung dịch NaOH, thu được các sản phẩm hữu cơ đều không làm mất màu nước brom?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Este phản ứng với NaOH tạo ra sản phẩm chỉ chứa liên kết đơn.
Giải chi tiết:
CH3CH2COOCH3 + NaOH → CH3CH2COONa + CH3OH
⟹ Sản phẩm hữu cơ là CH3CH2COONa và CH3OH đều không làm mất màu nước brom.
Câu 15:
Tổng số chất hữu cơ mạch hở, có cùng công thức phân tử C2H4O2 là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Xác định số đồng phân của C2H4O2.
Giải chi tiết:
C2H4O2 có các đồng phân: CH3COOH ; HCOOCH3 ; HO-CH2-CHO
Câu 16:
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Saccarozơ → Glucozơ + Fructozơ
Giải chi tiết:
Saccarozơ → Glucozơ + Fructozơ
1 → 1 1 (mol)
Câu 17:
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Ta có nE = nNaOH = nmuối = nancol
Mà mmuối > mE ⟹ MNa = 23 > MR’(E) ⟹ Ancol tạo nên este trong E là CH3OH.
Áp dụng ĐLBTKL ⟹ neste.
Từ phản ứng đốt cháy ⟹ trong este.
⟹ Tìm được CTCT của X, Y, Z. ⟹ %mY.
Giải chi tiết:
Gọi số mol X, Y và Z trong E lần lượt là 4,5x ; 1,5x và x (mol)
Ta có nE = nNaOH = nmuối = nancol = 7x (mol)
Mà mmuối > mE ⟹ MNa = 23 > MR’(E) ⟹ Ancol tạo nên este trong E là CH3OH.
*
Áp dụng ĐLBTKL ⟹ mE + mNaOH = mmuối + mCH3OH
⟹ 9,34 + 40.7x = 10,46 + 32.7x ⟹ x = 0,02 mol.
*
Gọi số mol của CO2 và H2O lần lượt là a và b (mol)
+ Áp dụng ĐLBTKL ⟹ mE + mO2 = mCO2 + mH2O
⟹ 44a + 18b = 21,34 (1)
+ BTNT O ⟹ 2nE + 2nO2 = 2nCO2 + nH2O
⟹ 2a + b = 1,03 (2)
Từ (1)(2) ⟹ a = 0,35 và b = 0,33.
* Este E có ⟹ X là HCOOCH3
Gọi số C trong R2 và R3 lần lượt là n và m (m > n ≥ 1)
BTNT C ⟹ 2nX + (n + 2)nY + (m + 2)nZ = nCO2 = 0,35
⟹ 3n + 2m = 7
⟹ n = 1 và m = 2.
Vậy Y trong E là CH3COOCH3 0,03 mol
⟹ %mY = 23,77% ≈ 24%.
Câu 18:
Có hai axit hữu cơ no mạch hở A đơn chức, B đa chức. Ta tiến hành thí nghiệm như sau:
- Thí nghiệm 1: Hỗn hợp X1 chứa a mol A và b mol B. Để trung hòa X1 cần 500ml dung dịch NaOH 1M, nếu đốt cháy hoàn toàn X1 thì thu được 11,2 lít CO2.
- Thí nghiệm 2: Hỗn hợp X2 chứa b mol A và a mol B. Để trung hòa X2 cần 400ml dung dịch NaOH 1M. Biết a + b = 0,3 mol.
Nhận định nào sau đây liên quan đến axit B là đúng?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
* Xét TN1:
X1 + NaOH → muối + H2O
⟹ Số gốc –COOH (trong X1) = nNaOH/nX1 = 0,5/(a + b) (1)
X1 + O2 → CO2 + H2O.
BTNT C ⟹ Số C (X1)= nCO2/nX1 = 0,5/(a + b) (2)
Từ (1)(2) ⟹ Số C (X1) = Số gốc –COOH (X1)
⟹ 2 axit A và B.
Giải chi tiết:
* Xét TN1:
X1 + NaOH → muối + H2O
⟹ Số gốc –COOH (trong X1) = nNaOH/nX1 = 0,5/(a + b) (1)
X1 + O2 → CO2 + H2O.
BTNT C ⟹ Số C (X1)= nCO2/nX1 = 0,5/(a + b) (2)
Từ (1)(2) ⟹ Số C (X1) = Số gốc –COOH (X1)
Mà A và B lần lượt là axit no đơn chức và đa chức
⟹ A là HCOOH và B là HOOC – COOH.
Vậy X1 chứa HCOOH a mol và (COOH)2 b mol với a + 2b = 0,5 (1)
* Xét TN2:
X2 chứa HCOOH b mol và (COOH)2 a mol
X2 + NaOH (0,4 mol) ⟹ b + 2a = 0,4 (2)
Lại có a + b = 0,3 (3)
Từ (2)(3) ⟹ a = 0,1 và b = 0,2 (thỏa mãn (1)).
Xét các nhận định với axit B là HOOC – COOH
A đúng: Oxi hóa anđehit oxalic có thể tạo thành B
Câu 19:
Khử glucozơ bằng H2 để tạo sobitol. Khối lượng glucozơ dùng để tạo ra 1,82 gam sobitol với hiệu suất 80% là bao nhiêu?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
C6H12O6 + H2 → C6H14O6
Giải chi tiết:
C6H12O6 + H2 → C6H14O6
180 182 (g)
x 1,82 (g)
⟹ gam.
Do H = 80% ⟹ mglucozơ (thực tế) = x/80% = 2,25 gam.
Câu 20:
Triolein không tác dụng với chất (hoặc dung dịch) nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Triolein là este trong phân tử có chứa liên kết đôi.
Giải chi tiết:
Triolein có CTCT là (C17H33COO)C3H5 không phản ứng với Cu(OH)2 ở nhiệt độ thường.
Câu 21:
Chất béo là thức ăn quan trọng của con người, là nguồn cung cấp dinh dưỡng và năng lượng đáng kể cho cơ thể hoạt động. Ngoài ra, một lượng lớn chất béo được dùng trong công nghiệp để sản xuất
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về chất béo.
Giải chi tiết:
Một lượng lớn chất béo được dùng trong công nghiệp để sản xuất xà phòng và glixerol.
Câu 22:
Trong phòng thí nghiệm người ta điều chế etyl axetat từ axit axetic, etanol và H2SO4 (xúc tác) theo sơ đồ hình vẽ sau:
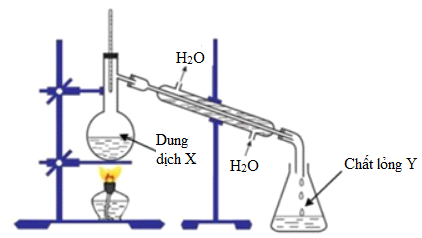
Sau khi kết thúc phản ứng este hóa, người ta tiến hành các bước sau:
+ Bước 1: Cho chất lỏng Y vào phễu chiết, lắc với dung dịch Na2CO3 đến khi quỳ tím chuyển màu xanh.
+ Bước 2: Mở khóa phễu chiết để loại bỏ phần chất lỏng phía dưới.
+ Bước 3: Thêm CaCl2 khan vào, sau đó tiếp tục bỏ đi rắn phía dưới thì thu được etyl axetat.
Cho các phát biểu sau:
(1) Nước trong ống sinh hàn nhằm tạo muôi trường có nhiệt độ thấp để hóa lỏng các chất hơi.
(2) CaCl2 được thêm vào để tách nước và ancol còn lẫn trong etyl axetat.
(3) Dung dịch Na2CO3 được thêm vào để trung hòa axit sunfuric và axit axetic trong chất lỏng Y.
(4) Dung dịch X được tạo từ axit axetic nguyên chất, etanol nguyên chất và H2SO4 98%.
(5) Có thể thay thế CaCl2 khan bằng dung dịch H2SO4 đặc.
Số phát biểu sai là:
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết về phản ứng điều chế este.
Giải chi tiết:
(1) đúng, tác dụng của ống sinh hàn là tạo môi trường có nhiệt độ thấp làm hóa lỏng các chất hơi.
(2) đúng, vì CaCl2 có tác dụng hút ẩm mạnh.
(3) sai, dung dịch Na2CO3 được thêm vào để trung hòa axit axetic trong chất lỏng Y còn H2SO4 là axit không bay hơi nên không có trong Y.
(4) đúng, sử dụng axit axetic nguyên chất, etanol nguyên chất và H2SO4 98% nhằm làm tăng hiệu suất phản ứng tạo este.
(5) sai, nếu dùng H2SO4 đặc thì có thể xảy ra phản ứng thủy phân este làm cho lượng este thu được bị hao hụt.
Vậy có 2 phát biểu sai.
Câu 23:
Trong số các este sau, este có mùi chuối chín là:
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Dựa vào tính chất vật lí của este.
Giải chi tiết:
Este có mùi chuối chín là: Isoamyl axetat (CTCT: CH3COO-CH2-CH2-CH(CH3)-CH3).
Câu 24:
Thuốc thử duy nhất có thể dùng để phân biệt 3 chất lỏng đựng trong 3 lọ riêng biệt mất nhãn: phenol, stiren, ancol benzylic là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Lý thuyết tổng hợp về hiđrocacbon, ancol, phenol.
Giải chi tiết:
Để phân biệt phenol, stiren, ancol benzylic ta dùng dung dịch Br2:
+ Xuất hiện kết tủa trắng → Phenol.
C6H5OH + 3Br2 → C6H2(OH)Br3 ↓ + 3HBr
+ Dung dịch Br2 nhạt màu → Stiren.
C6H5CH=CH2 + Br2 → C6H5CHBr-CH2Br
+ Không hiện tượng → Ancol benzylic.
Câu 25:
Một ancol no, mạch hở có công thức thực nghiệm (C2H5O)n. Số công thức cấu tạo của ancol có thể hòa tan Cu(OH)2 tạo dung dịch màu xanh lam là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
- Ancol no, mạch hở có H = 2C + 2.
- Các ancol có thể hòa tan Cu(OH)2 tạo dung dịch màu xanh lam là các ancol đa chức có các nhóm OH gắn vào những nguyên tử C cạnh nhau.
Giải chi tiết:
Giả sử CTPT của ancol là C2nH5nOn.
Vì là ancol no, mạch hở nên H = 2C + 2 ⟹ 5n = 2.2n + 2 ⟹ n = 2.
⟹ CTPT C4H10O2
Các ancol có thể hòa tan Cu(OH)2 tạo dung dịch màu xanh lam là các ancol đa chức có các nhóm OH gắn vào những nguyên tử C cạnh nhau.
⟹ Các ancol thỏa mãn là:
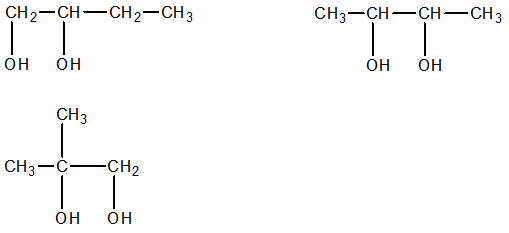
Câu 26:
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Lý thuyết về phản ứng tách nước ancol.
Giải chi tiết:
CH3-CH(CH3)-CH2-CH2-OH CH3-CH(CH3)-CH=CH2 + H2O
(3-metylbutan-1-ol)
Câu 27:
Cho sơ đồ phản ứng: Xenlulozơ X Y Z T. Chất T là
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Lý thuyết tổng hợp về cacbohiđrat.
Giải chi tiết:
Sơ đồ:
(C6H10O5)n C6H12O6 (X) C2H5OH (Y) CH3COOH (Z) CH3COOC2H5 (T).
PTHH:
(C6H10O5)n + nH2O nC6H12O6
C6H12O6 2C2H5OH + 2CO2
C2H5OH + O2 CH3COOH + H2O
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Câu 28:
Anđehit X có tỉ khối hơi so với H2 bằng 36. Số công thức cấu tạo có thể có của anđehit X là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Tính khối lượng mol của anđehit.
- Xét các trường hợp:
+ Nếu X là anđehit đơn chức RCHO ⟹ R
+ Nếu X là anđehit 2 chức R'(CHO)2 ⟹ R'
Giải chi tiết:
MX = 36 . 2 = 72 (g/mol)
+ Nếu X là anđehit đơn chức RCHO → R + 29 = 72 → R = 43 (C3H7-)
CH3-CH2-CH2-CHO
CH3-CH(CH3)-CHO
+ Nếu X là anđehit 2 chức R'(CHO)2 → R' + 29.2 = 72 → R' = 14 (-CH2-)
OHC-CH2-CHO
Vậy có 3 anđehit thỏa mãn.
Câu 29:
X và Y là hai cacbohiđrat. X là chất rắn, tinh thể không màu, dễ tan trong nước, có vị ngọt nhưng không ngọt bằng đường mía. Y là chất rắn ở dạng sợi, màu trắng, không có mùi vị. Tên gọi của X, Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Lý thuyết tổng hợp về cacbohiđrat.
Giải chi tiết:
- Theo các phương án A, B, C, D thì X là glucozơ hoặc fructozơ. Mà X không ngọt bằng đường mía → X là glucozơ.
- Y là chất rắn ở dạng sợi, màu trắng, không có mùi vị → Y là xenlulozơ.
Câu 30:
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Lý thuyết về tinh bột.
Giải chi tiết:
Khi thủy phân hoàn toàn tinh bột ta thu được glucozơ.
Câu 31:
X là hợp chất hữu cơ (chứa C, H, O) trong đó hiđro chiếm 2,439% về khối lượng. Đốt cháy hoàn toàn X thu được số mol nước bằng số mol X. Mặt khác, 1 mol X phản ứng vừa đủ với 4 mol AgNO3 trong dung dịch amoniac. Nhận định nào sau đây về X là đúng?
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Từ dữ kiện số mol nước bằng số mol X ⟹ Số nguyên tử H trong X.
- Từ phần trăm khối lượng H trong X ⟹ MX = 82
- Mặt khác, 1 mol X phản ứng vừa đủ với 4 mol AgNO3 → X là anđehit 2 chức (X không phải là HCHO vì MX = 82).
- Dựa vào MX suy ra CTCT của X.
Giải chi tiết:
Số H = = = 2 (do nH2O = nX)
Trong X, nguyên tố H chiếm 2,439% về khối lượng ⟹ MX = 2.(100/2,439) = 82 (g/mol)
Mặt khác, 1 mol X phản ứng vừa đủ với 4 mol AgNO3 → X là anđehit 2 chức.
Giả sử CTPT X là R(CHO)2 → R + 58 = 82 → R = 24 (-C≡C-)
⟹ X là OHC-C≡C-CHO
- A đúng, sơ đồ:
OHC-C≡C-CHO HO-(CH2)4-OH CH2=CH-CH=CH2 cao su buna.
- B sai, X là anđehit không no.
- C sai, X có số C > H.
- D sai, X có chứa 4 liên kết π.
Câu 32:
Để điều chế 45 gam axit lactic từ tinh bột qua con đường lên men lactic, hiệu suất thủy phân tinh bột và lên men lactic tương ứng là 90% và 80%. Khối lượng tinh bột cần dùng là
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Để đơn giản ta coi tinh bột có công thức C6H10O5.
Sơ đồ:
C6H10O5 C6H12O6 2 CH3-CH(OH)-COOH (axit lactic).
Theo sơ đồ nC6H10O5 = ½ naxit lactic ⟹ mtinh bột (lý thuyết)
⟹ mtinh bột (cần dùng) = mtinh bột (lý thuyết) . (100/H1) . (100/H2).
Giải chi tiết:
Để đơn giản ta coi tinh bột có công thức C6H10O5.
C6H10O5 C6H12O6 2 CH3-CH(OH)-COOH (axit lactic).
naxit lactic = 45 : 90 = 0,5 mol
Theo sơ đồ nC6H10O5 = ½ naxit lactic = 0,25 mol
⟹ mtinh bột (cần dùng) = 0,25 . 162 . (100/90) . (100/80) = 56,25 gam.
Câu 33:
 Xem đáp án
Xem đáp án
Đáp án B
Phương pháp giải:
Ancol + [O] → Hỗn hợp X
BTKL → mO pư = mX - mancol → nO pư = nancol pư = nanđehit
Đánh giá số mol ancol ban đầu từ đó đánh giá được khối lượng mol của ancol ⟹ Ancol là CH3OH.
Giải chi tiết:
Ancol + [O] → Hỗn hợp X
BTKL → mO pư = mX - mancol = 6,2 - 4,6 = 1,6 gam → nO pư = 0,1 mol = nancol pư
⟹ nancol (bđ) > 0,1 mol
⟹ Mancol < 4,6 : 0,1 = 46
⟹ Ancol chỉ có thể là CH3OH.
CH3OH + [O] → HCHO + H2O
0,1 → 0,1 (mol)
HCHO → 4Ag
0,1 → 0,4 (mol)
→ mAg = 0,4.108 = 43,2 gam.
Câu 34:
Cho 500 ml dung dịch glucozơ phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được 10,8 gam Ag. Nồng độ của dung dịch glucozơ đã dùng là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Tính toán theo sơ đồ rút gọn: Glucozơ → 2Ag.
Giải chi tiết:
nAg = 10,8 : 108 = 0,1 mol
Glu → 2Ag
0,05 ← 0,1 (mol)
→ CM glucozơ = n : V = 0,05 : 0,5 = 0,1M.
Câu 35:
Cho 6,0 gam HCOOCH3 phản ứng hết với dung dịch NaOH đun nóng. Khối lượng muối HCOONa thu được là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Tính toán theo PTHH: HCOOCH3 + NaOH → HCOONa + CH3OH (đun nóng).
Giải chi tiết:
nHCOOCH3 = 6 : 60 = 0,1 mol
PTHH: HCOOCH3 + NaOH → HCOONa + CH3OH (đun nóng)
0,1 → 0,1 (mol)
→ mHCOONa = 0,1.68 = 6,8 gam.
Câu 36:
Sắp xếp các hợp chất: CH3COOH, C2H5OH và C6H5OH (phenol) theo thứ tự tăng dần tính axit. Trường hợp nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án D
Phương pháp giải:
Tính axit: Ancol < Phenol < Axit cacboxylic.
Giải chi tiết:
Tính axit: C2H5OH < C6H5OH < CH3COOH.
Câu 37:
Hỗn hợp T gồm ba este X, Y, Z mạch hở (MX < MY < MZ). Cho 48,28 gam T tác dụng vừa đủ với dung dịch chứa 0,47 mol NaOH, thu được một muối duy nhất của axit cacboxylic đơn chức và hỗn hợp Q gồm các ancol no, mạch hở, có cùng số nguyên tử cacbon trong phân tử. Đốt cháy hoàn toàn Q, thu được 13,44 lít khí CO2 (đktc) và 14,4 gam H2O. Phần trăm khối lượng của nguyên tố cacbon trong Z là
 Xem đáp án
Xem đáp án
Đáp án C
Phương pháp giải:
Q là ancol no nên: nQ = nH2O - nCO2 → Số C của ancol = nCO2 : nQ = 3
Q gồm C3H8O, C3H8O2, C3H8O3
Giả sử Q có a mol X, b mol Y và c mol Z
Nên nQ = a + b + c = n ancol (1)
Và nNaOH = nX + 2nY + 3nZ = a + 2b+ 3c (2)
Ta có:
BTKL mmuối = mQ + mNaOH - mancol (3)
Thay (1) và (2) vào (3) tính được m muối. Từ đó xác định được công thức của muối → CTPT Z → %mC(Z)
Giải chi tiết:
Đốt cháy Q có CO2: 0,6 mol và H2O: 0,8 mol → nQ = 0,8 - 0,6 = 0,2 mol
→ Q có CTTB là CnH2n+2Ox: 0,2 mol → n = 3
Q gồm C3H8O, C3H8O2, C3H8O3
Giả sử Q có a mol X, b mol Y và c mol Z
Nên nQ = a + b + c = 0,2 mol
Và nNaOH = a + 2b+ 3c = 0,47
Ta có:
mmuối = 48,28 + 0,47.40 - (60a + 76b + 92c) = 48,28 + 0,7.40 - 44 (a + b + c) -16 (a + 2b + 3c) = 50,76
→ Mmuối = 108 → Muối là C3H5COONa → Z là (C3H5COO)3C3H5
→ %mC(Z) = 60,81%
Câu 38:
Số este có công thức phân tử C4H8O2 mà khi thủy phân trong môi trường axit thì thu được axit fomic là
 Xem đáp án
Xem đáp án
Đáp án C
Các este có công thức phân tử C4H8O2 mà khi thủy phân trong môi trường axit thì thu được axit fomic là:
HCOO-CH2-CH2-CH3
HCOO-CH(CH3)-CH3
Vậy có 2 este thỏa mãn.
Câu 39:
Hỗn hợp M gồm ancol no, đơn chức X và axit cacboxylic đơn chức Y, đều mạch hở và có cùng số nguyên tử C, tổng số mol hai chất là 0,5 mol (số mol của Y lớn hơn số mol của X). Nếu đốt cháy hoàn toàn M thu được 33,6 lít CO2 (đktc) và 25,2 gam H2O. Nếu đun nóng M với H2SO4 đặc để thực hiện phản ứng este hóa với hiệu suất 80% thì số gam este thu được là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
- Tính Ctb = nC : nhh = 3
⟹ Ancol và axit đều chứa 3C
⟹ Ancol là C3H8O
- Tính Htb = nH : nhh = 5,6
Mà Hancol > 5,6 ⟹ Haxit < 5,6 ⟹ Haxit = 4 hoặc Haxit = 2.
- Xét 2 trường hợp sau và tính số mol X, Y:
+ Nếu Haxit = 4
+ Nếu Haxit = 2
Tìm trường hợp thỏa mãn nY > nX.
Giải chi tiết:
- BTNT "C" → nC = nCO2 = 33,6/22,4 = 1,5 mol
⟹ Ctb = nC : nhh = 1,5 : 0,5 = 3
⟹ Ancol và axit đều chứa 3C
⟹ Ancol là C3H8O
- BTNT "H" → nH = 2nH2O = 2.(25,2/18) = 2,8 mol
⟹ Htb = nH : nhh = 2,8 : 0,5 = 5,6
Mà Hancol > 5,6 ⟹ Haxit < 5,6 ⟹ Haxit = 4 hoặc Haxit = 2.
+ Nếu Haxit = 4 → Axit là CH2=CH-COOH
Giả sử (thỏa mãn dữ kiện nY > nX).
*Phản ứng este hóa:
PTHH: CH2=CH-COOH + C3H7OH ⇄ CH2=CH-COOC3H7 + H2O
Do nY > nX nên lượng phản ứng tính theo X.
→ neste = nX(pư) = 0,2.80% = 0,16 mol
→ meste = 0,16.114 = 18,24 gam.
+ Nếu Haxit = 2 → Axit là CH≡C-COOH
Giả sử (không thỏa mãn nY > nX).
Câu 40:
Vào mùa mưa khí hậu ẩm ướt, đặc biệt ở các vùng mưa lũ đễ phát sinh một số bệnh như ghẻ nở. Người bị bệnh khi đó được khuyên nên bôi vào các vị trí ghẻ nở một loại thuốc thông dụng là DEP. Thuốc DEP có thành phần hóa học quan trọng là đietyl phtalat:
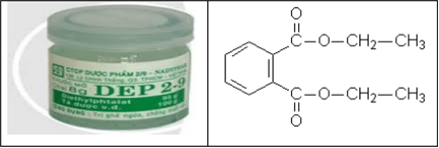
Công thức của đietyl phtalat là
 Xem đáp án
Xem đáp án
Đáp án A
Phương pháp giải:
Xác định công thức dựa vào hình vẽ.
Giải chi tiết:
Từ hình vẽ ta thấy được công thức của đietyl phtalat là C6H4(COOC2H5)2.
