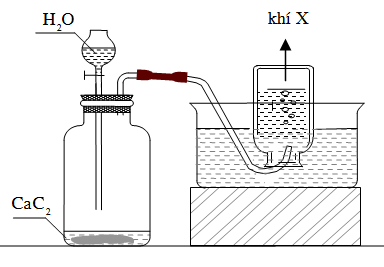
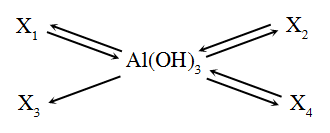
Chuyên đề ôn thi THPTQG môn Hóa Học cực hay có đáp án (Chuyên đề 3)
-
2969 lượt thi
-
40 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 1:
Cho dãy các kim loại kiềm: Na, Li, Cs, Rb. Kim loại có nhiệt độ nóng chảy thấp nhất là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 3:
Để đánh giá độ nhiễm bẩn không khí của một nhà máy, người ta tiến hành như sau: Lấy 2 lít không khí rồi dẫn qua dung dịch Pb(NO3)2 dư thì thu được chất kết tủa màu đen. Hãy cho biết hiện tượng đó chứng tỏ trong không khí đã có khí nào trong các khí sau?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 5:
Kim loại kiềm có nhiều ứng dụng quan trọng: (1) Chế tạo các hợp kim có nhiệt độ nóng chảy thấp; (2) Hợp kim Na - K dùng làm chất trao đổi nhiệt trong các lò phản ứng hạt nhân; (3) Kim loại xesi dùng làm tế bào quang điện; (4) Các kim loại Na, K dùng để điều chế các dung dịch bazơ; (5) Chế tạo hợp kim Li - Al siêu nhẹ, dùng trong kĩ thuật hàng không. Phát biểu đúng là:
 Xem đáp án
Xem đáp án
Đáp án A
Câu 6:
Cho Cu tác dụng với dung dịch hỗn hợp gồm NaNO3 và H2SO4 loãng giải phóng khí X (không màu, dễ hoá nâu trong không khí). Khí X là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 7:
Cho dãy các chất: FeO, Fe3O4, Al2O3, HCl, Fe2O3, FeCO3. Số chất trong dãy bị oxi hoá bởi dung dịch H2SO4 đặc, nóng là
 Xem đáp án
Xem đáp án
Đáp án B
Các chất bị oxi hóa là: FeO, Fe3O4, FeCO3
Câu 10:
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau :
|
Mẫu thử |
Thí nghiệm |
Hiện tượng |
|
X |
Tác dụng với Cu(OH)2 |
Hợp chất màu tím |
|
Y |
Quì tím ẩm |
Quì đổi xanh |
|
Z |
Tác dụng với dung dịch Br2 |
Dung dịch mất màu và có kết tủa trắng |
|
T |
Tác dụng với dung dịch Br2 |
Dung dịch mất màu |
Các chất X, Y, Z, T lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án D
Câu 15:
Cho chất X có công thức phân tử C4H8O2 tác dụng với dung dịch NaOH sinh ra chất Y có công thức phân tử C2H3O2Na. Công thức của X là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 17:
Các dung dịch NaCl, HCl, CH3COOH, H2SO4 có cùng nồng độ mol, dung dịch có pH nhỏ nhất là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 19:
Công thức phân tử CaCO3 tương ứng với thành phần hoá học chính của loại đá nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 20:
Cho dãy các chất: H2NCH(CH3)COOH, C6H5OH (phenol), CH3COOC2H5, C2H5OH, CH3NH3Clphenolphtalein hoá xanh phản ứng với dung dịch KOH đun nóng là
 Xem đáp án
Xem đáp án
Đáp án C
Các chất phản ứng là:
Câu 21:
Đun nóng 24 gam axit axetic với 23 gam ancol etylic (xúc tác H2SO4 đặc), thu được 26,4 gam este. Hiệu suất của phản ứng este hóa là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 22:
Khi thủy phân hoàn toàn một tetrapeptit X mạch hở chỉ thu được amino axit chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho m gam X tác dụng vừa đủ với 0,3 mol NaOH thu được 34,95 gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 23:
Một mẫu supephotphat đơn khối lượng 15,55 gam chứa 35,43% Ca(H2PO4)2 còn lại là CaSO4. Độ dinh dưỡng của loại phân trên là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 25:
Chia 0,15 mol hỗn hợp X gồm một số chất hữu cơ (trong phân tử cùng chứa C, H và O) thành ba phần bằng nhau. Đốt cháy phần một bằng một lượng oxi vừa đủ rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư thu được 5 gam kết tủa. Phần hai tác dụng với một lượng dư dung dịch AgNO3 trong NH3 thu được 8,64 gam Ag. Phần ba tác dụng với một lượng Na vừa đủ thu được 0,448 lít H2 (đktc). Các phản ứng xảy ra hoàn toàn. Khối lượng của 0,15 mol hỗn hợp X là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 26:
Đun nóng 0,1 mol este đơn chức X với 135 ml dung dịch NaOH 1M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được ancol etylic và 9,6 gam chất rắn khan. Công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 27:
Sục khí H2S cho tới dư vào 100 ml dung dịch hỗn hợp gồm FeCl3 0,2M và CuCl2 0,2M; phản ứng xong thu được a gam kết tủa. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 28:
Cho 3,35 gam hỗn hợp X gồm 2 ancol no, đơn chức kế tiếp nhau trong dãy đồng đẳng phản ứng với Na dư, thu được 0,56 lít H2 (đktc). Công thức cấu tạo thu gọn của 2 ancol đó là:
 Xem đáp án
Xem đáp án
Đáp án C
Câu 29:
Hòa tan hoàn toàn m gam hỗn hợp X gồm K, K2O, KOH, KHCO3, K2CO3 trong lượng vừa đủ dung dịch HCl 14,6%, thu được 6,72 lít (đktc) hỗn hợp gồm hai khí có tỉ khối so với H2 là 15 và dung dịch Y có nồng độ 25,0841%. Cô cạn dung dịch Y, thu được 59,6 gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 30:
X là chất hữu cơ có công thức C7H6O3. Biết X tác dụng với NaOH theo tỉ lệ mol 1 : 3. Số công thức cấu tạo phù hợp với X là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 31:
Thuỷ phân 324 gam tinh bột với hiệu suất của phản ứng 75%, khối lượng glucozơ thu được là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 32:
Cho từ từ chất X vào dung dịch Y, sự biến thiên lượng kết tủa Z tạo thành trong thí nghiệm được biểu diễn trên đồ thị sau:
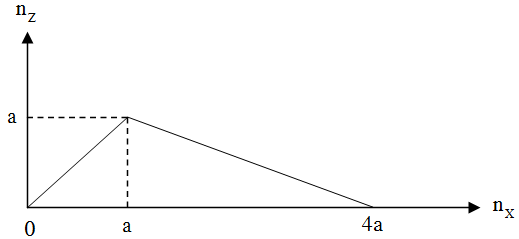
Thí nghiệm nào sau đây ứng với thí nghiệm trên?
 Xem đáp án
Xem đáp án
Đáp án D
Dựa vào đồ thị, ta thấy: Khi cho từ từ X vào dung dịch Y, phản ứng thứ nhất tạo kết tủa Z và lượng kết tăng dần đến cực đại là a mol, phản ứng này cần dùng a mol X. Phản ứng thứ hai hòa tan từ từ kết tủa Z đến hết, phản ứng này cần 3a mol chất X.
Suy ra: Đây là thí nghiệm cho từ từ đến dư dung dịch HCl vào dung dịch NaAlO2.
Phương trình phản ứng:
Câu 33:
Nhỏ từ từ từng giọt đến hết 30 ml dung dịch HCl 1M vào 100 ml dung dịch chứa Na2CO3 0,2M và NaHCO3 0,2M. Sau khi phản ứng kết thúc, thể tích (đktc) khí CO2 thu được là
 Xem đáp án
Xem đáp án
Đáp án D
+ Bản chất phản ứng (1) xảy ra hoàn toàn sau đó đến (2):
+ Sử dụng công thức trên suy ra:
Câu 34:
Dãy gồm các chất được sắp xếp theo thứ tự tăng dần lực bazơ từ trái sang phải là
 Xem đáp án
Xem đáp án
Đáp án B
Tính bazơ của amin phụ thuộc vào mật độ electron trên N của amin hoặc phân tử NH3. Mật độ electron trên nitơ càng lớn thì tính bazơ càng mạnh và ngược lại.
Mật độ electron trên N lại phụ thuộc vào gốc hiđrocacbon liên kết với chức amin. Nếu gốc hiđrocacbon là gốc đẩy electron thì làm cho mật độ electron trên N tăng và ngược lại.
Suy ra : Dãy gồm các chất được sắp xếp theo thứ tự tăng dần lực bazơ là phenylamin, amoniac, etylamin.
Câu 35:
Nung nóng một hỗn hợp gồm CaCO3 và MgO tới khối lượng không đổi, thì số gam chất rắn còn lại chỉ bằng 2/3 số gam hỗn hợp trước khi nung. Vậy trong hỗn hợp ban đầu thì CaCO3 chiếm phần trăm theo khối lượng là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 36:
Cho a mol sắt tác dụng với a mol khí clo, thu được hỗn hợp rắn X. Cho X vào nước, thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y không tác dụng với chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án C
Bản chất phản ứng:
Câu 37:
Cho 7,65 gam hỗn hợp X gồm Al và Al2O3 (trong đó Al chiếm 60% khối lượng) tan hoàn toàn trong dung dịch Y gồm H2SO4 và NaNO3, thu được dung dịch Z chỉ chứa 3 muối trung hòa và m gam hỗn hợp khí T (trong T có 0,015 mol H2). Cho dung dịch BaCl2 dư vào Z đến khi các phản ứng xảy ra hoàn toàn, thu được 93,2 gam kết tủa. Còn nếu cho Z phản ứng với NaOH thì lượng NaOH phản ứng tối đa là 0,935 mol. Giá trị của m gần giá trị nào nhất sau đây?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 38:
Lấy m gam Mg tác dụng với 500 ml dung dịch AgNO3 0,2M và Fe(NO3)3 2M. Kết thúc phản ứng thu được (m+4) gam kim loại. Gọi a là tổng các giá trị m thỏa mãn bài toán trên, giá trị của a là?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 39:
Hỗn hợp X gồm 2 este đơn chức (đều tạo bởi axit no, đều không có phản ứng cộng với brom trong nước) là đồng phân của nhau. 0,2 mol X phản ứng được với tối đa 0,3 mol NaOH, khi đó tổng khối lượng sản phẩm hữu cơ thu được là 37,4 gam. số cặp este tối đa có thể có trong hỗn hợp X là
 Xem đáp án
Xem đáp án
Đáp án D
Do axit tạo este là axit no nên X có 4 cặp chất thỏa mãn. Còn nếu không có điều kiện này thì số cặp đồng phân sẽ nhiều hơn, vì este có thể tạo bởi axit thơm.
Nhóm HCOO– có khả năng phản ứng với dung dịch brom trong nước nhưng đó là phản ứng oxi hóa – khử, không phải là phản ứng cộng.
Câu 40:
Tripeptit X mạch hở có công thức phân tử C10H19O4N3. Thủy phân hoàn toàn một lượng X trong dung dịch 400,0 ml dung dịch NaOH 2M (lấy dư), đun nóng, thu được dung dịch Y chứa 77,4 gam chất tan. Cho dung dịch Y tác dụng với lượng dư dung dịch HCl, sau đó cô cạn cẩn thận, thu được m gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D