Chuyên đề ôn thi THPTQG môn Hóa Học cực hay có đáp án (Chuyên đề 8)
-
2998 lượt thi
-
40 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 3:
Một chất có chứa nguyên tố oxi, dùng để làm sạch nước và có tác dụng bảo vệ các sinh vật trên Trái Đất không bị bức xạ cực tím. Chất này là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 4:
Kim loại X là kim loại cứng nhất, được sử dụng để mạ các dụng cụ kim loại, chế tạo các loại thép chống gỉ, không gỉ…Kim loại X là?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 5:
Nhôm thể hiện tính chất nào sau đây?
(1) Nhôm có cấu tạo mạng tinh thể lập phương tâm diện.
(2) Là kim loại màu trắng bạc, mềm, dễ kéo sợi và dát mỏng.
(3) Nhôm dẫn điện và dẫn nhiệt tốt, tốt hơn các kim loại Fe và Cu.
(4) Nhôm là kim loại nhẹ, nóng chảy ở nhiệt độ 660oC.
(5) Nhôm là nguyên tố s.
 Xem đáp án
Xem đáp án
Đáp án D
Câu 6:
Cho dung dịch AgNO3 tác dụng với dung dịch chứa chất X thấy tạo kết tủa T màu vàng. Cho kết tủa T tác dụng với dung dịch HNO3 dư thấy kết tủa tan. Chất X là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 7:
Cho dãy các chất: AgNO3, CuS, FeO, Fe, Cr(OH)3, Fe(NO3)2. Số chất trong dãy phản ứng được với dung dịch HCl là
 Xem đáp án
Xem đáp án
Đáp án D
Các chất là: AgNO3, FeO, Fe, Cr(OH)3, Fe(NO3)2
Câu 10:
Tiến hành thí nghiệm với các chất X, Y, Z, T, kết quả được trình bày trong bảng dưới đây:
|
|
X |
Y |
Z |
T |
|
Nước brom |
Không mất màu |
Mất màu |
Không mất màu |
Không mất màu |
|
Nước |
Tách lớp |
Tách lớp |
Dung dịch đồng nhất |
Dung dịch đồng nhất |
|
Dung dịch
|
Không có kết tủa |
Không có kết tủa |
Có kết tủa |
Không có kết tủa |
X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 11:
Nhúng 2 đũa thuỷ tinh vào 2 bình đựng dung dịch HCl đặc và NH3 đặc. Sau đó đưa 2 đũa lại gần nhau thì thấy xuất hiện
 Xem đáp án
Xem đáp án
Đáp án A
Câu 13:
Chất nào sau đây có thể sử dụng để loại H2O ra khỏi ancol etylic 96o để thu được ancol etylic khan ?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 15:
Cho các este : etyl fomat (1), vinyl axetat (2), triolein (3), metyl acrylat (4), phenyl axetat (5). Dãy gồm các este đều phản ứng được với dung dịch NaOH (đun nóng) sinh ra ancol là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 16:
Cho phản ứng của Fe với oxi như hình vẽ sau. Vai trò của lớp nước ở đáy bình là
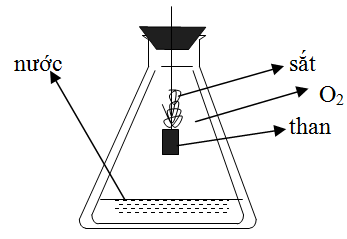
 Xem đáp án
Xem đáp án
Đáp án C
Câu 17:
Trong dung dịch H3PO4 (bỏ qua sự phân li của H2O) chứa bao nhiêu loại ion?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 19:
Tủ lạnh dùng lâu sẽ có mùi hôi, có thể cho vào tủ lạnh một ít cục than hoa để khử mùi hôi này. Đó là vì:
 Xem đáp án
Xem đáp án
Đáp án B
Câu 21:
Hỗn hợp X gồm propin và ankin A có tỉ lệ mol 1 : 1. Lấy 0,3 mol X tác dụng với dung dịch AgNO3/NH3 dư, thu được 46,2 gam kết tủa. Tên của A là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 22:
Đốt cháy hoàn toàn một amin đơn chức, mạch hở X bằng một lượng không khí (chứa 20% thể tích O2, còn lại là N2) vừa đủ, thu được 0,08 mol CO2; 0,1 mol H2O và 0,54 mol N2. Khẳng định nào sau đây là đúng?
 Xem đáp án
Xem đáp án
Đáp án A
+ Theo BTNT O và tính chất của không khí ta có:
+ X là , X chỉ có 1 đồng phân:
Câu 23:
Cho dung dịch muối X đến dư vào dung dịch muối Y, thu được kết tủa Z. Cho Z vào dung dịch HNO3 (loãng, dư), thu được chất rắn T và khí không màu hóa nâu trong không khí. X và Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
X và Y lần lượt là AgNO3 và FeCl2. Phương trình phản ứng:
Câu 24:
Có 100 ml dung dịch X gồm: NH4+, K+, CO32–, SO42–. Chia dung dịch X làm 2 phần bằng nhau. Phần 1 cho tác dụng với dung dịch Ba(OH)2 dư, thu được 6,72 lít (đktc) khí NH3 và 43 gam kết tủa. Phần 2 tác dụng với lượng dư dung dịch HCl, thu được 2,24 lít (đktc) khí CO2. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
+ Bản chất phản ứng:
Câu 25:
Nung nóng 19,52 gam hỗn hợp gồm Al và Cr2O3 trong điều kiện không có không khí, sau một thời gian, thu được hỗn hợp rắn X. Hòa tan hết X cần dùng 600 ml dung dịch HCl 1,6M, thu được 0,18 mol khí H2 và dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được x gam kết tủa. Giá trị của x là
 Xem đáp án
Xem đáp án
Đáp án B
+ Sơ đồ phản ứng:
Câu 26:
Cho hỗn hợp X gồm 2 anđehit no, đơn chức. Lấy 0,25 mol X cho phản ứng với dung dịch AgNO3/NH3 dư, thu được 86,4 gam kết tủa, khối lượng dung dịch sau phản ứng giảm 76,1 gam. Công thức của hai anđehit là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 27:
Cho 0,1 mol este tạo bởi axit 2 lần axit hai chức và ancol một ancol đơn chức tác dụng hoàn toàn với dung dịch NaOH, thu được 6,4 gam ancol và một lượng muối có khối lượng nhiều hơn 13,56% khối lượng este. Công thức cấu tạo của este là :
 Xem đáp án
Xem đáp án
Đáp án C
Câu 28:
Có các chất sau: Na2O, NaCl, Na2CO3, NaHCO3, Na2SO4. Có bao nhiêu chất mà bằng một phản ứng có thể tạo ra NaOH?
 Xem đáp án
Xem đáp án
Đáp án B
Có 5 chất điều chế trực tiếp được NaOH. Phương trình phản ứng:
Câu 29:
Khối lượng saccarozơ thu được từ một tấn nước mía chứa 13% saccarozơ với hiệu suất thu hồi đạt 80% là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 30:
Sục từ từ khí CO2 vào dung dịch chứa Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau (số liệu các chất tính theo đơn vị mol):
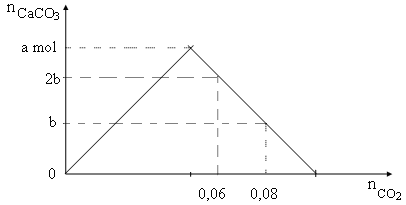
Tỉ lệ a : b là
 Xem đáp án
Xem đáp án
Đáp án B
+ Dựa vào bản chất phản ứng ta có đồ thị:
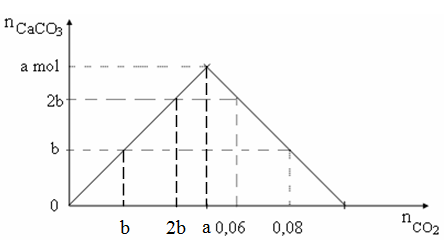
+ Căn cứ vào tính đối xứng của đồ thị ta có:
Câu 31:
Cho 4,05 gam bột nhôm vào 100 ml dung dịch Fe(NO3)3 3M. Sau khi phản ứng xảy ra hoàn toàn, thu được m gam kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 32:
Cho 200 ml dung dịch Ba(OH)2 0,1M vào 300 ml dung dịch NaHCO3 0,1M, thu được dung dịch X và kết tủa Y. Cho từ từ dung dịch HCl 0,25M vào X đến khi bắt đầu có khí thoát ra thì hết V ml. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 33:
Methadone là thuốc dùng trong cai nghiện ma túy, nó thực chất cũng là 1 loại chất gây nghiện nhưng “nhẹ” hơn các loại ma túy thông thường và dễ kiểm soát hơn. Công thức cấu tạo của nó như sau:
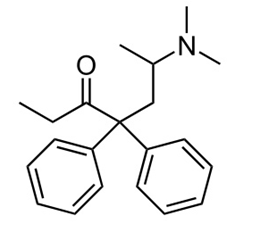
Công thức phân tử của methadone là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 34:
Cho sơ đồ phản ứng:
Công thức cấu tạo của X thỏa mãn sơ đồ đã cho là
 Xem đáp án
Xem đáp án
Đáp án A
+ Dễ thấy C2H3O2Na là CH3COONa. Suy ra: Z là CH3COONH4, Y là CH3CHO, X là CH3COOCH=CH2.
+ Phương trình phản ứng :
Câu 35:
Cho hỗn hợp X gồm một tetrapeptit và một tripeptit. Để thủy phân hoàn toàn 50,36 gam X cần dung dịch chứa 0,76 mol NaOH, sau phản ứng hoàn toàn cô cạn thu được 76,8 gam hỗn hợp muối chỉ gồm a mol muối của glyxin và b mol muối của alanin. Mặt khác đốt cháy hoàn toàn 0,11 mol X bằng O2 dư thu được m gam CO2. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 36:
X, Y là 2 hợp chất hữu cơ no, mạch hở, trong phân tử chỉ chứa một loại nhóm chức; X, Y khác chức hóa học (MX < MY). Đốt cháy hoàn toàn a mol X cũng như Y đều thu được x mol CO2 và y mol H2O với x = y + a. Lấy 0,25 mol hỗn hợp E chứa X, Y tác dụng với AgNO3/NH3 dư thu được 86,4 gam Ag. Mặt khác, đun nóng 0,25 mol E với dung dịch NaOH dư thì sản phẩm thu được chứa 15 gam hỗn hợp 2 muối của 2 axit hữu cơ no, đơn chức và 7,6 gam một ancol Z. Đốt cháy hoàn toàn 14,25 gam X cần dùng V lít O2 (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 37:
Hòa tan hết 10,62 gam hỗn hợp gồm Fe, Zn vào 800 ml dung dịch hỗn hợp X gồm NaNO3 0,45M và H2SO4 1M, thu được dung dịch Y và 3,584 lít khí NO (duy nhất). Y hòa tan được tối đa m gam bột sắt và thu được V lít khí. Các khí đo ở đktc và NO là sản phẩm khử duy nhất của N+5 trong các thí nghiệm trên. Giá trị của m và V lần lượt là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 38:
Cho 8,654 gam hỗn hợp X gồm khí Cl2 và O2 tác dụng vừa đủ với 0,396 mol hỗn hợp Y gồm Mg, Zn, Al, thu được 23,246 gam hỗn hợp Z gồm muối clorua và oxit của 3 kim loại. Cho Z phản ứng vừa đủ với V ml dung dịch HCl 1M, thu được dung dịch T. Cho từ từ dung dịch Ba(OH)2 2M vào T đến khi lượng kết tủa thu được không thay đổi về khối lượng thì cần vừa đủ 286 ml. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 39:
Hòa tan hoàn toàn 29,6 gam hỗn hợp H gồm FeS2 và CuO vào 500 gam dung dịch HNO3 C% (dùng dư 10% so với lượng phản ứng), cô cạn dung dịch sau phản ứng thu được 56,12 gam hỗn hợp muối khan. Biết trong quá trình xảy ra phản ứng chỉ có NO2 là sản phẩm khử duy nhất. Giá trị C gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 40:
X, Y, Z là 3 este đều đơn chức, mạch hở (trong đó Y và Z không no chứa một liên kết C = C và có tồn tại đồng phân hình học). Đốt cháy 21,62 gam hỗn hợp E chứa X, Y, Z với oxi vừa đủ, sản phẩm cháy dẫn qua dung dịch Ca(OH)2 dư thấy khối lượng dung dịch giảm 34,5 gam so với trước phản ứng. Mặt khác, đun nóng 21,62 gam E với 300 ml dung dịch NaOH 1M (vừa đủ), thu được hỗn hợp F chỉ chứa 2 muối và hỗn hợp gồm 2 ancol kế tiếp thuộc cùng dãy đồng đẳng. Khối lượng của muối có khối lượng phân tử lớn trong hỗn hợp F là
 Xem đáp án
Xem đáp án
Đáp án B
