Chuyên đề ôn thi THPTQG môn Hóa Học cực hay có đáp án (Chuyên đề 5)
-
2961 lượt thi
-
40 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 4:
Cho Al lần lượt vào các dung dịch: H2SO4 loãng, HNO3 (đậm đặc, to), Ba(OH)2, HNO3 loãng, H2SO4 đặc, thấy sinh ra khí X có tỉ khối so với O2 nhỏ hơn 0,9. Số dung dịch phù hợp là
 Xem đáp án
Xem đáp án
Đáp án B
Các dung dịch là: H2SO4 loãng, Ba(OH)2, HNO3 loãng
Câu 5:
Trong tự nhiên, caxi sunphat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 6:
Chất X tan trong nước và tác dụng được với dung dịch H2SO4 loãng. Chất X là chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 7:
Cho dãy các chất: CaCO3, K, Mg, Cu, Al, PbS. Số chất tác dụng với dung dịch HCl là?
 Xem đáp án
Xem đáp án
Đáp án B
Các chất tác dụng với dung dịch HCl là: CaCO3, K, Mg, Al
Câu 8:
Hiện tượng các chất có cấu tạo và tính chất hoá học tương tự nhau, phân tử hơn kém nhau một hay nhiều nhóm metylen (–CH2–) được gọi là hiện tượng
 Xem đáp án
Xem đáp án
Đáp án C
Câu 10:
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
|
Mẫu thử |
Thí nghiệm |
Hiện tượng |
|
X |
Tác dụng với Cu(OH)2 trong môi trường kiềm |
Có màu tím |
|
Y |
Ðun nóng với dung dịch NaOH (loãng, dư), để nguội. Thêm tiếp vài giọt dung dịch CuSO4 |
Tạo dung dịch màu xanh lam |
|
Z |
Ðun nóng với dung dịch NaOH loãng (vừa đủ). Thêm tiếp dung dịch AgNO3 trong NH3, đun nóng |
Tạo kết tủa Ag |
|
T |
Tác dụng với dung dịch I2 loãng |
Có màu xanh tím |
Các chất X, Y, Z, T lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án A
Câu 15:
Thuỷ phân phenyl axetat trong dung dịch NaOH dư thu được các sản phẩm hữu cơ là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 16:
Cho phản ứng:
Các hệ số a, b, c, d, e là những số nguyên, đơn giản nhất thì tổng (a+b) bằng
 Xem đáp án
Xem đáp án
Đáp án B
Câu 19:
Chất nào sau đây không phải là nguyên liệu của công nghiệp sản xuất xi măng?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 20:
Cho dãy các dung dịch: Glucozơ, saccarozơ, etanol, glixerol. Số dung dịch phản ứng với Cu(OH)2 ở nhiệt độ thường tạo dung dịch có màu xanh lam là
 Xem đáp án
Xem đáp án
Đáp án A
Các dung dịch phản ứng là: Glucozơ, saccarozơ, glixerol
Câu 21:
Cho 3,38 gam hỗn hợp X gồm CH3OH, CH3COOH, C6H5OH tác dụng vừa đủ với Na, thấy thoát ra 672 ml H2 (đktc) và thu được hỗn hợp chất rắn X1 có khối lượng là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 22:
X là tetrapeptit Gly-Val-Ala-Val, Y là tripeptit Val-Ala-Val. Đun nóng 14,055 gam hỗn hợp X và Y bằng dung dịch NaOH vừa đủ, sau khi phản ứng kết thúc thu được dung dịch Z. Cô cạn dung dịch Z thu được 19,445 gam muối. Phần trăm khối lượng của X trong hỗn hợp là
 Xem đáp án
Xem đáp án
Đáp án A
+Bản chất phản ứng:
Câu 23:
Một loại phân supephotphat kép có chứa 69,62% muối canxi đihiđrophotphat, còn lại gồm các chất không chứa photpho. Độ dinh dưỡng của loại phân lân này là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 24:
Có 5 hỗn hợp, mỗi hỗn hợp gồm 2 chất rắn có số mol bằng nhau: Na2O và Al2O3; Cu và Fe2(SO4)3; KHSO4 và KHCO3; BaCl2 và CuSO4; Fe(NO3)2 và AgNO3. Số hỗn hợp có thể tan hoàn toàn trong nước (dư) chỉ tạo ra các chất tan trong nước là
 Xem đáp án
Xem đáp án
Đáp án B
+ Hai hỗn hợp thỏa mãn điều kiện đề bài là Na2O và Al2O3; Cu và Fe2(SO4)3. Phương trình phản ứng:
|
|
|
+ Hỗn hợp KHSO4 và KHCO3 xảy ra phản ứng tạo khí; hỗn hợp BaCl2 và CuSO4; Fe(NO3)2 và AgNO3 xảy ra phản ứng tạo kết tủa.
Câu 25:
Hỗn hợp T gồm X, Y, Z (58 < MX < MY < MZ < 78), là hợp chất hữu cơ tạp chức, phân tử chỉ chứa C, H và O có các tính chất sau:
- X, Y, Z đều tác dụng được với Na.
- Y, Z tác dụng được với NaHCO3.
- X, Y đều có phản ứng tráng bạc.
Nếu đốt cháy hết 0,25 mol hỗn hợp T thì thu được m gam chất CO2, m gần nhất với giá trị:
 Xem đáp án
Xem đáp án
Đáp án B
+ Từ giả thiết suy ra: T gồm
Câu 26:
Thủy phân hoàn toàn 16,12 gam tripanmitin ((C15H31COO)3C3H5) cần vừa đủ V ml dung dịch NaOH 0,5M. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 27:
Oxi hóa hoàn toàn 0,728 gam bột Fe, thu được 1,016 gam hỗn hợp hai oxit sắt (hỗn hợp X). Lấy hỗn hợp X này trộn với 5,4 gam bột Al rồi tiến hành phản ứng nhiệt nhôm (hiệu suất 100%). Hòa tan hỗn hợp thu được sau phản ứng bằng dung dịch HCl dư. Thể tích khí bay ra (đktc) là
 Xem đáp án
Xem đáp án
+ Sơ đồ phản ứng:
Câu 28:
Phenolphtalein X có tỉ lệ khối lượng mC : mH : mO = 60 : 3,5 : 16. Biết khối lượng phân tử của X nằm trong 300 đến 320u. Số nguyên tử cacbon của X là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 29:
Hòa tan hết 4,667 gam hỗn hợp Na, K, Ba và ZnO (trong đó oxi chiếm 5,14% khối lượng) vào nước, thu được dung dịch X và 0,032 mol khí H2. Cho 88 ml dung dịch HCl 1M vào X đến khi các phản ứng kết thúc, thu được m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 30:
Chất X mạch hở có công thức phân tử C4H8O2, X tham gia phản ứng tráng bạc và tác dụng với Na giải phóng khí H2. Có bao nhiêu công thức cấu tạo của X thỏa mãn các tính chất trên
 Xem đáp án
Xem đáp án
Đáp án C
Theo giả thiết suy ra X là hợp chất tạp chức vừa có nhóm HO vừa có nhóm CHO. X có 5 đồng phân thỏa mãn:
Câu 31:
Cho m gam glucozơ phản ứng hoàn với lượng dư dung dịch AgNO3/NH3, đun nóng, thu được 21,6 gam Ag. Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 32:
Cho từ từ chất X vào dung dịch Y, sự biến thiên lượng kết tủa Z tạo thành trong thí nghiệm được biểu diễn trên đồ thị sau:
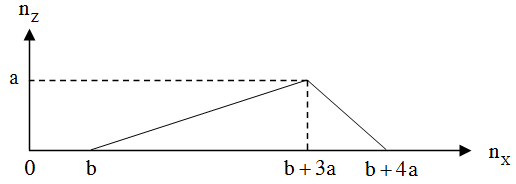
Thí nghiệm nào sau đây ứng với thí nghiệm trên?
 Xem đáp án
Xem đáp án
Đáp án C
Dựa vào đồ thị, ta thấy: Khi cho từ từ X vào dung dịch Y, phản ứng thứ nhất không tạo ra kết tủa, phản ứng này cần dùng b mol X. Phản ứng thứ hai bắt đầu tạo kết tủa Z và tăng dần đến cực đại là a mol, phản ứng này cần 3a mol X. Cuối cùng kết tủa Z bị hòa tan từ từ đến hết, phản ứng này cần a mol chất X.
Suy ra: Đây là thí nghiệm cho từ từ đến dư dung dịch NaOH vào dung dịch hỗn hợp gồm HCl và Al(NO3)3.
Phương trình phản ứng:
Câu 33:
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al, Fe vào dung dịch H2SO4 loãng dư, thu được 10,08 lít khí (đkc). Biết Fe chiếm 60,87% về khối lượng. Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 34:
Cho chất hữu cơ X có công thức phân tử C2H8O3N2 tác dụng với dung dịch NaOH, thu được chất hữu cơ đơn chức Y và các chất vô cơ. Khối lượng phân tử (theo đvC) của Y là
 Xem đáp án
Xem đáp án
Đáp án C
C2H8N2O3 (X) tác dụng với dung dịch NaOH thu được chất hữu cơ Y đơn chức, chứng tỏ X là muối amoni tạo bởi NH3 hoặc amin đơn chức. Như vậy, gốc axit trong X có 1 nguyên tử N và 3 nguyên tử O, đó là gốc ![]() . Suy ra X là C2H5NH3NO3 (etylamoni nitrat) hoặc (CH3)2NH2NO3 (đimetylamoni nitrat); Y là C2H5NH2 (etyl amin) hoặc (CH3)2NH2 (đimetyl amin), có khối lượng phân tử là 45 đvC.
. Suy ra X là C2H5NH3NO3 (etylamoni nitrat) hoặc (CH3)2NH2NO3 (đimetylamoni nitrat); Y là C2H5NH2 (etyl amin) hoặc (CH3)2NH2 (đimetyl amin), có khối lượng phân tử là 45 đvC.
Phương trình phản ứng:
Câu 35:
Sục 3,36 lít khí CO2 (đktc) vào 200 ml dung dịch NaOH 1M. Tổng khối lượng muối thu được sau phản ứng là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 36:
Cho dãy biến hóa sau:
R có thể là kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án C
Dựa vào (4) ta thấy R(OH)3 có tính lưỡng tính nên R là Al hoặc Cr. Dựa vào (1) ta thấy R không thể là Al. Vậy R là Cr.
Câu 37:
Hòa tan 11,25 gam hỗn hợp Na, K, Na2O, K2O vào nước dư, thu được 2,8 lít khí và dung dịch X trong đó có chứa 8 gam NaOH. Dẫn V lít CO2 vào dung dịch X được dung dịch Y. Cho từ từ 280 ml dung dịch HCl 1M vào dung dịch Y thấy thoát ra 4,48 lít khí CO2. Các chất khí đều đo ở đktc. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 38:
Hòa tan hoàn toàn m gam hỗn hợp X gồm Al và Al2O3 trong 200,0 ml dung dịch NaOH 2M, thu được dung dịch Y và 3,36 lít khí H2 (đktc). Thêm 300,0 ml hoặc 700,0 ml dung dịch HCl yM vào dung dịch Y đều thu được cùng một lượng kết tủa có khối lượng m gam. Giá trị gần nhất của m là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 39:
Đốt cháy m gam este etyl axetat, hấp thụ hết sản phẩm vào 200 gam dung dịch Ba(OH)2 6,84% sau đó lọc được 194,38 gam dung dịch Ba(HCO3)2. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 40:
Cho 16,5 gam chất A có công thức phân tử là C2H10O3N2 vào 200 gam dung dịch NaOH 8%. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch B và khí C. Tổng nồng độ phần trăm các chất có trong B gần nhất với giá trị
 Xem đáp án
Xem đáp án
Đáp án B
Suy ra A là muối amoni.
+ Trong A có 3O nên gốc axit cảu A là hoặc hoặc
- Nếu gốc axit thì gốc amoni là (loại).
- Nếu gốc axit là thì gốc amoni là (loại).
- Nếu gốc axit là thì 2 gốc amoni là
+ Vậy A là
+ Phương trình phản ứng:
+ Dung dịch sau phản ứng chứa: