Chuyên đề ôn thi THPTQG môn Hóa Học cực hay có đáp án (Chuyên đề 9)
-
2999 lượt thi
-
40 câu hỏi
-
30 phút
Danh sách câu hỏi
Câu 3:
Trong thành phần của khí than ướt và khí than khô (khí lò gas) đều có khí X. X không màu, không mùi, rất độc; X có tính khử mạnh và được sử dụng trong quá trình luyện gang. X là khí nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 4:
Trong thực tế, không sử dụng cách nào sau đây để bảo vệ kim loại sắt khỏi bị ăn mòn?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 6:
Trong số các nguồn năng lượng sau đây, nhóm các nguồn năng lượng nào được coi là năng lượng sạch?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 7:
Cho từ từ đến dư dung dịch NaOH loãng vào mỗi dung dịch sau: NaHCO3, Ba(HCO3)2, FeCl3, CuCl2, AlCl3, FeSO4. Sau khi các phản ứng xảy ra hoàn toàn, số trường hợp thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án A
Các trường hợp xảy ra kết tủa là: Ba(HCO3)2, FeCl3, CuCl2, FeSO4
Câu 9:
Khi bị ong đốt, để giảm đau, giảm sưng, kinh nghiệm dân gian thường dùng chất nào sau đây để bôi trực tiếp lên vết thương?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 10:
Tiến hành thí nghiệm với các chất X, Y, Z, T. Kết quả được ghi ở bảng sau:
|
Mẫu |
Thí nghiệm |
Hiện tượng |
|
X |
Tác dụng với Cu(OH)2 trong môi trường kiềm |
Có màu xanh lam |
|
Đun nóng với dung dịch H2SO4 loãng. Thêm tiếp dung dịch AgNO3 trong NH3, đun nóng |
Tạo kết tủa Ag |
|
|
Y |
Đun nóng với dung dịch NaOH (loãng, dư), để nguội. Thêm tiếp vài giọt dung dịch CuSO4 |
Tạo dung dịch màu xanh lam |
|
Z |
Tác dụng với quỳ tím |
Quỳ tím chuyển màu xanh |
|
T |
Tác dụng với nước Brom |
Có kết tủa trắng |
Các chất X, Y, Z, T lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án C
Câu 11:
Để phòng nhiễm độc CO, là khí không màu, không mùi, rất độc người ta dùng mặt nạ phòng độc có chứa
 Xem đáp án
Xem đáp án
Đáp án D
Câu 15:
Cho các chất có công thức cấu tạo sau đây:
(1) CH3CH2COOCH3; (2) CH3OOCCH3;
(3) HCOOC2H5; (4) CH3COC2H5.
Chất không thuộc loại este là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 17:
Trong các cặp chất cho dưới đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 19:
Cho hình vẽ mô tả thí nghiệm tạo “khói trắng” từ hai dung dịch X và Y:
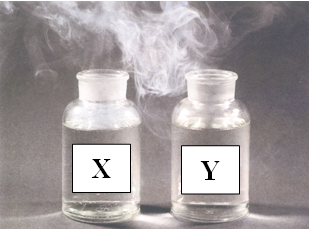
Biết mỗi dung dịch chỉ chứa một chất tan duy nhất. X, Y không phải cặp chất nào dưới đây?
 Xem đáp án
Xem đáp án
Đáp án D
Các phản ứng tạo ra “khói trắng”:
Câu 20:
Cho dãy gồm các chất: metyl metacrylat; triolein; saccarozơ; xenlulozơ; glyxylalanin; tơ nilon-6,6. Số chất trong dãy bị thủy phân khi đun nóng trong môi trường axit là
 Xem đáp án
Xem đáp án
Đáp án B
Các chất là: metyl metacrylat; triolein; saccarozơ; xenlulozơ; glyxylalanin; tơ nilon-6,6
Câu 21:
Hỗn hợp X gồm C4H4, C4H2, C4H6, C4H8 và C4H10. Tỉ khối của X so với H2 là 27. Đốt cháy hoàn toàn X cần dùng vừa đủ V lít O2 (đktc), thu được CO2 và 0,03 mol H2O. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 22:
Cho hỗn hợp 2 amino axit no chứa 1 chức –COOH và 1 chức –NH2 tác dụng với 110 ml dung dịch HCl 2M, thu được dung dịch X. Để tác dụng hết với các chất trong X, cần dùng 140 ml dung dịch KOH 3M. Tổng số mol 2 amino axit là
 Xem đáp án
Xem đáp án
Đáp án C
+ Bản chất phản ứng:
Câu 23:
Thuốc thử dùng để phân biệt các dung dịch riêng biệt, mất nhãn: NaCl, HCl, NaHSO4, Na2CO3 là
 Xem đáp án
Xem đáp án
Đáp án D
+ Thuốc thử nhận biết 4 dung dịch NaCl, HCl, NaHSO4, Na2CO3 là BaCl2.
|
thuốc thử |
NaCl |
HCl |
NaHSO4 |
Na2CO3 |
|
BaCl2 |
không tạo kết tủa |
không tạo kết tủa |
tạo kết tủa |
tạo kết tủa |
+ Giờ ta chia 4 dung dịch ban đầu thành 2 nhóm: (1) không tạo kết tủa; (2) tạo kết tủa.
+ Lấy một trong hai dung dịch ở nhóm (1) cho phản ứng với nhóm (2).
- Nếu không có hiện tượng gì xảy ra thì dung dịch ở nhóm (1) là NaCl, dung dịch còn lại là HCl. Cho HCl vào 2 dung dịch ở nhóm (2), nếu không có hiện tượng gì thì đó là NaHSO4, có khí bay ra là Na2CO3.
- Nếu một mẫu giải phóng khí thì dung dịch ở nhóm (1) là HCl, dung dịch còn lại là NaCl; dung dịch ở nhóm (2) là Na2CO3, dung dịch còn lại là NaHSO4.
Câu 24:
Dung dịch X chứa 0,12 mol Na+; x mol ; 0,12 mol và 0,05 mol . Cho 300 ml dung dịch Ba(OH)2 0,1M vào X đến khi các phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa, thu được dung dịch Y. Cô cạn Y, thu được m gam chất rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 25:
Cho m gam Fe vào bình đựng dung dịch H2SO4 và HNO3, thu được dung dịch X và 1,12 lít khí NO. Thêm tiếp H2SO4 dư vào bình, thu được 0,448 lít NO và dung dịch Y. Trong cả 2 trường hợp đều có NO là sản phẩm khử duy nhất ở kiện tiêu chuẩn. Dung dịch Y hòa tan vừa hết 2,08 gam Cu không tạo sản phẩm khử N+5. Các phản ứng đều hoàn toàn. Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án A
+ Bản chất phản ứng:
Câu 26:
Hòa tan m gam ancol etylic (d = 0,8 g/ml) vào 108 ml nước (D = 1 g/ml) tạo thành dung dịch X. Cho X tác dụng với Na dư, thu được 85,12 lít (đktc) khí H2. Dung dịch X có độ ancol bằng
 Xem đáp án
Xem đáp án
Đáp án A
+ Bản chất phản ứng của dung dịch ancol với Na:
Câu 27:
Đốt cháy hoàn toàn a gam triglixerit X cần vừa đủ 3,26 mol O2, thu được 2,28 mol CO2 và 39,6 gam H2O. Mặt khác, thủy phân hoàn toàn a gam X trong dung dịch NaOH, đun nóng, thu được dung dịch chứa b gam muối. Giá trị của b là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 28:
Điện phân dung dịch gồm NaCl và HCl (điện cực trơ, màng ngăn xốp). Trong quá trình điện phân, so với dung dịch ban đầu, giá trị pH của dung dịch thu được
 Xem đáp án
Xem đáp án
Đáp án A
Điện phân dung dịch NaCl và HCl (điện cực trơ, màng ngăn xốp). Trong quá trình điện phân, so với dung dịch ban đầu thì giá trị pH của dung dịch thu được tăng lên. Lúc đầu dung dịch có pH nhỏ hơn 7, trong quá trình điện phân, HCl bị điện phân trước làm nồng độ H+ giảm nên pH bắt đầu tăng, khi H+ bị điện phân hết thì dung dịch có pH = 7. Tiếp đó NaCl bị điện phân làm cho nồng độ tăng lên và pH tiếp tục tăng lên lớn hơn 7.
Câu 29:
Biết CO2 chiếm 0,03% thể tích không khí, thể tích không khí (đktc) cần cung cấp cho cây xanh quang hợp để tạo 162 gam tinh bột là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 30:
Khi sục từ từ đến dư CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
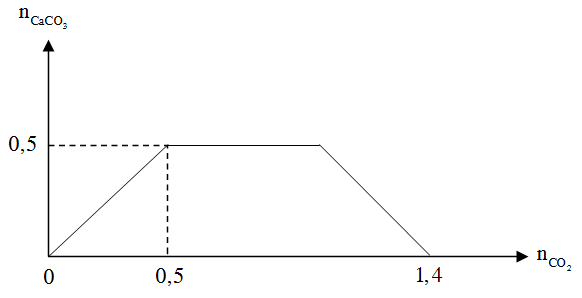
Tỉ lệ a : b là
 Xem đáp án
Xem đáp án
Đáp án A
+ Dựa vào giả thiết và bản chất phản ứng ta có đồ thị:
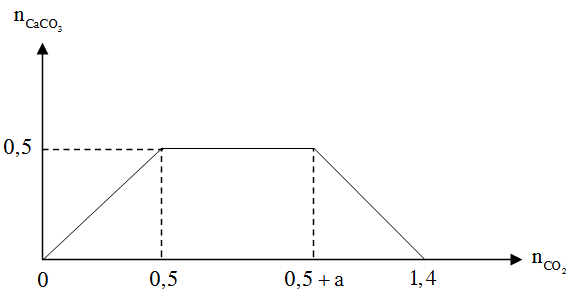
Câu 31:
Điện phân (điện cực trơ, hiệu suất 100%) 300 ml dung dịch CuSO4 0,5M với cường độ dòng điện không đổi 2,68A, trong thời gian t giờ thu được dung dịch X. Cho dung dịch Ba(OH)2 dư vào X thấy xuất hiện 45,73 gam kết tủa. Giá trị của t là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 32:
Cho m gam hỗn hợp X gồm Na, Ca tan hết vào dung dịch Y chứa 0,08 mol NaHCO3 và 0,04 mol CaCl2, sau phản ứng thu được 7 gam kết tủa và thấy thoát ra 0,896 lít khí (đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 33:
X có công thức C4H14O3N2. Khi cho X tác dụng với dung dịch NaOH thì thu được hỗn hợp Y gồm 2 khí ở điều kiện thường và đều có khả năng làm xanh quỳ tím ẩm. Số công thức cấu tạo phù hợp của X là
 Xem đáp án
Xem đáp án
Đáp án D
X tác dụng với dung dịch NaOH, thu được hỗn hợp khí đều có khả năng là xanh giấy quỳ tím ẩm. Chứng tỏ: X là muối amoni; hai khí là NH3 và amin hoặc là 2 amin. Amin ở thể khí nên số nguyên tử C trong phân tử bằng 1 hoặc 2, nếu có 3 nguyên tử C thì phải là amin bậc 3.
Vì hai nguyên tử N đã nằm trong hai khí nên gốc axit trong X không thể chứa N. Mặt khác, gốc axit có 3 nguyên tử O, suy ra X là muối amoni của axit cacbonic, chứa gốc để liên kết với hai gốc amoni.
Số công thức cấu tạo của X thỏa mãn là 3:
Câu 34:
Hợp chất hữu cơ mạch hở X có công thức phân tử C5H10O. Chất X không phản ứng với Na, thỏa mãn sơ đồ chuyển hóa sau: Este có mùi chuối chín.
Tên của X là
 Xem đáp án
Xem đáp án
Đáp án D
Este có mùi chuối chín là iso – amylaxetat CH3COOCH2CH2CH(CH3)CH3. Suy ra Y là ancol iso – amylic CH3CH(CH3)CH2CH2OH; X là 3 – metylbutanal CH3CH(CH3)CH2CHO. Sơ đồ phản ứng:
Câu 35:
Hỗn hợp X gồm Gly và Ala. Người ta lấy m gam X cho tác dụng với lượng vừa đủ KOH, thu được 13,13 gam hỗn hợp muối. Mặt khác, cũng từ lượng X trên ở điều kiện thích hợp người ta điều chế được hỗn hợp Y chỉ gồm hỗn hợp các peptit có tổng khối lượng m’ gam và nước. Đốt cháy hoàn toàn m’ gam hỗn hợp peptit trên cần 7,224 lít khí O2 (đktc). Giá trị đúng của m gần nhất với?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 36:
Hỗn hợp X gồm (CH3COO)3C3H5, CH3COOCH2CH(OOCCH3)CH2OH, CH3COOH, CH3COOCH2CHOHCH2OH và CH2OHCHOHCH2OH trong đó CH3COOH chiếm 10% tổng số mol hỗn hợp. Đun nóng m gam hỗn hợp X với dung dịch NaOH vừa đủ, thu được dung dịch chứa 20,5 gam natri axetat và 0,604m gam glixerol. Để đốt cháy m gam hỗn hợp X cần V lít O2 (đktc). Giá trị của V gần nhất là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 37:
Hỗn hợp bột X gồm 3 kim loại Ba, Na, Zn có tỉ lệ mol tương ứng là 2:3:x. Cho 7,98 gam X vào lượng nước dư, thu được V lít khí (đktc). Nếu cũng lượng X trên cho vào dung dịch KOH dư thì thu được 2,352 lít khí (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 38:
Cho m gam hỗn hợp X gồm Cu và Fe2O3 vào 200,0 ml dung dịch chứa NaNO3 1M và H2SO4 2M, thu được dung dịch Y và thấy thoát ra 1,12 lít khí NO. Thêm dung dịch HCl dư vào dung dịch Y, lại thấy thoát ra 1,12 lít khí NO. Biết NO là sản phẩm khử duy nhất của ion nitrat và thể tích khí đo ở đktc. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 39:
Hòa tan hoàn toàn 31 gam hỗn hợp M gồm Fe và Mg vào 250 gam dung dịch H2SO4 73,1276% đun nóng, thu được dung dịch X; 1,68 gam rắn không tan; 32,287 gam hỗn hợp khí Y gồm H2S và SO2 có tỉ khối so với hiđro là d. Cho từ từ dung dịch Ba(OH)2 0,75M vào dung dịch X đến khi kết tủa đạt cực đại thì thấy vừa hết 1,65 lít. Lọc lấy kết tủa đem cân thì thấy có khối lượng là 359,7125 gam. Giá trị của d là
 Xem đáp án
Xem đáp án
Đáp án B
+ Sơ đồ phản ứng:
Câu 40:
Hỗn hợp X gồm 2 este đơn chức (chứa C, H, O). Thủy phân hoàn toàn 0,15 mol X cần 200 ml dung dịch NaOH 1M, thu được một ancol Y và 16,7 gam hỗn hợp hai muối. Đốt cháy hoàn toàn Y, sau đó hấp thụ toàn bộ sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư, khối lượng bình tăng 8 gam. Hỗn hợp X là
 Xem đáp án
Xem đáp án
Đáp án A
