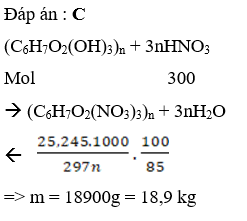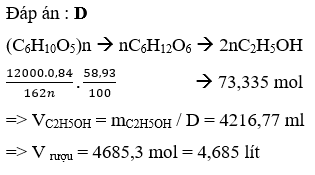15 đề Ôn luyện Hóa học cực hay có lời giải (Đề số 6)
-
3057 lượt thi
-
50 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 3:
Đun nóng hỗn hợp gồm hai ancol đơn chức, mạch hở, kế tiếp nhau trong dãy đồng đẳng với H2SO4 đặc ở 140oC. Sau khi các phản ứng kết thúc, thu được 6 gam hỗn hợp gồm ba ete và 1,8 gam nước. Công thức phân tử của hai ancol trên là
 Xem đáp án
Xem đáp án
Đáp án : A
Câu 4:
Hợp chất A là chất rắn, có nhiều ứng dụng như: chế tạo thuốc nổ, pháo hoa, sản xuất diêm. Chất A là
 Xem đáp án
Xem đáp án
Đáp án : C
Câu 5:
Xà phòng hóa 8,8 gam etyl axetat bằng 200 ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn khan có khối lượng là
 Xem đáp án
Xem đáp án
Đáp án D
neste = 0,1 mol ; nNaOH = 0,04 mol
CH3COOC2H5 + NaOH -> CH3COONa + C2H5OH
=> Sau phản ứng có : 0,04 mol CH3COONa
=> m rắn khan = 3,28g
Câu 8:
Dung dịch X chứa các ion sau: Al3+, Cu2+, SO42- và NO3-. Để kết tủa hết ion SO42- có trong 250 ml dung dịch X cần 50 ml dung dịch BaCl2 1M. Cho 500 ml dung dịch X tác dụng với dung dịch NH3 dư thì được 7,8 gam kết tủa. Làm bay hơi hết nước có trong 500 ml dung dịch X được 37,3 gam hỗn hợp muối khan. Nồng độ mol của NO3- trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án : B
250 ml X phản ứng với 50 ml BaCl2
=> 500 ml X phản ứng với 100 ml BaCl2 => nSO4 = nBa2+ = 0,1 mol
X phản ứng với NH3 => tạo kết tủa Al(OH)3 ( Cu(OH)2 tan trong NH3)
=> nAl3+ = nAl(OH)3 = 0,1 mol
Trong X : Bảo toàn điện tích : 3nAl3+ + 2nCu2+ = nNO3- + 2nSO42-
Laij cos : mmuối X = 27.nAl3+ + 64nCu2+ + 62nNO3 + 96nSO4 = 37,3g
=> nNO3- = 0,3 mol
=> CM(NO3-) = 0,6M
Câu 9:
Khi thủy phân đến cùng xenlulozơ và tinh bột, ta đều thu được các phân tử glucozơ. Thí nghiệm đó chứng tỏ điều gì
 Xem đáp án
Xem đáp án
Đáp án : C
Câu 10:
Tổng số liên kết pi và vòng trong phân tử C7H6O3 là
 Xem đáp án
Xem đáp án
Đáp án : D
(pi + vòng) = (2C + 2 - H)/2
Câu 11:
Dẫn mẫu khí thải của một nhà máy qua dung dịch Pb(NO3)2 dư thì thấy xuất hiện kết tủa màu đen. Hiện tượng đó chứng tỏ trong khí thải nhà máy có chứa khí nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án : C
Dựa vào phản ứng : Pb(NO3)2 + H2S -> 2HNO3 + PbS↓ đen
Câu 12:
Phát biểu nào sau đây không chính xác
 Xem đáp án
Xem đáp án
Đáp án : A
Đồng phân là các chất có cùng công thức phân tử.
Các chất có cùng khối lượng phân tử chưa chắc đã cùng công thức phân tử
Câu 13:
Hoà tan hoàn toàn 4,8 gam kim loại R trong H2SO4 đặc nóng thu được 1,68 lít SO2 (đktc). Lượng SO2 thu được cho hấp thụ hoàn toàn vào dung dịch NaOH dư thu được m gam muối. Kim loại R và giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án : B
. 2NaOH + SO3 -> Na2SO3 + H2O
=> mmuối = nNa2SO3.126 = nSO2.126 = 9,45g
Câu 14:
Cho các chất sau: xiclopropan, benzen, stiren, metyl acrylat, vinyl axetat, đimetyl ete. Số chất có khả năng làm mất màu dung dịch Br2 là
 Xem đáp án
Xem đáp án
Đáp án : C
Các chất thỏa mãn là : xiclopropan , Stiren , metylacrylat , vinylaxetat
=> Có 4 chất
Câu 16:
Cho phản ứng hóa học: 6nCO2 + 5nH2O -> (C6H10O5)n + 6nO2.
Phản ứng trên thuộc quá trình nào sau đây
 Xem đáp án
Xem đáp án
Đáp án : C
Câu 17:
Hai este X và Y có cùng CTPT C8H8O2 và chứa vòng benzen trong phân tử. Cho 6,8 gam hỗn hợp gồm X và Y tác dụng với dung dịch NaOH dư, đun nóng, lượng NaOH phản ứng tối đa là 0,06 mol, thu được dung dịch Z chứa 4,7 gam ba muối. Khối lượng muối của axit cacboxylic có phân tử khối lớn hơn trong Z là
 Xem đáp án
Xem đáp án
Đáp án : B
, nhh = 0,05 mol < nNaOH = 0,06 mol < 2nhh
Phản ứng xà phòng tạo 3 muối
=> Trong hỗn hợp có 1este của phenol
=> hỗn hợp có este :
+) TH1 : C6H5COOCH3 ; R1COOC6H4R2 với số mol lần lượt là x và y
=> nNaOH = x + 2y = 0,06 ; nhh = x + y = 0,05
=> x = 0,04 ; y = 0,01 mol
=> Axit có phân tử khối lớn hơn là C6H5COOH
C6H5COOCH3 + NaOH -> C6H5COONa + CH3OH
R1COOC6H4R2 + 2NaOH -> R1COONa + R2C6H4ONa + H2O
=> phản ứng tạo nC6H5COONa = nC6H5COOCH3 = x = 0,04 mol
=> mmuối cần tìm = 5,76g > 4,7 => Loại
+) TH2 : Hỗn hợp este gồm HCOOCH2C6H5 và CH3COOC6H5
=> Axit có khối lượng phân tử lớn hơn là CH3COOH
=> nCH3COONa = nCH3COOC6H5 = 0,01 mol
=> mCH3COONa = 0,82g
Câu 18:
Một hỗn hợp gồm etilen và axetilen có thể tích 6,72 lít (đktc). Cho hỗn hợp đó qua dung dịch brom dư để phản ứng xảy ra hoàn toàn, lượng brom phản ứng là 64 gam. Phần trăm về thể tích của etilen và axetilen lần lượt là
 Xem đáp án
Xem đáp án
Đáp án : B
Gọi số mol etilen và axelilen lần lượt là a và b mol
=> a + b = 0,3 mol
C2H4 + Br2 -> C2H4Br2
C2H2 + 2Br2 -> C2H2Br4
Khi phản ứng với Br2 : nBr2 = a + 2b = 0,4 mol
=> a = 0,2 ; b = 0,1 mol
=> %V etilen = 66,67%
Câu 20:
Cho 3 axit: ClCH2COOH, BrCH2COOH, ICH2COOH. Dãy sắp xếp theo thứ tự tăng dần tính axit là
 Xem đáp án
Xem đáp án
Đáp án : D
Câu 22:
Cho sơ đồ phản ứng sau: CH4 → X → Y→ Z→ T → C6H5OH. (X, Y, Z là các chất hữu cơ khác nhau). Z có thể là
 Xem đáp án
Xem đáp án
Đáp án : D
Sơ đồ : CH4 → C2H2 → C6H6 → C6H5Br → C6H5ONa → C6H5OH
Câu 23:
Thí nghiệm với dung dịch HNO3 thường sinh ra khí độc NO2. Để hạn chế khí NO2 thoát ra từ ống nghiệm, biện pháp nào sau đây là hiệu quả nhất?
 Xem đáp án
Xem đáp án
Đáp án : A
Câu 26:
Hòa tan hoàn toàn 20,6 gam hỗn hợp gồm Na2CO3 và CaCO3 bằng dung dịch HCl dư, thu được V lít khí CO2 (đktc) và dung dịch chứa 22,8 gam hỗn hợp muối. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án : B
Ta thấy : Phản ứng có thể coi là : 1 mol CO32- thay bằng 2 mol Cl- trong muối
Đặt số mol CO3 trong muối là x mol
=> mmuối sau - mmuối trước = 22,8 – 20,6 = 35,5.2x – 60x
=> x = 0,2 mol
=> nCO2 = x = 0,2 mol => V = 4,48 lit
Câu 27:
Hỗn hợp X gồm Al, Fe3O4 và CuO, trong đó oxi chiếm 25% khối lượng hỗn hợp. Cho 1,344 lít khí CO (đktc) đi qua m gam X nung nóng, sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hòa tan hoàn toàn Y trong dung dịch HNO3 loãng (dư), thu được dung dịch chứa 3,08m gam muối và 0,896 lít khí NO (ở đktc, là sản phẩm khử duy nhất). Giá trị m gần giá trị nào nhất sau đây?
 Xem đáp án
Xem đáp án
Đáp án : B
Z có : nCO = nCO2 = 0,03 mol
=> nO pứ = nCO pứ = 0,03 mol. Đặt nO dư = a
=> Coi Y gồm Kim loại và O dư a mol
=> m = (100/25).16(a + 0,03) = 64(a + 0,03)
=> nNO3 muối = 2a + 0,04.3 = 2a + 0,12 mol
=> 3,08.64(a + 0,03) = [64(a + 0,03) – 16(a + 0,03)] + 62(2a + 0,12)
=> a = 0,118 => m = 64( 0,118 + 0,03) = 9,472g
Câu 28:
Cho 8 gam Ca tan hoàn toàn trong 200ml dung dịch hỗn hợp HCl 2M và H2SO4 0,75M thu được khí H2 và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Đáp án nào sau đây là đúng về giá trị của m?
 Xem đáp án
Xem đáp án
Đáp án : B
Z có : nCO = nCO2 = 0,03 mol
=> nO pứ = nCO pứ = 0,03 mol. Đặt nO dư = a
=> Coi Y gồm Kim loại và O dư a mol
=> m = (100/25).16(a + 0,03) = 64(a + 0,03)
=> nNO3 muối = 2a + 0,04.3 = 2a + 0,12 mol
=> 3,08.64(a + 0,03) = [64(a + 0,03) – 16(a + 0,03)] + 62(2a + 0,12)
=> a = 0,118 => m = 64( 0,118 + 0,03) = 9,472g
Câu 29:
Cho 8 gam Ca tan hoàn toàn trong 200ml dung dịch hỗn hợp HCl 2M và H2SO4 0,75M thu được khí H2 và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Đáp án nào sau đây là đúng về giá trị của m?
 Xem đáp án
Xem đáp án
Đáp án : B
Z có : nCO = nCO2 = 0,03 mol
=> nO pứ = nCO pứ = 0,03 mol. Đặt nO dư = a
=> Coi Y gồm Kim loại và O dư a mol
=> m = (100/25).16(a + 0,03) = 64(a + 0,03)
=> nNO3 muối = 2a + 0,04.3 = 2a + 0,12 mol
=> 3,08.64(a + 0,03) = [64(a + 0,03) – 16(a + 0,03)] + 62(2a + 0,12)
=> a = 0,118 => m = 64( 0,118 + 0,03) = 9,472g
Câu 30:
Trộn 100 ml dung dịch A gồm KHCO3 1M và K2CO3 1M vào 100 ml dung dịch B gồm NaHCO3 1M và Na2CO3 1M thu được dung dịch C. Nhỏ từ từ 100ml dung dịch D gồm H2SO4 1M và HCl 1M vào dung dịch C thu được V lít khí CO2 (đktc) và dung dịch E. Cho dung dịch Ba(OH)2 tới dư vào dung dịch E thu được m gam kết tủa. Giá trị của m và V là
 Xem đáp án
Xem đáp án
Đáp án : C
Sau khi trộn thì trong dung dịch có : 0,2 mol HCO3- và 0,2 molCO32-
D có : nH+ = 0,3 mol ; 0,1 mol SO42-
Khi nhỏ từ từ D và thì thứ tự phản ứng là :
CO32- + H+ -> HCO3-
HCO3- + H+ -> CO2 + H2O
=> Còn lại : 0,3 mol HCO3‑ ; 0,1 mol SO42-
Phản ứng với Ba(OH)2 => kết tủa gồm : 0,3 mol BaCO3 và 0,1 mol BaSO4
=> m = 82,4g
VCO2 = 0,1 mol = 2,24 lit
Câu 31:
Thủy phân este X trong môi trường kiềm, thu được natri axetat và ancol etylic. Công thức của X là
 Xem đáp án
Xem đáp án
Đáp án : C
Câu 32:
Axit malic là hợp chất hữu cơ tạp chức, có mạch cacbon không phân nhánh, là nguyên nhân chính gây nên vị chua của quả táo. Biết rằng 1 mol axit malic phản ứng được với tối đa 2 mol NaHCO3. Công thức của axit malic là
 Xem đáp án
Xem đáp án
Đáp án : C
Câu 34:
Hợp chất X có công thức phân tử C4H6O3. X phản ứng được với Na, NaOH và có phản ứng tráng bạc. Công thức cấu tạo của X có thể là
 Xem đáp án
Xem đáp án
Đáp án : B
Câu 35:
Cho hỗn hợp gồm 0,1 mol HCHO và 0,1 mol HCOOH tác dụng với lượng dư AgNO3 trong NH3 đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng Ag tạo thành là
 Xem đáp án
Xem đáp án
Đáp án : A
nAg = 4nHCHO + 2nHCOOH = 0,1.4 + 0,1.2 = 0,6 mol
=> mAg = 64,8g
Câu 36:
Cho khí X đi qua hơi nước thấy có hiện tượng bốc cháy. Khí X có thể là
 Xem đáp án
Xem đáp án
Đáp án : B
F2 phản ứng với nước tạo O2 => bốc cháy
Câu 38:
Cho phản ứng:
FeSO4 + KMnO4 + H2SO4 -> Fe2(SO4)3 + K2SO4 + MnSO4 + H2O.
Sau khi cân bằng (với hệ số là các số nguyên, tối giản), tổng hệ số của các chất tham gia phản ứng là
 Xem đáp án
Xem đáp án
Đáp án : C
10FeSO4 + 2KMnO4 + 8H2SO4 -> 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
Câu 39:
Có bốn lọ mất nhãn, riêng biệt chứa: glixerol, ancol etylic, glucozơ và axit axetic. Thuốc thử nào sau đây có thể dùng để phân biệt các dung dịch trong từng lọ trên?
 Xem đáp án
Xem đáp án
Đáp án : D
Dùng Cu(OH)2/OH- :
+) ancol etylic không phản ứng
+) axit axetic : tạo dung dcihj màu xanh lam
+) Glixerol : tạo phức xanh đặc trưng
+) Glucozo : tạo phức xanh đặc trưng ở điều kiện thường , khi đun nóng thì tạo kết tủa đỏ gạch
Câu 40:
Cho hỗn hợp X gồm hai hợp chất hữu cơ no, đơn chức tác dụng vừa đủ với 100ml dung dịch KOH 0,4M, thu được một muối và 336ml hơi một ancol (đktc). Nếu đốt cháy hoàn toàn lượng hỗn hợp X trên, sau đó hấp thụ hết sản phẩm cháy vào bình đựng dung dịch Ca(OH)2 dư thì khối lượng bình tăng 6,82 gam. Công thức của hai hợp chất hữu cơ trong X là
 Xem đáp án
Xem đáp án
Đáp án : D
, nancol = 0,015 mol < nKOH = 0,04 mol
=> hỗn hợp gồm 1 axit và 1 este.
=> số mol axit = 0,025 mol ; số mol este = 0,015 mol
Khi đốt cháy thì thu được nCO2 = nH2O
=> mbình tăng = mCO2 + mH2O => nCO2 = nH2O = 0,11 mol
Gọi số C trong axit và este lần lượt là a và b
Bảo toàn C : 0,025a + 0,015b = nCO2 = 0,11
=> a = 2 ; b = 4
=> CH3COOH và este C4H8O2
Câu 43:
Chọn đáp án đúng
 Xem đáp án
Xem đáp án
Đáp án : A
_ Tinh thể I2 thuộc loại mạng tinh thể phân tử
_ Kim cương : mạng tinh thể nguyên tử ; Nước đá : mạng tinh thể phân tử
_ hóa trị của N trong HNO3 là 4
_ Không phải mọi hợp chất của các phi kim chỉ có liên kết cộng hóa trị. Ví dụ như có thể chứa liên kết cho nhận ( SO2, SO3 , ..)
Câu 46:
Một thí nghiệm với khí amoniac được bố trí như hình sau:
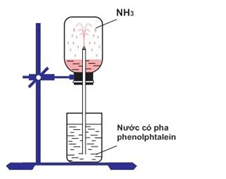
Qua hiện tượng thí nghiệm cho thấy
 Xem đáp án
Xem đáp án
Đáp án : B
Câu 48:
Hỗn hợp X gồm N2 và H2 có tỉ khối so với He bằng 1,8. Đun nóng X một thời gian trong bình kín (có bột Fe làm xúc tác) thu được hỗn hợp Y có tỉ khối so với He bằng 2. Hiệu suất của phản ứng tổng hợp NH3 là
 Xem đáp án
Xem đáp án
Đáp án : A
MX = 7,2 . Áp dụng qui tắc đường chéo ta có : nH2 : nN2 = 4 : 1
=> Giả sử ban đầu có 4 mol H2 và 1 mol N2 trong X
N2 + 3H2 ↔ 2NH3
,x -> 3x -> 2x
=> sau phản ứng : nY = 2x + (1 – x) + (4 – 3x) = 5 – 2x mol
Bảo toàn khối lượng : mX = mY
=> 5.7,2 = (5 – 2x).2.4
=> x = 0,25 mol
=> H% ( tính theo N2) = 25%
Câu 49:
Phát biểu nào sau đây không đúng
 Xem đáp án
Xem đáp án
Đáp án : D
Cả Glucozo và Fructozo đều có phản ứng tráng bạc
Câu 50:
Ứng với công thức phân tử C4H8O2 có số đồng phân este là
 Xem đáp án
Xem đáp án
Đáp án : A
Có 4 đồng phân :
HCOOCH2CH2CH3 ; HCOOCH(CH3)2
CH3COOC2H5
C2H5COOCH3