Bộ đề ôn thi THPTQG 2019 Hóa học cực hay có lời giải chi tiết
Bộ đề ôn thi THPTQG 2019 Hóa học cực hay có lời giải chi tiết (Đề số 4)
-
5805 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây khử được HCl ở nhiệt độ thường?
 Xem đáp án
Xem đáp án
Đáp án B
vì chỉ có Fe đứng trước H+ trong dãy điện hóa
Câu 2:
Cho 0,15 mol phenyl axetat tác dụng với lượng dư dung dịch KOH 0,5M (đun nóng). Thể tích KOH 0,5M phản ứng là.
 Xem đáp án
Xem đáp án
Đáp án C
nKOH = 2n(CH3-COOC6H5)= 2.0,15= 0,3 mol
=> V(KOH) =0,3/0,5 = 0,6(l)= 600 ml
Câu 3:
Kim loại nào sau đây khi cho vào dung dịch CuSO4 bị hòa tan hết và phản ứng tạo thành kết tủa gồm 2 chất
 Xem đáp án
Xem đáp án
Đáp án C
Câu 4:
Chất nào sau đây được dùng làm tơ sợi?
 Xem đáp án
Xem đáp án
Đáp án C
vì Xenlulozo có cấu trúc không phân nhánh và không xoắn, có độ bền cơ học bền nhiệt cao hơn so với tinh bột do đó được dùng để chế tạo sợi thiên nhiên và nhân tạo
Câu 5:
Polime X là chất rắn trong suốt, có khả năng cho ánh sáng truyền qua tốt nên được dùng chế tạo thủy tinh hữu cơ plexiglas. Tên gọi của X là:
 Xem đáp án
Xem đáp án
Đáp án C
Câu 6:
Hòa tan hoàn toàn 3,02 gam hỗn hợp X chứa Al, Fe, Mg trong 200 ml dung dịch hỗn hợp chứa HCl 0,6M và H2SO4 0,3M. Sau phản ứng thu được 1,792 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là?
 Xem đáp án
Xem đáp án
Đáp án B
vì nH2=1.792/22.4=0.08 mol
=>nH+p.ứng= 0.16 mol
nHCl=0.12 mol
nH2SO4=0.06 mol
=>H+ dư
TH1: HCl hết
=> m= 3.02+0.12x35.5+0.02x96=9.2g
TH2:H2SO4 hết
=> m= 3.02+0.04x35.5+0.06x96=10.2g
Câu 7:
Kim loại nào sau đây tác dụng với dung dịch FeCl3 tạo thành Fe
 Xem đáp án
Xem đáp án
Đáp án D
vì Zn ko tan trong nc và đứng trc Fe2+ trong dãy điện hóa
Câu 9:
Loại đá nào sau đây không chứa CaCO3?
 Xem đáp án
Xem đáp án
Đáp án B
vì Thạch cao là khoáng vật trầm tích hay phong hóa rất mềm, với thành phần là muối canxi sulfat ngậm 2 phân tử nước (CaSO4. 2H2O)
Câu 11:
Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc lá. Chất gây nghiện và gây ung thư có trong thuốc lá là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 13:
Dãy các chất đều tác dụng với dung dịch nước Br2 là.
 Xem đáp án
Xem đáp án
Đáp án C
vì Fructozo, etyl fomat và saccarozo ko phan ưng vs dd brom
Câu 14:
Sục 3,36 lít khí CO2 vào 100ml dung dịch chứa Ca(OH)2 0,6M và KOH 0,6M thu được m gam kết tủa. Giá trị của m là?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 15:
Chất hữu cơ X (chứa vòng benzen) có công thức là CH3COOC6H4OH. Khi đun nóng, a mol X tác dụng được với tối đa bao nhiêu mol NaOH trong dung dịch?
 Xem đáp án
Xem đáp án
Đáp án C
vì CH3COOC6H4OH + NaOH 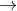 CH3COONa + C6H4(OH)2
CH3COONa + C6H4(OH)2
C6H4(OH)2 + 2NaOH 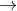 C6H4(ONa)2 + 2H2O
C6H4(ONa)2 + 2H2O
nNaOH = 3a mol
Câu 17:
Để trung hòa 6,72 g axit cacboxylic Y no, đơn chức cần 200 g dung dịch NaOH 2,24%. Công thức của Y là
 Xem đáp án
Xem đáp án
Đáp án C vì
nNaOH = 0,112 mol
Y là axit no, mạch hở => nRCOOH = nNaOH = 0,112 mol
=> M = 6,72 / 0,112 = 60 => Y là CH3COOH
Câu 19:
Trong các dãy chất sau, dãy nào đều gồm các chất điện li mạnh
 Xem đáp án
Xem đáp án
Đáp án A vì
C6H6, H2S điện ly yếu
Câu 20:
Đốt cháy hoàn toàn m gam ancol no, đơn chức, mạch hở, sau phản ứng thu được 13,2g CO2 và 8,lg H2O. Công thức cấu tạo thu gọn của ancol đó là:
 Xem đáp án
Xem đáp án
Đáp án B vì
nCO2 = 13,2: 44 = 0,3 (mol), nH2O = 8,1 : 18 = 0,45 (mol)
nC : nH = 0,3 : (2.0,45) = 1:3
=> C2H6O vì ko tồn tại CH3O và C3H9O
Câu 21:
Cho các thí nghiệm sau:
(a) Đốt thanh Cu ngoài không khí.
(b) Nhúng thanh Mg vào dung dịch FeCl2.
(c) Nhúng thanh Fe vào dung dịch hỗn hợp CuCl2 và HCl.
(d) Nhúng thanh Al vào dung dịch H2SO4 loãng có pha thêm vài giọt CuSO4.
Tổng số thí nghiệm có xảy ra quá trình ăn mòn hóa học là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 22:
Dung dịch X chứa K2SO4 0,1M và Al(SO4)3 0,12m. Cho rất từ từ dung dịch chứa Ba(OH)2 vào 100 ml dung dịch X thì khối lượng kết tủa lớn nhất có thể thu được là?
 Xem đáp án
Xem đáp án
Đáp án D
Câu 23:
Đốt cháy hoàn toàn 17,68 gam một chất béo X cần vừa đủ 1,6 mol O2 thu được 1,04 mol nước. Cho toàn bộ lượng chất béo trên tác dụng với NaOH dư thì khối lượng ancol thu được là?
 Xem đáp án
Xem đáp án
Đáp án A vì
mCO2 = m(chất béo) + mO2(cháy) - mH2O
= 17,68 +1,6.32 -1,04.18= 50,16g
=> nCO2 =1,14 mol
nO(trong cbeo) = nO(CO2) + nO(H2O) - nO(O2)= 1,14.2 + 1.04 - 1,6.2= 0,12mol
=> n(C3H8O3) =0,12/6 = 0,02mol
=> m(C3H8O3)= 0,02 .92= 1.84g
Câu 24:
Hòa tan hoàn toàn 29,95 gam hỗn hợp X chứa Al, Ca và Ba trong nước dư thu được 12,32 lít khí H2 (đktc) và dung dịch Y chứa 41,45 gam chất tan. Số mol Al có trong hỗn hợp X là?
 Xem đáp án
Xem đáp án
Đáp án C
Câu 25:
Cho hỗn hợp gồm Fe(NO3)2, CuO và ZnO vào dung dịch H2SO4 (loãng, dư) thu được dung dịch Y. Cho dung dịch Ba(OH)2 (dư) vào Y thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 26:
Hỗn hợp X gồm axit axetic và etyl fomat (tỷ lệ mol 1:1) tác dụng vừa đủ với 100 ml dung dịch Y chứa đồng thời KOH 1,0M và NaOH 1,0M thu được dung dịch Z. Cô cạn dung dịch Z thu được m gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 27:
Cho các thí nghiệm sau:
(1).Sục khí H2S vào dung dịch FeSO4.
(2). Sục khí H2S vào dung dịch CuSO4.
(3). Sục khí CO2 dư vào dung dịch Na2SiO3.
(4). Sục khí CO2 dư vào dung dịch Ca(OH)2.
(5).Nhỏ từ từ dung dịch NH3 đến dư vào dung dịch Al2(SO4)3.
(6). Nhỏ từ từ dung dịch Ba(OH)2 đến dư vào dung dịch Al2(SO4)3
Thí nghiệm thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án B
1,H2S + FeSO4→ không phản ứng.
2,H2S + CuSO4 → CuS↓ + H2SO4
3, 2CO2 + 2H2O + Na2SiO3 → H2SiO3↓ + 2NaHCO3
4,CO2 + Ca(OH)2 → CaCO3↓ + H2O
CO2 dư + H2O + CaCO3 → Ca(HCO3)2
5, 6NH3 + 6H2O + Al2(SO4)3 → Al(OH)3↓ + 3(NH4)2SO4
6, 3Ba(OH)2 + Al2(SO4)3 → 3BaSO4 ↓ + 2Al(OH)3↓
Ba(OH)2 dư + 2Al(OH)3 → Ba[Al(OH)4]2.
=>Các thí nghiêm (2); (3); (5) và (6) thu được kết tủa
Câu 28:
Hỗn hợp A gồm N2 và H2 theo tỷ lệ thể tích 1:3, tạo phản ứng giữa N2 và H2 sinh ra NH3. Sau phản ứng được hỗn hợp khí B có tỉ khối so với khí A là 0,6. Hiệu suất phản ứng là
 Xem đáp án
Xem đáp án
Đáp án A vì
Coi hỗn hợp có 1 mol N2 và 3 mol H2
Số mol khí trước p.ứ: nA = 1 + 3 = 4 (mol)
Gọi số mol N2 phản ứng là x
N2 + 3H2 ⇆ 2NH3
Ban đầu: 1 3
P.ứ: x → 3x → 2x
Cân bằng:1-x 3-3x 2x
Số mol khí sau p.ứ: nB = 1-x + 3-3x + 2x = 4-2x (mol)
Ta có:
Nếu phản ứng xảy ra hoàn toàn thì N2 và H2 phản ứng vừa đủ với nhau.
Câu 29:
Cho dd Ba(OH)2 đến dư vào 10 ml dd X chứa các ion: , , thì có 2,33 gam kết tủa tạo thành và đun nóng thì có 0,672 lít (đktc) một khí bay ra. Nồng độ mol của (NH4)2SO4 và NH4NO3 đã hòa tan trong 10 ml X là
 Xem đáp án
Xem đáp án
Đáp án A vì
Ta có: n.ktủa =nBaSO4=0,1 mol=n(SO4)2-
Lại có nKhí =nNH3=nNH4+=0,3 mol
Bảo toàn điện tích trong X: nNH4=2n(SO4)2- +nNO3-⇒nNO3-=0,1 mol
⇒ X có 0,1 mol NH4NO3 và 0,1 mol (NH4)2SO4
⇒ 2 chất có CM là 1M
Câu 30:
Cho lần lượt các chất C2H5CHO, HCOOH, C6H5OH, C6H5CH2OH, CH2=CH-COOH, CH3OH vào dung dịch NaOH, đun nóng. Số chất tham gia phản ứng là
 Xem đáp án
Xem đáp án
Đáp án C vì
chỉ có axit và phenol phản ứng NaOH trong các chất trên
Câu 31:
Lấy một lượng ancol but-2-in-l,4-diol cho qua bình đựng CuO đun nóng một thời gian được 14,5 gam hỗn hợp X gồm khí và hơi (Giả sử chỉ xảy ra phản ứng oxi hóa chức ancol thành chức andehit). Chia X thành 2 phần bằng nhau:
- Phần 1: Tác dụng với Na dư thu được 1,68 lít H2 (đktc)
- Phần 2: Tác dụng vừa đủ với dung dịch nước chứa m gam Br2.
Xác định m?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 32:
Tiến hành các thí nghiệm sau ở điều kiện thường:
(a) Sục khí H2S vào dung dịch FeCl3
(b) Sục khí Cl2 vào dung dịch amoniac
(c) Cho KMnO4 vào dung dịch HCl đặc
(d) Sục khí Cl2 vào dung dịch NaOH
(e) Cho Si vào dung dịch NaOH
(g) Đốt khí NH3 trong khí oxi có mặt xúc tác
Số thí nghiệm có sinh ra đơn chất là
 Xem đáp án
Xem đáp án
Đáp án D
vì a tạo ra S, b tạo ra N2, c tạo ra Cl2, g tạo ra N2
Câu 33:
Cho các phát biểu sau:
(a) Tất cả các peptit đều có phản ứng thủy phân (ở điều kiện thích hợp).
(b) Muối phenylamoni clorua không tan trong nước.
(c) Ở điều kiện thường, metylamin và đimetylamin là những chất khí.
(d) Trong phân tử peptit mạch hở Gly-Ala-Gly có 4 nguyên tử oxi.
(e) Ở điều kiện thường, amino axit là những chất lỏng.
(f) Đa số amin độc, một số ít không độc.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án D vì
(a) đúng
(b) sai, muối phenylamoni clorua tan được trong nước.
(c) đúng. HS ghi nhớ 4 amin là chất khí ở điều kiện thường: metylamin, đimetylamin, trimetylamin, etylamin.
(d) đúng, CTCT: H2N-CH2-CONH-CH(CH3)-CONH-CH2-COOH có 4 nguyên tử O
(e) sai, ở điều kiện thường amino axit là những chất rắn kết tinh
(f) sai vì tất cả các amin đều độc
Câu 34:
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(2) Cho dung dịch HCl tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(3) Sục khí H2S vào dung dịch FeCl2.
(4) Sục khí NH3 tới dư vào dung dịch AlCl3.
(5) Sục khí CO2 tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(6) Sục khí etilen vào dung dịch KMnO4.
(7) Cho Ba(OH)2 dư vào ZnSO4.
(8) Cho AgNO3 vào dung dịch FeCl3.
Sau khi các phản ứng kết thúc, tổng số thí nghiệm thu được kết tủa là:
 Xem đáp án
Xem đáp án
Đáp án B
vì chỉ có 2 và 3 ko thu được kết tủa
Câu 35:
Hỗn hợp E gồm chất X (C3H10N2O4, là muối của axit hữu cơ đa chức) và chất Y (C2H7NO3, là muối của một axit vô cơ). Cho một lượng E tác dụng hết với dung dịch chứa 0,3 mol NaOH, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,16 mol hỗn hợp hai khí có số mol bằng nhau và dung dịch Z. Cô cạn cẩn thận dung dịch Z thu được m gam chất rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Câu 36:
Đốt cháy hoàn toàn a mol X (là trieste của glixerol với các axit đơn chức, mạch hở), thu được b mol CO2 và c mol H2O (b – c = 6a). Hiđro hóa gam X cần 2,688 lít H2 (đktc), thu được 25,86 gam Y (este no). Đun nóng gam X với dung dịch chứa 0,12 mol NaOH, cô cạn dung dịch sau phản ứng, thu được gam chất rắn. Giá trị của là:
 Xem đáp án
Xem đáp án
Đáp án D
Câu 37:
Sục từ từ khí CO2 đến dư vào dung dịch chứa Ca(OH)2 và NaAlO2 (hay Na[Al(OH)4]). Khối lượng kết tủa thu sau phản ứng được biểu diễn trên đồ thị như hình vẽ.
Giá trị của m và X lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 38:
Nung hỗn hợp gồm m gam Al và 0,04 mol Cr2O3 một thời gian, thu được hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HCl đặc, nóng, vừa đủ (không có không khí) thu được 0,1 mol khí H2 và dung dịch Y. Y phản ứng tối đa với 0,56 mol NaOH (biết các phản ứng xảy ra trong điều kiện không có không khí). Giá trị m là:
 Xem đáp án
Xem đáp án
Đáp án B
Câu 39:
Hòa tan hoàn toàn m gam hỗn hợp X gồm Zn, Fe3O4 và Fe(NO3)2 trong dung dịch chứa 1,12 mol HCl và 0,08 mol NaNO3. Sau phản ứng thu được dung dịch Y chi chứa muối clorua và 2,24 lít hỗn hợp khí Z (đktc) có tỉ khối hơi đối với H2 là 10,8 gồm hai khí không màu trong đó có một khí hóa nâu ngoài không khí. Nếu cũng cho dung dịch Y tác dụng với một lượng dư dung dịch NaOH, lọc lấy kết tủa và nung trong không khí đến khối lượng không đổi thu được 4,8 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Số mol của Fe(NO3)2 có trong m gam X là?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 40:
X, Y, Z đều là các peptit mạch hở. Nếu đốt cháy hoàn toàn x mol X hoặc y mol Y hoặc z mol Z thì đều thấy số mol CO2 lớn hơn số mol H2O là 0,075 mol. Mặt khác, cho 96,6 gam hỗn hợp E chứa X, Y, Z với số mol như trên tác dụng vừa đủ với 1 mol NaOH thì thu được hai muối của Gly và Val. Phần trăm khối lượng của chất có PTK nhỏ nhất trong E gần nhất với?
 Xem đáp án
Xem đáp án
Đáp án A

