25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án
25 đề thi minh họa THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề 10)
-
5256 lượt thi
-
40 câu hỏi
-
90 phút
Danh sách câu hỏi
Câu 1:
X là một kim loại nhẹ, màu trắng bạc, được ứng dụng rộng rãi trong đời sống. X là
 Xem đáp án
Xem đáp án
Đáp án D.
– Nhôm là kim loại nhẹ, màu trắng bạc, được ứng dụng rộng rãi trong đời sống.
Kim loại này được dùng để tạo thành vỏ máy bay do độ bền chắc và mỏng nhẹ của nó. Nhôm cũng được dùng để sản xuất các thiết bị và dụng cụ sinh hoạt như nồi, chảo, các đường dây tải điện, các loại cửa,… Phản ứng nhiệt nhôm còn được sử dụng để điều chế các kim loại có nhiệt độ nóng chảy cao (như crom hay vonfarm).
Câu 2:
Quặng nào sau đây có thành phần chính là A12O3 ?
 Xem đáp án
Xem đáp án
Đáp án B.
Quặng boxit có thành phần chính là Al2O3.
Câu 3:
Nước thải công nghiệp thường chứa các ion kim loại nặng như Hg2+, Pb2+, Fe3+... Để xử lí sơ bộ nước thải trên, làm giảm nồng độ các ion kim loại nặng với chi phí thấp, người ta sử dụng chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án D.
- Để xử lí sơ bộ nước thải trên, cần dùng dung dịch kiềm để kết tủa hiđroxit các ion kim loại nặng như Hg2+, Pb2+, Fe3+…
- Dùng Ca(OH)2 thay vì NaOH hay KOH vì Ca(OH)2 giá thành rẻ hơn và phổ biến hơn so với các dung dịch kiềm khác.
Câu 4:
Thủy phân este X trong dung dịch NaOH đun nóng, thu được natri acrylat và ancol metylic. Công thức cấu tạo thu gọn của X là
 Xem đáp án
Xem đáp án
Đáp án C.
PTHH: .
Câu 5:
Ion nào gây nên tính cứng của nước?
 Xem đáp án
Xem đáp án
Đáp án A.
Nước cứng là nước chứa nhiều ion Ca2+, Mg2+.
Câu 6:
 Xem đáp án
Xem đáp án
Đáp án D.
Alanin: quỳ tím không đổi màu.
Axit axetic: quỳ tím hóa đỏ.
Metylamin: quỳ tím hóa xanh.
Câu 7:
Cho Cu phản ứng với dung dịch HNO3 loãng, đun nóng thu được khí không màu, hóa nâu trong không khí. Khí đó là
 Xem đáp án
Xem đáp án
Đáp án A.
NO: khí không màu hóa nâu trong không khí.
N2: khí không màu.
N2O: khí không màu.
NO2: khí màu nâu.
Câu 8:
Nguyên tố có trong hemoglobin (huyết cầu tố) của máu làm nhiệm vụ vận chuyển oxi, duy trì sự sống là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 9:
Trong số các loại tơ sau: tơ tằm, tơ visco, tơ nilon-6,6, tơ axetat, tơ capron, tơ enang. Số tơ thuộc loại tơ nhân tạo là
 Xem đáp án
Xem đáp án
Đáp án A.
- Tơ thiên nhiên: tơ tằm.
- Tơ nhân tạo (bán tổng hợp): tơ visco, tơ axetat.
- Tơ tổng hợp: tơ nilon-6,6, tơ capron, tơ enang.
Câu 10:
Cho các kim loại: Na, K, Al, Fe, Cu, Ag. Số kim loại được điều chế bằng phương pháp điện phân nóng chảy là
 Xem đáp án
Xem đáp án
Đáp án B.
Các kim loại được điều chế bằng phương pháp điện phân nóng chảy: Na, K, Al.
Câu 11:
Cho dãy các chất: glucozơ, saccarozơ, xenlulozơ, tinh bột. Số chất trong dãy không tham gia phản ứng thủy phân là
 Xem đáp án
Xem đáp án
Đáp án B.
- Đisaccarit và polisaccarit tham gia phản ứng thủy phân trong môi trường axit tạo thành monosaccarit.
- Glucozơ là monosaccarit nên không tham gia phản ứng thủy phân.
Câu 12:
Dùng chất nào sau đây để phân biệt ancol etylic và glixerol?
 Xem đáp án
Xem đáp án
Đáp án D.
Glixerol tác dụng với Cu(OH)2/NaOH tạo phức xanh lam.
PTHH:
Câu 13:
Khử hoàn toàn 16 gam bột oxit sắt bằng CO ở nhiệt độ cao. Sau phản ứng khối lượng khí tăng thêm 4,8 gam. Công thức của oxit sắt là công thức nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án C.
Xem phản ứng khử oxit kim loại là quá trình chất khử lấy O trong oxit.
Nên sau phản ứng khối lượng khí tăng thêm 4,8 gam chính là khối lượng O trong oxit mất đi.
Ta có:
Nên oxit sắt là Fe2O3.
Câu 14:
Hấp thụ hoàn toàn 2,24 lít khí CO2 (ở đktc) vào dung dịch chứa 8 gam NaOH, thu được dung dịch X. Khối lượng muối tan trong X là
 Xem đáp án
Xem đáp án
Đáp án A.
Ta có:
Nên sau phản ứng chỉ tạo 1 muối là Na2CO3.
Vậy .
Câu 15:
Cho quỳ tím vào các dung dịch sau: axit axetic (1); glyxin (2); axit ađipic (3); axit -amino propionic (4); phenol (5). Dãy dung dịch làm quỳ tím chuyển sang màu đỏ là
 Xem đáp án
Xem đáp án
Đáp án C.
- Dung dịch làm quỳ tím hóa đỏ: (1), (3).
- Dung dịch không làm quỳ tím đổi màu: (2), (4), (5).
Câu 16:
Khử glucozơ bằng H2 để tạo sobitol. Khối lượng glucozơ dùng để tạo ra 1,82 gam sobitol là bao nhiêu?
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 17:
Cho 0,2 mol -aminoaxit X (có dạng H2NRCOOH) phản ứng vừa đủ với NaOH thu được 22,2 gam muối khan. Phân tử khối của X là
 Xem đáp án
Xem đáp án
Đáp án A.
Cách 1:
Cách 2:
Câu 18:
Cho hỗn hợp các ankan sau: pentan (sôi ở 36oC), heptan (sôi ở 98oC), octan (sôi ở 126oC), nonan (sôi ở 151oC). Có thể tách riêng các chất đó bằng cách nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B.
Những chất có nhiệt độ sôi khác nhau được tách riêng bằng phương pháp chưng cất.
Một số phương pháp tách chất bằng phương pháp vật lí:
- Phương pháp lắng gạn: dùng để tách các chất rắn có khối lượng riêng khác nhau khỏi nước hoặc dung dịch.
- Phương pháp cô cạn: dùng để tách chất tan rắn (không hóa hơi khi gặp nhiệt độ cao) ra khỏi dung dịch.
- Phương pháp hóa học: dùng để tách kết tủa (chất rắn) khỏi dung dịch.
- Phương pháp chưng cất: dùng để tách các chất lỏng dễ bay hơi ra khỏi hỗn hợp.
Sau đó dùng phương pháp ngưng tụ để thu lại các chất.
- Phương pháp chiết tách: dùng để tách các chất lỏng không tan vào nhau từ hỗn hợp tách lớp.
- Phương pháp từ tính: dùng để tách chất bị nhiễm từ (bị nam châm hút) ra khỏi hỗn hợp rắn gồm chất bị nhiễm từ và chất không bị nhiễm từ.
Câu 19:
Dãy gồm các ion cùng tồn tại trong một dung dịch là
 Xem đáp án
Xem đáp án
Đáp án C.
A sai vì
B sai vì
D sai
Câu 20:
Cho các phát biểu sau về cacbohiđrat:
(a) Glucozơ và saccarozơ đều là chất rắn có vị ngọt, dễ tan trong nước.
(b) Tinh bột và xenlulozơ đều là polisaccarit.
(c) Trong dung dịch, glucozơ và saccarozơ đều hòa tan Cu(OH)2, tạo phức màu xanh lam.
(d) Khi thủy phân hoàn toàn hỗn hợp gồm tinh bột và saccarozơ trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất.
(e) Có thể phân biệt glucozơ và fructozơ bằng phản ứng với dung dịch AgNO3/NH3.
(g) Glucozơ và saccarozơ đều tác dụng với H2 (xúc tác Ni, đun nóng) tạo sobitol.
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
Đáp án B.
Những phát biểu đúng: (a), (b), (c).
(d) sai vì thủy phân tinh bột thu được glucozơ, còn thủy phân saccarozơ thu được glucozơ và fructozơ.
(e) sai vì cả glucozơ và fructozơ đều phản ứng với dung dịch AgNO3/NH3 tạo thành kết tủa bạc nên không thể phân biệt được.
(g) sai vì chỉ có glucozơ tác dụng với H2 (xúc tác Ni, đun nóng) tạo sorbitol.
Câu 21:
Chọn nhận xét sai
 Xem đáp án
Xem đáp án
Đáp án C.
Kim loại thể hiện tính khử trong các phản ứng hóa học.
Câu 22:
Chất làm mất màu dung dịch Br2 là
 Xem đáp án
Xem đáp án
Đáp án C.
Triolein là chất béo không no: (C17H33COO)3C3H5 (k = 6, số liên kết C=C là 3) nên có khả năng làm mất màu dung dịch Br2.
Câu 23:
Cho các phát biểu sau:
(a) Các chất metylamin, metylamoni cacbonat, glyxin và anilin đều có khả năng phản ứng với HCl.
(b) Phản ứng thế brom vào vòng benzen của anilin dễ hơn của benzene.
(c) Oxi hóa không hoàn toàn etilen là phưong pháp hiện đại để sản xuất anđehit axetic.
(d) Phenol (C6H5OH) tan tốt trong etanol.
Trong các phát biểu trên, số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án A.
Những phát biểu đúng: (a), (b), (c).
Câu 24:
Phản ứng trong trường hợp nào sau đây không thể tạo sản phẩm là muối Fe(II)?
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 25:
Cho 1,37 gam Ba vào 1 lít dung dịch CuSO4 0,01M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng kết tủa thu được là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 26:
Thực hiện phản ứng este hóa giữa 6,6 gam axit axetic và 16,6 gam ancol etylic thu được 7,48 gam etyl axetat. Hiệu suất của phản ứng este hóa là
 Xem đáp án
Xem đáp án
Đáp án A.
Hiệu suất tính theo axit axetic.
Câu 27:
Cho các phát biểu sau:
(a) Chất béo được gọi chung là triglixerit hay triaxylglixerol.
(b) Chất béo nhẹ hơn nước, không tan trong nước nhưng tan nhiều trong dung môi hữu cơ.
(c) Phản ứng thủy phân chất béo trong môi trường axit là phản ứng thuận nghịch.
(d) Tristearin, triolein có công thức lần lượt là: (C17H33COO)3C3H5, (C17H35COO)3C3H5.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án A.
Những phát biểu đúng: (a), (b), (c).
D sai vì tristearic, triolein có công thức lần lượt là:
Câu 28:
Cho hình vẽ mô tả quá trình điều chế Cl2 trong phòng thí nghiệm như sau:
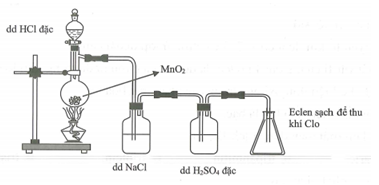
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án A.
Không thể dùng CaO được vì: mặc dù CaO hút ẩm tốt, nhưng sau khi hút nước tạo thành Ca(OH)2, Ca(OH)2 dễ dàng tác dụng với khí Cl2 sinh ra nên không thể thu được khí Cl2.
Câu 29:
Nhiệt phân hoàn toàn hỗn hợp X gồm a mol KNO3 và b mol Fe(NO3)2 trong bình chân không thu được chất rắn Y và hỗn họp khí Z. Cho toàn bộ Z vào nước thì thu được dung dịch HNO3 và không có khí thoát ra. Biểu thức liên hệ giữa a và b là
 Xem đáp án
Xem đáp án
Đáp án C.
a 5a
b 2b 0,25b
Hỗn hợp Z tác dụng hết với nước nên khí NO2 và O2 phản ứng vừa đủ.
Lưu ý phương trình nhiệt phân đặc biệt:
Câu 30:
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X metan, axetilen, buta-1,3-đien và vinylaxetilen thu được 24,2 gam CO2 và 7,2 gam H2O. Biết a mol hỗn họp X làm mất màu tối đa 112 gam Br2 trong dung dịch. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án D.
0,2 mol X làm mất màu 0,35 mol Br2. Vậy muốn làm mất màu 0,7 mol Br2 cân 0,4 mol X.
Đối với dạng bài hỗn hợp nhiều chất, có thể tìm điểm chung các chất rồi quy về hỗn hợp với số lượng chất ít hơn. Nhưng ở bài này, đề chỉ yêu cầu tính số mol Br2, tức là tính số mol liên kết nên chỉ cần áp dụng các công thức tính nhanh, biến đổi chúng thì có thể giải quyết bài toán.
Câu 31:
Hòa tan hoàn toàn m gam K vào 100 ml dung dịch Y gồm H2SO4 0,5M và HCl 1M, thấy thoát ra 6,72 lít khí (đktc). Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam chất rắn?
 Xem đáp án
Xem đáp án
Đáp án A.
0,1
Vì nên K tác dụng với nước
Cô cạn dung dịch sau phản ứng thu được chất rắn gồm:
Câu 32:
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Cu(OH)2 trong môi trường kiềm. |
Có màu tím. |
|
Y |
Đun nóng với dung dịch NaOH dư, sau đó làm nguội, cho tiếp vài giọt dung dịch CuSO4 |
Xuất hiện màu xanh lam. |
|
Z |
Nước Br2. |
Kết tủa trắng. |
|
T |
Dung dịch AgNO3 trong NH3, đun nóng. |
Kết tủa Ag trắng sáng. |
Dung dịch X, Y, z, T lần lượt là
 Xem đáp án
Xem đáp án
Đáp án A.
X: Lòng trắng trứng (anbumin) là protein nên tham gia phản ứng màu biurê.
Y: Triolein thủy phân trong môi trường kiềm thu được glixerol tác dụng được với CuSO4/NaOH.
Z: Anilin tham gia phản ứng thế với Br2 làm mất màu dung dịch Br2 và tạo kết tủa trắng.
T: Glucozơ chứa nhóm chức anđehit nên tham gia phản ứng tráng bạc.
Câu 33:
Điện phân dung dịch hỗn hợp CuSO4 và KCl bằng dòng điện một chiều có cường độ 5A (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch). Toàn bộ khí sinh ra trong quá trình điện phân (ở cả hai điện cực) theo thời gian được biểu diễn bằng đồ thị dưới.
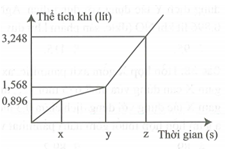
Giá trị của z là
 Xem đáp án
Xem đáp án
Đáp án B.
Dựa vào độ dốc của đồ thị, xác định được:
- Giai đoạn 1: điện phân hết, sinh ra khí Cl2. (1)
- Giai đoạn 2: H2O ở anot điện phân, khí O2 thoát ra. (2)
- Giai đoạn 3: Khí thoát ra rất nhanh nên lúc này H2O ở cả 2 điện cực điện phân, khí O2 và H2 thoát ra.
(1):
(2):
0,04 0,08
0,03 0,12
BT e:
(3):
0,1 0,2 0,04 0,08
2x x y 4y
BT e:
Câu 34:
Hỗn hợp X gồm hai este đều no, mạch hở có cùng số nhóm chức, trong phân tử mỗi este chỉ chứa một loại nhóm chức. Đun nóng 0,2 mol X với dung dịch NaOH vừa đủ, thu được hỗn hợp Y gồm các ancol và hỗn hợp Z gồm hai muối. Dẫn toàn bộ Y qua bình đựng Na dư, thấy khối lượng bình tăng 17,04 gam; đồng thời thoát ra 4,48 lít khí H2 (đktc). Đốt cháy hoàn toàn Z cần dùng 0,52 mol O2, thu được Na2CO3 và 0,78 mol hỗn hợp gồm CO2 và H2O . Phần trăm khối lượng của ancol có khối lượng phân tử lớn nhất trong hỗn hợp Y là
 Xem đáp án
Xem đáp án
Đáp án D.
và 2 este này cùng số nhóm chức nên đây là 2 este 2 chức.
Ta thấy, khi đốt muối, số mol CO2 lớn hơn số mol H2O, mà 2 muối này từ 2 este no, nên trong 2 muối có muối 2 chức.
Vậy các ancol gồm ancol đơn chức và ancol 2 chức đều no.
Với yêu cầu bài này thì không nhất thiết phải tìm công thức 2 muối:
Câu 35:
Nung hỗn hợp gồm m gam Al và 0,04 mol Cr2O3 một thời gian, thu được hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HCl đặc, nóng, vừa đủ thu được 0,1 mol khí H2 và dung dịch Y. Y phản ứng tối đa với 0,56 mol NaOH (biết các phản ứng xảy ra trong điều kiện không có không khí). Giá trị m là
 Xem đáp án
Xem đáp án
Đáp án B.
Đối với hiđroxit của Crom thì chỉ có Cr(OH)3 có tính lưỡng tính, còn Cr(OH)2 thì không.
Câu 36:
Cho các phát biểu sau:
(a) Trong công nghiệp có thể chuyển hoá chất béo lỏng thành chất béo rắn.
(b) Khi thủy phân hoàn toàn saccarozơ, tinh bột và xenlulozơ đều cho một loại monosaccarit.
(c) Độ ngọt của mật ong chủ yếu do glucozơ gây ra.
(d) Một số polime như polietilen, poli(vinyl clorua), poli(metyl metacrylat) được dùng làm chất dẻo.
(e) Các loại dầu thực vật và dầu bôi trơn đều không tan trong nước nhưng tan trong các dung dịch axit.
(g) Các chất (C17H33COO)3C3H5, (C15H31COO)3C3H5 là chất béo dạng lỏng ở nhiệt độ thường.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án B
Những phát biểu đúng: (a), (d).
(a) đúng. Có thể chuyển hóa chất béo lỏng thành chất béo rắn bằng phản ứng hiđro hóa.
(b) sai vì thủy phân saccarozơ thu được glucozơ và fructozơ.
(c) sai vì mật ong có chứa 30% là glucozơ nhưng có chứa 40% là fructozơ.
(e) sai vì dầu thực vật là chất béo nên không tan trong nước nhưng thủy phân trong axit, nhưng dầu bôi trơn là hiđrocacbon nên không tan trong nước, cũng không tan trong axit.
(g) sai vì (C15H31COO)3C3H5 là chất béo no, ở điều kiện thường là chất rắn.
Câu 37:
Hỗn hợp X gồm Cu, Fe2O3 và Fe3O4 trong đó oxi chiếm 52/305 về khối luợng. Cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được dung dịch Y có tổng khối lượng chất tan là 39,42 gam và còn 5,12 gam chất rắn không tan. Lọc bỏ chất rắn rồi cho dung dịch Y tác dụng với dung dịch AgNO3 dư thụ được m1 gam hỗn hợp kết tủa và có 0,896 lít khí NO (đktc, sản phẩm khử duy nhất của N) thoát ra. Giá trị của m1 gần nhất với
 Xem đáp án
Xem đáp án
Đáp án D
Dung dịch Y tác dụng với AgNO3 có thoát khí NO, chứng tỏ trong Y còn ion H+
Ta có:
BTĐT:
Từ (1) (2) (3)
Câu 38:
Hỗn hợp X gồm axit panmitic, axit stearic và một triglixerit. Đốt cháy hoàn toàn m gam X cần dùng vừa đủ 7,675 mol O2, thu được H2O và 5,35 mol CO2. Mặt khác, cho m gam X tác dụng với dung dịch chứa 0,3 mol NaOH, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối gồm natri panmitat và natri steatat. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án A
Xem hỗn hợp X gồm:
Câu 39:
Cho sơ đồ biến hóa sau:

Trong các phản ứng trên có bao nhiêu phản ứng oxi hóa - khử?
 Xem đáp án
Xem đáp án
Đáp án B
A có mùi trứng thối nên A là H2S, suy ra X là S.
(1)
(2)
(3)
(4)
(5)
(6)
Những phản ứng oxi hóa khử: (1), (2), (3), (4), (5).
Câu 40:
Cho 48,05 gam hỗn hợp E gồm chất hữu cơ mạch hở X (CnH2n+1O4N) và este hai chức Y (C4H6O4) (có tỉ lệ mol tương ứng là 3:4) tác dụng hết với dung dịch NaOH vừa đủ, đun nóng. Kết thúc phản ứng, thu được hỗn hợp Z gồm hai ancol đơn chức kế tiếp nhau trong dãy đồng đẳng và m gam hỗn hợp ba muối khan (đều có cùng số cacbon trong phân tử, trong đó có hai muối của axit cacboxylic). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D.
E tác dụng với NaOH thu được ancol đơn chức nên Y có công thức: (COOCH3)2
Ancol còn lại là: C2H5OH
X là: CH3COONH3CH2COOC2H5
