Đề thi THPT Quốc gia môn Hóa học năm 2022 chọn lọc, có lời giải (20 đề)
Đề thi THPT Quốc gia môn Hóa học năm 2022 chọn lọc, có lời giải (Đề số 4)
-
26003 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại kiềm thổ nào sau đây không phản ứng với nước ở nhiệt độ thường?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Các kim loại kiềm thổ gồm: Be, Mg, Ca, Sr, Ba.
+ Ở điều kiện thường: Ca, Sr và Ba tác dụng được với nước.
+ Mg phản ứng chậm ở nhiệt độ thường, phản ứng nhanh khi đun nóng.
+ Be không phản ứng ở bất kì nhiệt độ nào.
Câu 2:
Dung dịch amin nào sau đây không làm quỳ tím chuyển màu xanh?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Amin thơm không làm đổi màu quỳ tím do có tính bazơ yếu.
Câu 3:
Trong các kim loại sau, kim loại dễ bị oxi hóa nhất là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Kim loại dễ bị oxi hóa nhất là kim loại có tính khử mạnh nhất. Trong dãy điện hóa, theo chiều từ trái sang phái, tính khử của kim loại giảm dần. Do đó kim loại có tính khử mạnh nhất là K.
Câu 4:
Chất nào sau đây thuộc loại hiđrocacbon không no?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Meatn, etan và butan thuộc dãy đồng đẳng của ankan là hiđrocacbon no.
Etilen thuộc dãy đồng đẳng của anken, là hiđrocacbon không no.
Câu 5:
Stiren (vinylbenzen) có công thức phân tử là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Vinyl benzen : C6H5-CH=CH2 CTPT: C8H8.
Câu 6:
Dung dịch nào sau đây hòa tan được Cr(OH)3?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Cr(OH)3 là hiđroxit lưỡng tính nên có thể hòa tan được trong dung dịch kiềm và axit.
Câu 7:
Độ dinh dưỡng của phân kali được tính theo
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Độ dinh dưỡng của các loại phân bón được tính như sau:
+ phân đạm: tính theo %N.
+ phân lân: tính theo %P2O5.
+ phân kali: tính theo %K2O.
Câu 8:
Thủy phân 1 mol (C17H35COO)C3H5(OOCC15H31)2 trong dung dịch NaOH, thu được a mol muối natri stearat. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
(C17H35COO)C3H5(OOC-C15H31)2 + 3NaOH C17H35COONa + 2C15H31COONa+ C3H5(OH)3
Câu 10:
Dung dịch nào sau đây không làm đổi màu quỳ tím?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Các aminoaxit có số nhom NH2 và số mol COOH bằng nhau thì không làm đổi màu quỳ tím.
Câu 11:
Dùng kim loại nào sau đây để điều chế Ag từ dung dịch AgNO3 bằng phương pháp thủy luyện?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Phương pháp thủy luyện dựa trên nguyên tắc: dùng kim loại có tính khử mạnh hơn đẩy kim loại có tính khử yếu hơn ra khỏi muối nhưng không xét với các kim loại tan trong nước.
Câu 12:
Kim loại phản ứng với dung dịch HCl và dung dịch NaOH tạo thành muối là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Trong số các kim loại đã cho chỉ có Al có khả năng phản ứng với cả axit và bazơ.
2Al + 6HCl 2AlCl3 +3 H2
2Al+ 2NaOH + 2H2O 2NaAlO2 + 3H2
Câu 13:
Hematit nâu là một loại quặng sắt quan trọng dùng để luyện gang, thép. Thành phần chính của quặng hematit nâu là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Trong tự nhiên sắt tồn tại trong các quặng:
Quặng hematit đỏ (Fe2O3), quặng hematit nâu (Fe2O3.nH2O),
quặng manhetit (Fe3O4, là quặng giàu sắt nhất nhưng hiếm gặp),
quặng xiđerit (FeCO3), quặng pirit (FeS2).
Câu 15:
Một trong những nguyên nhân chính gây ra sự suy giảm tầng ozon là do
 Xem đáp án
Xem đáp án
Chọn đáp án C
Câu 16:
Oxit nào sau đây tác dụng với dung dịch H2SO4 loãng sinh ra hỗn hợp muối?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Fe3O4 + 4H2SO4 FeSO4 + Fe2(SO4)3 + 4H2O
Câu 18:
Cho dung dịch NaHCO3 tác dụng với dung dịch Ca(OH)2 loãng dư, thu được kết tủa X và dung dịch Y. Thành phần của dung dịch Y gồm:
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
NaHCO3+ Ca(OH)2 CaCO3 + NaOH + H2O
Kết tủa là CaCO3. Dung dịch Y gồm NaOH và Ca(OH)2 dư.
Câu 19:
Số hợp chất là đồng phân cấu tạo, có cùng công thức phân tử C4H8O2, tác dụng được với dung dịch NaOH nhưng không tác dụng được với Na là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Hợp chất tác dụng với NaOH và không tác dụng với Na là este. Các CTCT của C4H8O2 gồm:
HCOO-CH2-CH2-CH3 HCOO-CH(CH3)-CH3
CH3COO-CH2-CH3 C2H5COOCH3
Câu 20:
Một miếng kim loại bằng bạc bị bám một lớp kim loại sắt ở bề mặt, ta có thể dùng lượng dư dung dịch nào sau đây để loại bỏ tạp chất ra khỏi tấm kim loại bằng bạc?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Để làm sạch sắt thì cần dùng các dung dịch có thể tác dụng với Fe mà không tác dụng với Ag, đồng thời không sinh ra kim loại mới.
CuSO4, NiSO4 đều hòa tan được Fe tuy nhiên sau khi phản ứng lại sinh ra kim loại mới nên không thỏa mãn.
Câu 21:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
A sai, tơ visco thuộc loại tơ bán tổng hợp.
B đúng.
C sai, tơ lapsan thuộc loại polieste.
D sai, cao su Buna-N được điều chế bằng phản ứng đồng trùng hợp buta-1,3-đien và acrilonitrin
Câu 22:
Cho các polime: poli(hexametylen–ađipamit), poliacrilonitrin, poli(butađien-stien), polienantoamit, poli(metyl metacrylat), teflon. Số polime được điều chế bằng phản ứng trùng hợp là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Polime được điều chế bằng phản ứng trùng hợp khi monome ban đầu thỏa mãn điều kiện:
+ Có liên kết đôi.
+ Có vòng kém bền
Câu 23:
Cho 11,25 gam C2H5NH2 tác dụng với 200 ml dung dịch HCl a(M). Sau khi phản ứng hoàn toàn thu được dung dịch có chứa 22,2 gam chất tan. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Câu 24:
Cho các chất sau: glucozơ, fructozơ, saccarozơ, tinh bột, xenlulozơ. Những chất khi phản ứng với dung dịch AgNO3/NH3 tạo thành Ag là:
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Trong số các cacbohiđrat chỉ có glucozơ và fructozơ có khả năng phản ứng với AgNO3/NH3 tạo thành Ag.
Câu 25:
Đốt cháy hoàn toàn m gam Al trong khí O2 lấy dư, thu được 10,2 gam Al2O3. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Câu 26:
Người ta điều chế C2H5OH từ xenlulozơ với hiệu suất chung của cả quá trình là 60% thì khối lượng C2H5OH thu được từ 32,4 gam xenlulozơ là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Câu 27:
Cho 1,17 gam kim loại kiềm R tác dụng với H2O (dư), thu được 336 ml khí H2 (đktc). R là
 Xem đáp án
Xem đáp án
Chọn đáp án A
Giải thích:
Câu 28:
Xà phòng hóa hoàn toàn m gam hỗn hợp E gồm các triglixerit bằng dung dịch NaOH, thu được glixerol và hỗn hợp X gồm ba muối C17HxCOONa, C15H31COONa, C17HyCOONa có tỉ lệ mol tương ứng là 3 : 4 : 5. Hiđro hóa hoàn toàn m gam E, thu được 68,96 gam hỗn hợp Y. Nếu đốt cháy hoàn toàn m gam E thì cần vừa đủ 6,14 mol O2. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Câu 29:
Hòa tan hoàn toàn 15,74 gam hỗn hợp X chứa Na, K, Ca và Al trong nước dư, thu được dung dịch chứa 26,04 gam chất tan và 9,632 lít khí H2 (đktc). Phần trăm khối lượng của Al trong X là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Câu 30:
Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu vào 300 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và 3,2 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 51,15 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, giá trị của m gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Câu 31:
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch chứa 4a mol HCl vào dung dịch chứa a mol NaAlO2.
(b) Cho Al2O3 dư vào lượng dư dung dịch NaOH.
(c) Cho Mg dư vào dung dịch HNO3 (phản ứng không thu được chất khí).
(d) Cho Fe vào dung dịch Fe2(SO4)3 dư.
(e) Cho dung dịch chứa a mol KHSO4 vào dung dịch chứa a mol NaHCO3.
Sau khi các phản ứng xảy ra hoàn toàn thì số thí nghiệm thu được dung dịch chứa hai muối là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Các thí nghiệm thu được dung dịch chứa hai muối là: a, c, d, e.
(a) HCl+ NaAlO2+ H2O NaCl + Al(OH)3
Al(OH)3 + 3HCl AlCl3+ 3H2O
Hai muối thu được là NaCl và AlCl3.
(b) Vì phản ứng không sinh ra khí nên sản phẩm khử là NH4NO3.
4Mg+10HNO3 4Mg(NO3)2 + NH4NO3+3 H2O
(c) Fe+ Fe2(SO4)3 FeSO4
Hai muối thu được là FeSO4 và Fe2(SO4)3 dư.
(d) KHSO4 + NaHCO3 K2SO4 + Na2SO4 + CO2 + H2
Câu 32:
Cho các phát biểu sau:
(a) Dầu mỡ sau khi sử dụng, có thể được dùng để tái chế thành nhiên liệu.
(b) Đipeptit Gly-Ala có phản ứng màu biure.
(c) Thủy phân vinyl fomat, thu được hai sản phẩm đều có phản ứng tráng bạc.
(d) Phenylamin tan ít trong nước nhưng tan tốt trong dung dịch NaOH
(e) Oligopeptit gồm các peptit có từ 2 đến 10 gốc α-amino axit và là cơ sở tạo nên protein.
(g) Thủy phân hoàn toàn chất béo bằng cách đun nóng với dung dịch NaOH dư luôn thu được sản phẩm gồm xà phòng và muối natri của glixerol.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Các phát biểu đúng là a và c.
(b) sai vì từ tripeptit trở lên mới có phản ứng màu biure.
(d) sai vì phenylamin (anilin) không tan trong nước và bazơ, tan được trong dung dịch axit.
(e) protein được tạo nên từ các chuỗi polipeptit.
(g) sai, thủy phân chất béo trong NaOH dư thu được xà phòng và glixerol
Câu 33:
Từ chất X (C10H10O4, chỉ có một loại nhóm chức) tiến hành các phản ứng (theo đúng tỉ lệ mol) như sau:
(a) X + 3NaOH Y + Z + T + H2O
(b) 2Y + H2SO4 → 2E + Na2SO4
(c) 2E + C2H4(OH)2 G + 2H2O
Biết MY < MZ < MT < 148, Y và Z là muối của axit cacboxylic. Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
A đúng vì: CH3COONa + NaOH CH4 + Na2CO3.
B đúng vì T có nhóm OH nên phản ứng được với Na.
C sai vì G có 6 nguyên tử H.
D đúng
Câu 34:
Hỗn hợp E gồm hai este đơn chức, là đồng phân cấu tạo, đều chứa vòng benzen. Đốt cháy hoàn toàn m gam E cần vừa đủ 21,06 lít khí O2 (đktc), thu được 35,2 gam CO2 và 7,2 gam H2O. Biết E phản ứng hoàn toàn với dung dịch chứa 5 gam NaOH, thu được 15,75 gam ba muối và m gam ancol. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Câu 35:
Hỗn hợp X gồm M và R2O trong đó M là kim loại kiềm thổ và R là kim loại kiềm. Cho m gam hỗn hợp X tan hết vào 58,4 gam dung dịch HCl 12%, thu được dung dịch Y chứa 15,312 gam các chất tan có cùng nồng độ mol. Biết Y chỉ chứa 1 loại anion. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
Câu 36:
Cho 38,55 gam hỗn hợp X gồm Mg, Al, ZnO và Fe(NO3)2 tan hoàn toàn trong dung dịch chứa 0,725 mol H2SO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 96,55 gam muối sunfat trung hòa (không chứa Fe3+) và 3,92 lít (đktc) khí Z gồm hai khí trong đó có một khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với H2 là 9. Phần trăm số mol của Al trong hỗn hợp X gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Câu 37:
X là hỗn hợp chứa một axit đơn chức, một ancol hai chức và một este hai chức (đều no, mạch hở). Đốt cháy hoàn toàn 0,09 mol X cần 10,752 lít khí O2 (đktc). Sau phản ứng thấy khối lượng của CO2 lớn hơn khối lượng của H2O là 10,84 gam. Mặt khác, 0,09 mol X tác dụng vừa hết với 0,1 mol KOH. Cô cạn dung dịch sau phản ứng thu được m gam muối khan và một ancol có 3 nguyên tử C trong phân tử. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Câu 38:
Hỗn hợp X chứa một amin no, đơn chức, mạch hở và một anken. Đốt cháy hoàn toàn 0,4 mol hỗn hợp X, thu được N2, 33,6 lít CO2 (đktc) và 35,1 gam H2O. Biết số nguyên tử cacbon trong amin lớn hơn trong anken. Cho toàn bộ lượng amin có trong 0,4 mol X tác dụng vừa đủ với HCl, thu được m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn đáp án D
Giải thích:
Câu 39:
Điều chế este CH3COOC2H5 trong phòng thí nghiệm được mô tả theo hình vẽ sau :
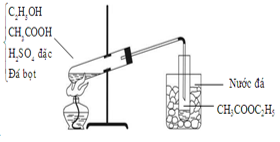
Cho các phát biểu sau:
(a) Etyl axetat có nhiệt độ sôi thấp (77°C) nên dễ bị bay hơi khi đun nóng.
(b) H2SO4 đặc vừa làm chất xúc tác, vừa có tác dụng hút nước.
(c) Etyl axetat qua ống dẫn dưới dạng hơi nên cần làm lạnh bằng nước đá để ngưng tụ.
(d) Khi kết thúc thí nghiệm, cần tắt đèn cồn trước khi tháo ống dẫn hơi etyl axetat.
(e) Vai trò của đá bọt là để bảo vệ ống nghiệm không bị vỡ.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn đáp án C
Giải thích:
Các phát biểu đúng là a,b,c,d.
(d) đúng vì tắt đèn cồn trước để tránh hiện tượng este sinh ra còn trong ống dẫn hơi gây cháy.
(e) sai, đá bọt có tác dụng giúp hỗn hợp chất lỏng sôi êm dịu.
Câu 40:
Cho 0,2 mol hỗn hợp E gồm chất X (CnH2n+4O4N2) và chất Y (CmH2m+3O2N) đều mạch hở tác dụng vừa đủ với 0,25 mol NaOH, đun nóng, thu được hỗn hợp sản phẩm hữu cơ gồm 21,25 gam hỗn hợp X gồm hai muối và 5,5 gam hỗn hợp hai khí làm quỳ tím ẩm hóa xanh có tỉ khối so với H2 là 13,75. Khối lượng nhỏ nhất của X có thể đạt được trong 0,2 mol E gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn đáp án B
Giải thích:
