Đề thi THPT Quốc gia môn Hóa học năm 2022 chọn lọc, có lời giải (20 đề)
Đề thi THPT Quốc gia môn Hóa học năm 2022 chọn lọc, có lời giải (Đề số 20)
-
25770 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 3:
Phương pháp nào sau đây được dùng để điều chế những kim loại có độ hoạt động hóa học thấp (như Au, Ag, Cu…) hay còn gọi là phương pháp ướt?
 Xem đáp án
Xem đáp án
Đáp án A. Thủy luyện.
Câu 5:
Natri clorua là gia vị quen thuộc đối với cuộc sống. Công thức của natri clorua là
 Xem đáp án
Xem đáp án
Đáp án B. NaCl.
Câu 9:
Kim loại X tan trong dung dịch HCl nhưng không tan trong dung dịch H2SO4 đặc, nguội. X là
 Xem đáp án
Xem đáp án
Đáp án C. Al.
Câu 12:
Một nguyên nhân gây ngộ độc khi uống rượu là do rượu uống có lẫn metanol. Công thức của metanol là
 Xem đáp án
Xem đáp án
Đáp án C. CH3OH.
Câu 13:
Thủy phân etyl butirat trong dung dịch NaOH, đun nóng thu được ancol có công thức là
 Xem đáp án
Xem đáp án
Đáp án C. C2H5OH.
Câu 16:
Cho dãy chất: alanin, valin, lysin và axit glutamic. Số chất trong dãy mà phân tử có 1 nhóm -NH2 và 1 nhóm -COOH là
 Xem đáp án
Xem đáp án
Đáp án B. 2.
Câu 18:
Polime nào sau đây không chứa nguyên tố nitơ trong thành phần phân tử?
 Xem đáp án
Xem đáp án
Đáp án B. Polietilen.
Câu 19:
Dung dịch nào sau đây làm phenolphtalein chuyển từ không màu thành màu hồng?
 Xem đáp án
Xem đáp án
Đáp án D. Ba(OH)2.
Câu 20:
Đốt cháy hoàn toàn chất nào sau đây sẽ thu được số mol H2O bằng số mol CO2?
 Xem đáp án
Xem đáp án
Đáp án B. Etilen.
Câu 21:
Hòa tan hoàn toàn Fe3O4 trong dung dịch H2SO4 loãng (dư) thu được dung dịch X, cho dung dịch NaOH dư vào dung dịch X thu được kết tủa Y, nung Y trong không khí đến khối lượng không đổi thu được chất rắn Z, thành phần của chất rắn Z là
 Xem đáp án
Xem đáp án
Đáp án C. Fe2O3.
Câu 22:
Cho các loại tơ: capron, xenlulozơ axetat, tơ tằm, nitron, nilon-6,6. Số tơ thuộc loại poliamit là
 Xem đáp án
Xem đáp án
Đáp án D. 3.
Câu 23:
Hòa tan 2,99 gam kim loại kiềm M vào nước dư, thu được 1,456 lít H. Kim loại M là
 Xem đáp án
Xem đáp án
Đáp án C. Na.
Câu 24:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án C. Kim loại cứng nhất là Ag, kim loại dẫn điện tốt nhất là Cr.
Câu 25:
Cho 9,125 gam dung dịch HCl 10% tác dụng với 1,5 gam glyxin (NH2-CH2-COOH), sau phản ứng thu được m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B. 2,230.
Câu 26:
Hợp chất X có công thức phân tử C5H8O2, khi tham gia phản ứng xà phòng hóa thu được một anđehit và một muối của axit cacboxylic. Số đồng phân cấu tạo thỏa mãn tính chất trên của X là
 Xem đáp án
Xem đáp án
Đáp án D. 4.
Câu 27:
Hợp chất X là một cacbohiđrat có trong hầu hết các bộ phận của cây như lá, hoa, rễ, … và nhất là trong quả nho chín (còn gọi là đường nho). Phát biểu nào sau đây về X là đúng?
 Xem đáp án
Xem đáp án
Đáp án C. Dung dịch X có thể hòa tan được Cu(OH)2 tạo thành dung dịch xanh lam.
Câu 28:
Thủy phân hoàn toàn m kilogam tinh bột thu được glucozơ, lên men rượu toàn bộ lượng glucozơ thu được 5 lít dung dịch C2H5OH 46o. Biết các phản ứng xảy ra hoàn toàn, khối lượng riêng của C2H5OH là 0,8 gam/ml. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A. 3,24.
Câu 29:
Nung 21,6 gam hỗn hợp Mg và Fe trong không khí, thu được 27,2 gam hỗn hợp X gồm các oxit và kim loại dư. Hòa tan hết X cần vừa đủ 550 ml dung dịch HCl 2M, thu được V lít khí H2 (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D. 4,48.
Câu 31:
Hấp thụ hết V hoặc 3V lít khí CO2 (đktc) vào dung dịch X chứa 0,2 mol NaOH và 0,15 mol Ba(OH)2, thu được m gam kết tủa. Mặt khác, hấp thụ hết 2V lít khí CO2 (đktc) vào dung dịch X, thu được 1,2m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn A.
Dung dịch X có chứa Ba2+ (0,15 mol), OH- (0,5 mol)
Câu 32:
Thực hiện các thí nghiệm sau:
(a) Cho hỗn hợp Ba và Al (có tỉ lệ mol tương ứng 1: 2) vào H2O dư.
(b) Cho hỗn hợp bột Cu và Fe3O4 (có tỉ lệ mol tương ứng 1 : 1) và dung dịch H2SO4 loãng, dư.
(c) Cho hỗn hợp bột Cu và Fe(OH)3 (có tỉ lệ mol tương ứng 1 : 1) vào dung dịch HCl loãng, dư.
(d) Cho hỗn hợp Al và Fe (có tỉ lệ mol tương ứng 1 : 1) vào dung dịch HNO3 đặc, nguội.
(e) Cho Ba và NaHCO3 (tỉ lệ mol 2 : 1) vào nước dư.
Sau khi các phản ứng xảy ra hoàn toàn, có bao nhiêu thí nghiệm có sự hòa tan chất rắn?
 Xem đáp án
Xem đáp án
Chọn C.
(a) Đúng. Hỗn hợp Ba và Al (tỉ lệ mol 1 : 1) tan hết trong nước dư.
(b) Đúng. Hỗn hợp Cu và Fe3O4 (tỉ lệ mol 1 : 1) hòa tan hết trong dung dịch H+ dư.
(c) Sai. Hỗn hợp Cu và Fe(OH)3 (tỉ lệ mol 1 : 2) hòa tan hết trong dung dịch H+ dư.
(d) Sai. Hỗn hợp Al và Fe không tan trong HNO3 đặc, nguội.
(e) Sai. Hỗn hợp Ba và NaHCO3 hòa tan vào nước thu được kết tủa BaCO3.
Câu 33:
Hỗn hợp X gồm 2 triglixerit. Đun nóng m gam hỗn hợp X với dung dịch NaOH vừa đủ, thu được hỗn hợp Y chứa các muối C17H33COONa, C17H31COONa, C15H31COONa. Dốt m gam hỗn hợp X thu được 1,662 mol CO2 và 1,488 mol H2O. Mặt khác, m gam X tác dụng tối đa với 0,114 mol Br2 trong dung dịch. Phần trăm khối lượng C15H31COONa trong Y gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D.
Đặt x, k là số mol và số liên kết pi của X.
= x.(k – 3) = 0,114 và = x.(k – 1) = 1,662 – 1,488 Þ x = 0,03; k = 6,8
Muối gồm C17H33COONa (a mol), C17H31COONa (b mol) và C15H31COONa (c mol)
Câu 34:
Cho các phát biểu sau:
(a) Tơ nilon-6,6 có chứa liên kết peptit.
(b) Khử glucozơ bằng H2 (xúc tác Ni, đun nóng) thu được sobitol.
(c) Xăng E5 là xăng sinh học được pha 5% etanol, 95% còn lại là xăng Ron A92 “truyền thống”.
(d) Triolein hòa tan được Cu(OH)2 tạo dung dịch màu xanh.
(e) Polipeptit là những phân tử peptit chứa từ 2 đến 10 gốc α-amino axit.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn D.
(a) Sai. Tơ nilon-6,6 có chứa liên kết amit.
(d) Sai. Triolein không hòa tan được Cu(OH)2.
(e) Sai. Polipeptit là những phân tử peptit chứa từ 11 đến 50 gốc α-amino axit.
Câu 35:
Hỗn hợp X gồm Na, K, Na2O và K2O. Hòa tan hoàn toàn 25,7 gam X vào nước dư, thu được 3,36 lít khí H2 (đktc) và dung dịch Y (trong đó có 22,4 gam KOH). Hòa tan hết 0,4 mol H3PO4 vào Y, thu được dung dịch Z. Cô cạn dung dịch Z, thu được m gam rắn khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
Khi cho KOH (0,4 mol), NaOH (0,3 mol) vào 0,4 mol H3PO4 thì:
BTKL: 0,4.56 + 0,3.40 + 0,4.98 = m + 18.0,7 (với ) m = 61 (g).
Câu 36:
Hỗn hợp X gồm glucozơ, lysin và hexametylenđiamin. Đốt chát hoàn toàn 0,2 mol X cần dùng 1,46 mol O2, sản phẩm cháy gồm CO2, H2O và N2 được dẫn qua bình đựng H2SO4 đặc nóng (dư), khí thoát ra khỏi bình có thể tích là 28,672 lít. Mặt khác, cho 24,06 gam X trên vào dung dịch HCl loãng dư thu được dung dịch Y có chứa m gam các chất hữu cơ. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
X chứa C6H12O6, C6H14N2O2, C6H16N2 với số mol tương ứng là a, b, c
Ta có: a = 0,12 mol và b = c = 0,04 mol
mX = 32,08 gam và nHCl = 2b + 2c = 0,16 m chất hữu cơ = mX + mHCl = 37,92 gam
Trong 24,06 gam X phản ứng với HCl có: 37,92.(32,08 : 24,06) = 28,44 gam chất hữu cơ.
Câu 37:
Hòa tan hỗn hợp X gồm 0,35 mol Mg, 0,1 mol Fe, MgCO3 và Mg(NO3)2 trong dung dịch chứa 0,05 mol HNO3 và 1,49 mol NaHSO4, thu được dung dịch Y chỉ chứa 198,21 gam các muối trung hòa và 0,3 mol hỗn hợp Z gồm 4 khí không màu không hóa nâu trong không khí; có tỉ khối so với H2 bằng 539/30. Cho dung dịch NaOH cho đến dư vào Y, lấy lượng kết tủa thu được nung nóng trong không khí đến khối lượng không đổi thu được 32 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Số mol N2 trong hỗn hợp khí Z là
 Xem đáp án
Xem đáp án
Chọn B.
Hỗn hợp khí Z gồm H2 (x mol), CO2 (y mol), N2 (z mol), N2O (t mol)
x + y + z + t = 0,3 (1) và 2x + 44y + 28z + 44t = 10,78 (2)
Chất rắn gồm Fe2O3 (0,05 mol) và MgO nMgO = 0,6 mol
(thay (1) vào biểu thức để tính)
Ta có:
và mmuối =
Thay vào (1), (2), (3) suy ra: x = 0,05 ; y = 0,2 ; z = 0,02 ; t = 0,03.
Câu 38:
Hỗn hợp X gồm các amin no và các hiđrocacbon không no (trong đó hiđro chiếm khối lượng của X và các chất trong X đều mạch hở). Cho 12,76 gam X tác dụng tối đa với 0,48 mol H2. Mặt khác, đốt cháy a mol X cần dùng 0,525 mol O2, thu được CO2, H2O, N2 trong đó tổng khối lượng CO2 và N2 là 17,24 gam. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn B.
Trong a mol X chứa C (x mol), H (y mol), N (z mol)
Theo đề ta có: mH = y =
Bảo toàn electron: 4x + y = 0,525.4 và mCO2 + mN2 = 44x + 14z = 17,24
x = 0,36; y = 0,66; z = 0,1 mX = 6,38 gam
Để làm no 12,76 gam X cần 0,48 mol H2
Để làm no 6,38 gam X cần 0,24 mol H2 X’: C (0,36 mol), N (0,1 mol) và H (0,66 + 0,24.2 = 1,14 mol)
X’ gồm các amin và ankan nên:
Amin = ?CH2 + ?NH + H2
Ankan = ?CH2 + H2
Quy đổi X’ thành CH2 (0,36), NH (0,1), bảo toàn H nH2 = 0,16
nX = nX’ = nAmin + nAnkan = 0,16 mol.
Câu 39:
Hỗn hợp X gồm ba este mạch hở đều tạo bởi axit cacboxylic với ancol, trong đó hai este có cùng số nguyên tử cacbon trong phân tử. Xà phòng hóa hoàn toàn 40,2 gam X bằng dung dịch NaOH vừa đủ, thu được 22,0 gam hỗn hợp Y gồm hai ancol đơn chức, kế tiếp trong dãy đồng đẳng và hỗn hợp Z gồm hai muối. Cho toàn bộ Y vào bình dung dịch H2SO4 đặc ở 140oC để chuyển hết toàn bộ ancol thành ete thì thấy có 16,6 gam ete tạo ra. Đốt cháy hoàn toàn Z cần vừa đủ 0,45 mol O2, thu được Na2CO3, CO2 và H2O. Phần trăm khối lượng của este có phân tử khối nhỏ nhất trong X là
 Xem đáp án
Xem đáp án
Chọn A.
Xử lí hỗn hợp Y: mY = mete +
Khi đốt cháy Z thu được Na2CO3 (a mol) CO2 (b mol) và H2O (c mol)
và
Khi cho X tác dụng với NaOH, theo BTKL: 40,2 + 40.0,6 = 22 + 44b + 18c + 17,4 (2)
Từ (1), (2) suy ra: b = 0,4; c = 0,4
Vì b = c nên các muối đều là no, đơn chức
Các este gồm HCOOCH3 (0,3 mol), CH3COOCH3 (0,1 mol), HCOOC2H5 (0,2 mol)
= 44,78%.
Câu 40:
Tiến hành thí nghiệm chứng minh tính chất hóa học của etanol theo các bước sau:
Bước 1: Đốt nóng sợi dây đồng đã cuộn thành lò xo trên ngọn lửa đèn cồn đến khi ngọn lửa không còn màu xanh (Hình 1).
- Bước 2: Nhúng nhanh sợi dây đồng đang nóng vào ống nghiệm đựng etanol và lặp lại vài lần (Hình 2). Kết thúc bước 2, thu được dung dịch Y.
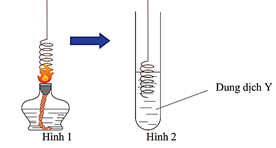
Cho các phát biểu sau:
(a) Ở bước 2, dây đồng chuyển từ màu đỏ sang màu đen.
(b) Dung dịch Y có màu xanh của muối đồng(II).
(c) Thí nghiệm trên chứng tỏ etanol có tính oxi hóa.
(d) Dung dịch Y có khả năng tham gia phản ứng tráng bạc.
(e) Trong thí nghiệm trên, nếu thay dây đồng bằng dây sắt thì hiện tượng xảy ra tương tự.
Trong số các phát biểu trên, có bao nhiêu phát biểu đúng?
 Xem đáp án
Xem đáp án
Chọn A.
Phương trình: 2Cu + O2 2CuO
C2H5OH + CuO CH3CHO + Cu + H2O
(a) Sai. Ở bước 2, dây đồng chuyển từ màu đen (CuO) sang màu đỏ (Cu).
(b) Sai. Dung dịch Y không màu.
(c) Sai. Thí nghiệm trên chứng tỏ etanol bị oxi hóa bởi CuO thành anđehit.
(e) Sai. Thí nghiệm chỉ áp dụng cho trường hợp của đồng.
