Bộ 25 đề thi thử THPT Hóa học có lời giải năm 2022 (Đề 3)
-
4528 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 2:
 Xem đáp án
Xem đáp án
Đáp án D
Al2O3 là hợp chất lưỡng tính nên tác dụng được với dung dịch axit và dung dịch bazơ.
Câu 3:
Chất nào sau đây thuộc polisaccarit?
 Xem đáp án
Xem đáp án
Đáp án A
Cacbohiđrat được chia thành:
Monosaccarit: Glucozơ và fructozơ.
Đisaccarit: Saccarozơ.
Polisaccarit: Tinh bột và xenlulozơCâu 4:
Kim loại nào dưới đây không phản ứng được với H2O ở nhiệt độ thường?
 Xem đáp án
Xem đáp án
Đáp án B
Các chất tác dụng được với nước ở nhiệt độ thường gồm các kim loại kiềm, kim loại kiềm thổ (trừ Be).
Chú ý: Mg phản ứng chậm với nước ở nhiệt độ thường.
Câu 5:
 Xem đáp án
Xem đáp án
Đáp án B
Trong dãy điện hóa của kim loại, từ trái sang phải, tính oxi hóa của các ion kim loại tăng dần.
→ Tính oxi hóa:
Câu 6:
Poli(vinyl doma) (PVC) được điều chế từ phản ứng trùng hợp chất nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Poli(vinyl doma) được điều chế từ monome tương ứng là vinyl clorua có công thức: CH2 = CHCl.
Câu 7:
Sắt bị thụ động trong dung dịch axit nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Các kim loại bị thụ động trong dung dịch HNO3 đặc, nguội và H2SO4 đặc, nguội là Al, Fe, Cr.
Câu 8:
Chất hữu cơ X tác dụng được với dung dịch HCl và khi X tác dụng với dung dịch brom tạo kết tủa. Tên gọi của X là
 Xem đáp án
Xem đáp án
Đáp án A
Chất hữu cơ X tác dụng được với dung dịch HCl nên X có thể là anilin, alanin, etylamin.
Tuy nhiên khi X tác dụng với dưng dịch brom tạo kết tủa nên X là anilin.
Câu 9:
Một chiếc nhiệt kế bị vỡ, để thu hồi thủy ngân rơi vãi tránh độc, người ta có thể dùng
 Xem đáp án
Xem đáp án
Đáp án C
Người ta dùng bột lưu huỳnh để thu hồi thủy ngân rơi vãi do lưu huỳnh tác dụng được với thủy ngân ngay ở nhiệt độ thường:
Câu 10:
Hòa tan hết m gam bột nhôm trong dung dịch HCl dư, thu được 0,16 mol H2. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 11:
 Xem đáp án
Xem đáp án
Đáp án A
Điều kiện để các ion có thể cùng tồn tại trong một dung dịch là khi các ion đó kết hợp với nhau không tạo ra kết tủa hoặc bay hơi hoặc chất điện li yếu.
A đúng.
B sai vì có phương trình hỏa học Ca2+ + → CaCO3
C sai vì có phương trình hóa học H+ + → CO2 + H2O
D sai vì có phương trình hóa học + OH– → NH3 + H2O
Câu 12:
 Xem đáp án
Xem đáp án
Đáp án B
Gọi công thức phân tử của ankan là .
Ta có:
→ Công thức phân tử của ankan là C3H8.
Câu 13:
Chất nào sau đây không tạo kết tủa khi tác dụng với dung dịch Na3PO4?
 Xem đáp án
Xem đáp án
Đáp án D
Chỉ có muối photphat của kim loại kiềm và amoni là tan được còn lại thì muối của các kim loại khác đều không tan nên CaCl2, Mg(HCO3)2, AgNO3 đều tạo kết tủa với Na3PO4.
Chỉ có HCl là không tạo kết tủa với Na3PO4.
Câu 14:
Trong phòng thí nghiệm, để xử lí sơ bộ một số chất thải ở dạng dung dịch chứa ion Fe2+ và Cu2+ ta dùng lượng dư
 Xem đáp án
Xem đáp án
Đáp án A
Người ta dùng lượng dư nước vôi trong do dễ kiếm, hiệu quả và rẻ tiền:
Fe2+ + 2OH– → Fe(OH)2↓
Cu2+ + 2OH– → Cu(OH)2↓Câu 15:
Thủy phân este nào sau đây trong dung dịch NaOH vừa đủ thu được natri axetat và ancol?
 Xem đáp án
Xem đáp án
Đáp án D
Thủy phân este thu được natri axetat nên dựa vào đáp án este đó có dạng CH3COOR’
→ Loại B, C.
Lại có sau phản ứng thu đươc ancol → Loại A vì có phương trình hóa học:
CH3COOCH = CH2 + NaOH → CH3COONa + CH3CHO
(anđehit axetic)
D đúng vì có phương trình hóa học:
CH3COOCH3 + NaOH → CH3COONa + CH3OH
(ancol metylic)
Câu 16:
 Xem đáp án
Xem đáp án
Đáp án A
Chất Y được điều chế từ hỗn hợp chất lỏng → Loại B, D (do Cu(OH)2, CaC2 là chất rắn). Khi thu Y cần sử dụng nước đá Y là chất dễ bay hơi → Loại C
Câu 17:
 Xem đáp án
Xem đáp án
Đáp án A
;;
Xét tỉ lệ: Thu được hai muối và .
Phương trình hóa học: Ba2+ + → BaCO3
0,1 0,05 →0,05 mol
Câu 18:
 Xem đáp án
Xem đáp án
Đáp án D
D sai vì saccarozơ được tạo bởi hai monosaccarit là glucozơ và fructozơ.
Câu 19:
X là một -amino axit chứa một nhóm NH2. Cho m gam X phản ứng vừa đủ với 25 ml dung dich HCl 1M, thu được 3,1375 gam muối. X là
 Xem đáp án
Xem đáp án
Đáp án D
X chứa một nhóm NH2:
Bảo toàn khối lượng:
Vậy X là alanin.
Câu 20:
Este X mạch hở có công thức phân tử là C5H10O2. Thủy phân hoàn toàn X trong dung dịch NaOH dư, đun nóng, thu được 5,76 gam muối cacboxylat và 2,76 gam ancol. Tên gọi của X là
 Xem đáp án
Xem đáp án
Đáp án D
Dựa vào công thức phân tử → X là este no, đơn chức mạch hở, có công thức dạng RCOOR’ (a mol).
Ta có:
Bảo toàn khối lượng:
→ Công thức của X là C2H5COOC2H5 (etyl propionat).
Câu 21:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án D
A đúng vì crom có lớp màng oxit Cr2O3 bền bảo vệ nên có thể bảo vệ kim loại khỏi bị ăn mòn.
B đúng vì đây là tính chất vật lí của crom.
C đúng vì crom được dùng để sản xuất thép không gỉ (inox).
D sai vì muối Cr(III) có số oxi hóa là +3 là số oxi hóa trung gian nên vừa thể hiện tính oxi hóa, vừa thể hiện tính khử.
Câu 22:
Đốt cháy hoàn toàn m gam triglixerit X cần 1,61 mol O2, sinh ra 1,14 mol CO2 và 1,06 mol H2O. Cho 7,088 gam X tác dụng vừa đủ với dung dịch NaOH thì khối lượng muối tạo thành là
 Xem đáp án
Xem đáp án
Đáp án C
Đốt cháy hoàn toàn m gam triglixerit X:
Bảo toàn nguyên tố O:
Ta có: (do trong triglixerit có 6 nguyên tố O).
Bảo toàn khối lượng:
Cho 7,088 gam X tác dụng vừa đủ với dung dịch NaOH:
Ta có:
Bảo toàn khối lượng:
Câu 23:
Cho dãy các dung dịch sau: metylamin, anilin, lysin, alanin. Số dung dịch trong dãy làm quỳ tím chuyển sang màu xanh là
 Xem đáp án
Xem đáp án
Đáp án B
Dung dịch các chất làm quỳ tím hóa xanh là metylamin, lysin.
Chú ý: Anilin có tính bazo rất yếu, không làm quỳ tím đổi màu.
Alanin có số nhóm NH2 = số nhóm COOH nên không làm quỳ tím đổi màu.
Câu 24:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án C
A đúng vì là khái niệm của protein.
B đúng vì protein được tạo bởi nhiều gốc -amino axit nên trong phân tử luôn có nguyên tố nitơ.
C sai vì không phải tất cả mà chỉ là nhiều các protein tan trong nước và tạo thành dung dịch keo.
D đúng vì protein chứa nhiều liên kết peptit nên có phản ứng màu biure.
Câu 25:
Cho dãy các chất: FeCl2, CuSO4, BaCl2 và KNO3. Số chất trong dãy phản ứng được với dung dịch NaOH là
 Xem đáp án
Xem đáp án
Đáp án D
Các chất phản ứng được với dung dịch NaOH là FeCl2, CuSO4.
Các chất BaCl2 và KNO3 không phản ứng được với dung dịch NaOH là do không thỏa mãn điều kiện để phản ứng trao đổi xảy ra.
Câu 26:
Hỗn hợp X gồm glyxin, alanin và axit glutamic (trong đó nguyên tố oxi chiếm 41,2% về khối lượng). Cho m gam X tác dụng với dung dịch NaOH dư, thu được 20,532 gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Ta có:
Bào toàn khối lượng:
Câu 27:
Cho 2,603 gam Ba vào 100 ml dung dịch chứa Al2(SO4)3 0,05M đến khi phản ứng hoàn toàn, thu được m gam kết tủa. Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án B
;
Phương trình hóa học:
Ba + 2H2O → Ba(OH)2 + H2
0,019 → 0,019 0,019 mol
Ta có: ; ; ;
Xét tỉ lệ: Kết tủa bị hòa tan một phần.
Lại có:
Kết tủa gồm Al(OH)3 (0,002 mol) và BaSO4 (0,015 mol) nên
→ Loại A và D.
Xét dung dịch sau phản ứng:
Ta thấy: Dung dịch sau phản ứng giảm 1,086 gam so với dung dịch Al2(SO4)3 ban đầu.
Câu 28:
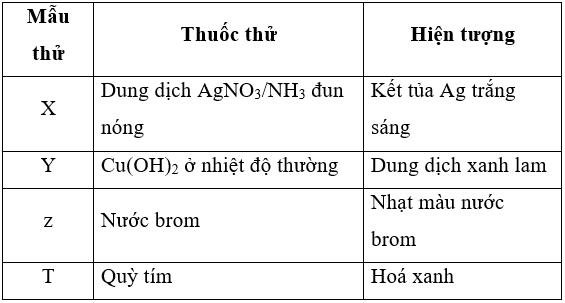
Các chất X, Y, Z, T lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án B
Dựa vào đáp án ta phân tích:
Chat X khi cho tác dụng với dung dịch AgNO3 trong NH3 đun nóng thu được kết tủa Ag → X là metyl fomat hoặc axit metanoic → Loại A.
Chất Z làm nhạt màu nước brom → Z là glucozơ → Loại C và D.
Vậy X, Y, Z, T lần lượt là: Metyl fomat, axit metanoic, glucozơ, metylamin.
Câu 29:
Đốt cháy hoàn toàn 5,4 gam hỗn hợp X gồm axit acrylic, axit oleic, vinyl axetat, metyl acrylat cần vừa đủ V lít O2 (ở đktc). Hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong dư, sau khi phản ứng hoàn toàn thu được 30 gam kết tủa. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án D
Axit acrylic, axit oleic, vinyl axetat, metyl acrylat đều có công thức phân tử dạng .
Gọi công thức chung của hỗn hợp X là .
Hấp thụ sản phẩm cháy vào nước vôi trong dư:
Phương trình hóa học:
0,3 mol
Ta có phương trình:
Theo phương trình:
Câu 30:
Cho hỗn hợp Na2C03 và KHC03 (tỉ lệ số mol tương ứng là 2 :1) vào bình chứa dung dịch Ba(HCG3)2 thu được m gam kết tủa X và dung dịch Y. Thêm tiếp dung dịch HCl IM vào bình đến khi không còn khí thoát ra thì hết 320 ml. Biết Y phản ứng vừa đủ với 160 ml dung dịch NaOH IM. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Gọi số mol của Na2CO3, KHCO3, Ba(HCO3)2 lần lượt là 2a, a, b mol.
Thêm tiếp dung dịch HCl 1M vào bình. Coi bình vẫn gồm các muối ban đầu phản ứng với HCl vì cả kết tủa X và dung dịch Y đều tác dụng với HCl.
Ta có:
Y phản ứng vừa đủ với 160 ml dung dịch NaOH 1M:
Phương trình hóa học:
0,16 ← 0,16 mol
Ta có: (**)
Từ (*) và (**) suy ra: ;
Phương trình hóa học:
Ba2+ + → BaCO3
0,06 0,08 → 0,06 mol
Câu 31:
Thực hiện các thí nghiệm sau:
(a) Nung nóng KNO3.
(b) Cho Fe(OH)2 vào dung dịch H2SO4 đặc, nóng, dư.
(c) Sục khí Cl2 vào dung dịch FeCl2.
(d) Cho dung dịch KHSO4 vào dung dịch FeCl2.
(e) Cho Si vào dung dịch NaOH.
Sau khi các phản ứng xảy ra, số thí nghiệm xảy ra phản ứng oxi hóa - khử là
 Xem đáp án
Xem đáp án
Đáp án A
Các thí nghiệm xảy ra phản ứng oxi hóa - khử là: (a), (b), (c), (e).
Câu 32:
 Xem đáp án
Xem đáp án
Đáp án C
Bảo toàn khối lượng:
Ta có:
Lại có:
Bảo toàn liên kết :
Câu 33:
Hỗn hợp X gồm axit panmitic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam X, thu được 1,56 mol CO2 và 1,52 mol H2O. Mặt khác, m gam X tác dụng vừa đủ với 0,09 mol NaOH trong dung dịch, thu được glixerol và dung dịch chỉ chứa a gam hỗn hợp muối natri panmitat, natri stearat. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án B
Khi cho X tác dụng với NaOH thu được dung dịch chỉ chứa muối natri panmitat, natri stearat nên triglixerit Y được tạo nên từ axit panmitic, axit stearic.
→ Y là trieste no, mạch hở.
Mà khi đốt cháy axit pânmitic, axit stearic (axit no, đơn chức, mạch hở) thu được
→ Khi đốt cháy hỗn hợp X gồm axit panmitic, axit stearic và triglixerit Y ta có:
Ta có quá trình:
Ta có:
Xét phản ứng đốt cháy m gam X:
Bảo toàn nguyên tố C, H:
Ta có:
Xét phản ứng của X với dung dịch NaOH
Bảo toàn khối lượng:
Câu 34:
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào ống nghiệm: 1 ml dung dịch lòng trắng trứng và 1 ml dung dịch NaOH 30%.
Bước 2: Cho tiếp vào ống nghiệm 1 giọt dung dịch CuSO4 2%. Lắc nhẹ ống nghiệm, sau đó để yên khoảng 2-3 phút.
Số phát biểu đúng trong các phát biểu dưới đây là
(a) Sau bước 1, hỗn hợp thu được có màu hồng.
(b) Sau bước 2, hỗn hợp xuất hiện chất màu tím.
(c) Thí nghiệm trên chứng minh anbumin có phản ứng màu biure.
(d) Thí nghiệm trên chứng minh anbumin có phản ứng thủy phân trong môi trường kiềm.
 Xem đáp án
Xem đáp án
Đáp án B
(a) sai vì cho vào ống nghiệm dung dịch lòng trắng trứng và dung dịch NaOH, thu được hỗn hợp không màu.
(b) đúng, (c) đúng vì khi cho tiếp vào ống nghiệm dung dịch CuSO4 và lắc nhẹ, xảy ra phản ứng màu biure với Cu(OH)2 (sinh ra từ phản ứng của CuSO4 với NaOH) nên hỗn hợp chất xuất hiện chất màu tím.
(d) sai.
Câu 35:
Hỗn hợp E chứa ba este đều mạch hở, trong phân tử chỉ chứa một loại nhóm chức gồm este X , este Y và este Z . Đun nóng 0,4 mol E với dung dịch NaOH vừa đủ, thu được 25,7 gam hỗn hợp gồm ba ancol cùng dãy đồng đẳng và 49,1 gam hỗn hợp T gồm ba muối. Đốt cháy toàn bộ T cần dùng 0,275 mol O2, thu được Na2CO3 và 0,49 mol hỗn hợp gồm CO2 và H2O. Phần trăm khối lượng của Y trong hỗn hợp E là
 Xem đáp án
Xem đáp án
Đáp án A
Xem muối gồm: X mol HCOONa; y mol C2H3COONa; z mol (COONa)2 và a mol CH2. Ta có hệ bốn ẩn:
Tổng số mol các muối: (1)
Tổng số mol H2O và CO2: (2)
Tổng khối lượng muối T: (3)
Số mol O2 cần để đốt là:
Giải hệ ta được: ; ; ;
Quy đổi ancol gồm 0,72 mol CH3OH và 0,19 mol CH2.
Ta thấy:
→ Có 0,05 mol HCOOC3H7 và 0,03 mol C2H3COOC4H9 và 0,32 mol (COOCH3)2.
Câu 36:
 Xem đáp án
Xem đáp án
Đáp án D
Trong Z chắc chắn có CO2 . Lại có:
→ Sản phẩm khử của N+5 là N2O (M = 44).
Ta có:
Ta có quá trình:
Bảo toàn khối lượng:
Bảo toàn nguyên tố H:
→ Có tao muối amoni:
Cho dung dịch NaOH dư vào dung dịch Y thu được kết tủa Mg(OH)2:
Dung dịch Y chứa Mg2+ (0,34 mol); Al3+ (a mol); (0,04 mol); Na+ (1,14 mol); (1,14 mol) và (b mol) .
(*)
Bảo toàn điện tích cho dung dịch Y:
(**)
Từ (*) và (**) suy ra: a = 0,18; b = 0,12
Bảo toàn nguyên tố N:
Ta có:
Câu 37:
 Xem đáp án
Xem đáp án
Đáp án C
Trong t giây:
Bảo toàn khối lượng:
Trong t giây tiếp theo:
Trong 2t giây:
Lại có:
Trong t giây:
Dung dịch Y chứa (0,72 mol); Na+ (0,16 mol); Cu2+ và H+.
Bảo toàn điện tích trong dung dịch Y:
Bảo toàn electron:
Ta có:
Câu 38:
Cho 4,6 gam hỗn hợp X gồm Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm b kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 đặc, nóng, dư, thu được 3,192 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 4,2 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm so mol của Fe trong X là
 Xem đáp án
Xem đáp án
Đáp án A
Theo thứ tự xuất hiện kim loại thì chất rắn Y gồm ba kim loại là Ag, Cu, Fe.
Ta có quá trình:
Gọi số mol Mg, Fe phản ứng, Fe dư lần lượt là a, b, c mol.
(*)
Bảo toàn electron cho quá trình X vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2:
Bảo toàn electron cho quá trình Y vào dung dịch H2SO4 đặc, nóng:
(**)
Bảo toàn nguyên tố Mg, Fe
Từ (*), (**), (***) suy ra: ; ;
Phần trăm số mol của Fe trong X:
Câu 39:
X là este no, hai chức, mạch hở; Y là este ba chức, mạch hở (được tạo bởi glixerol và một axit cacboxylic đơn chức, có chứa hai liên kết TC). Đốt cháy hoàn toàn 17,02 gam hỗn hợp E chứa X, Y thu được 18,144 lít CO2 (đktc). Mặt khác, đun nóng 0,12 mol E cần dùng 570 ml dung dịch NaOH 0,5M thu được dung dịch G. Cô cạn dung dịch G thu được hỗn hợp T chứa ba muối có khối lượng m gam và hỗn hợp hai ancol có cùng số nguyên tử cacbon. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Đun nóng 0,12 mol E cần dùng 570 ml dung dịch NaOH 0,5M:
Ta có:
X là este hai chức, Y là este ba chức:
Ta có hệ phương trình:
Gọi công thức phân tử của X và Y lần lượt là (5a mol) và (3a mol).
Đốt cháy hoàn toàn 17,02 gam hỗn hợp E chứa X, Y:
Bảo toàn nguyên tố C:
Ta có:
Đun nóng 0,12 mol E cần dùng 570 ml dung dịch NaOH 0,5M:
Sau phản ứng thu được hai ancol có cùng số nguyên tử C, mà trong đó có C3H5(OH)3, vậy ancol còn lại là C3H6(OH)2.
Bảo toàn khối lượng:
Câu 40:
Hòa tan hết m gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 vào dung dịch HCl dư, thu được a mol H2 và dung dịch chứa 31,19 gam hỗn hợp muối. Mặt khác, hòa tan hoàn toàn m gam X trong dung dịch chứa 0,55 mol H2SO4 (đặc) đun nóng, thu được dung dịch Y và 0,14 mol SO2 (sản phẩm khử duy nhất của S+6). Cho 400 ml dung dịch NaOH 1M vào Y, sau khi phản ứng kết thúc được 10,7 gam một chất kết tủa. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án D
Gọi số mol của FeCl2, FeCl3 trong muối lần lượt là x, y mol (*)
Quy đổi hỗn hợp X thành Fe và O.
Bảo toàn nguyên tố Fe:
Gọi số mol của O trong hỗn hợp X là z mol.
Xét phản ứng của X với H2SO4 đặc, nóng.
Trường hợp 1: H2SO4 đặc, nóng dư.
→ Kết tủa là Fe(OH)3,
Quá trình cho nhận electron:
Bảo toàn electron:
(**)
Ta có: 4H+ + + 2e → SO2 + 2H2O
0,56 ← 0,14 mol
Theo phương trình số mol H+ phản ứng tạo ra SO2 là 0,56 mol.
Dung dịch Y chứa Fe3+, H+ dư, .
Khi cho NaOH vào dung dịch Y:
→ (***)
Từ (*), (**), (***) suy ra: ;
Bảo toàn nguyên tố Cl:
Bảo toàn nguyên tố H và O:
Trường hợp 2: H2SO4 không dư.
Ta có: Y phản ứng với NaOH thu được kết tủa duy nhất → Trong Y chứa muối duy nhất Fe2+ hoặc Fe3+.
Trong Y có:
Giả sử Y chứa Fe3+:
Mặt khác, bảo toàn điện tích trong Y ta thấy: Loại.
Giả sử Y chứa Fe2+:
Mặt khác, bảo toàn điện tích trong Y, ta thấy: Loại.
