Đề thi thử THPT Quốc gia môn Hóa học năm 2022 có đáp án (30 đề)
Đề thi thử THPT Quốc gia môn Hóa học năm 2020 có đáp án (Đề số 20)
-
14726 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Phương trình phản ứng nào sau đây không thể hiện tính khử của NH3?
 Xem đáp án
Xem đáp án
Đáp án B
Phản ứng: NH3 + HCl → NH4Cl.
Do số oxi hóa của nguyên tố nitơ không tăng sau phản ứng nên phản ứng không thể hiện tính khử của NH3
Câu 2:
Nhiệt phân hoàn toàn KNO3 thu được sản phẩm gồm
 Xem đáp án
Xem đáp án
Đáp án B
Nhiệt phân hoàn toàn KNO3
Câu 3:
Trong các chất sau, chất nào khi thuỷ phân trong môi trường axit tạo thành sản phẩm có khả năng tham gia phản ứng tráng gương:
 Xem đáp án
Xem đáp án
Đáp án A
Este thủy phân trong môi trường axit tạo sản phẩm có khả năng phản ứng tráng gương là HCOOC2H5:
HCOOH là chất tham gia phản ứng tráng gương.
Câu 4:
Chất nào sau đây vừa tác dụng được với dung dịch axit, vừa tác dụng được với dung dịch bazơ?
 Xem đáp án
Xem đáp án
Đáp án B
Chất vừa tác dụng được với dung dịch axit, vừa tác dụng được với dung dịch bazơ là NH2-CH2-COOH.
Do nhóm -NH2 phản ứng được với dung dịch axit, -COOH phản ứng được với dung dịch bazơ.
Câu 5:
Phát biểu nào sau đây không đúng?
 Xem đáp án
Xem đáp án
Đáp án C
Phát biểu không đúng: “Trong phân tử đipeptit mạch hở có hai liên kết peptit”.
Do trong phân tử đipeptit mạch hở có 1 liên kết peptit.
Câu 6:
Dãy các chất nào sau đây đều có phản ứng thuỷ phân trong môi trường axit?
 Xem đáp án
Xem đáp án
Đáp án C
Do glucozơ và fructozơ không có phản ứng thủy phân trong môi trường axit.
→ Dãy các chất đều có phản ứng thuỷ phân trong môi trường axit: Tinh bột, xenlulozơ, saccarozơ.
Câu 7:
Trong các loại tơ: bông, tơ capron, tơ xenlulozơ axetat, tơ tằm, tơ nitron, nilon - 6,6. Số tơ tổng hợp là:
 Xem đáp án
Xem đáp án
Đáp án A
Tơ tổng hợp: capron, nitron, nilon-6,6.
Câu 8:
Hiện tượng xảy ra khi nhỏ vài giọt dung dịch H2SO4 vào dung dịch Na2CrO4 là:
 Xem đáp án
Xem đáp án
Đáp án D
màu vàng màu da cam
Câu 9:
Cho dãy các chất: Cr(OH)3, Al2(SO4)3, Mg(OH)2, Zn(OH)2, MgO, CrO3. Số chất trong dãy có tính chất lưỡng tính là
 Xem đáp án
Xem đáp án
Đáp án B
Những chất có tính chất lưỡng tính là: Cr(OH)3, Zn(OH)2
Câu 10:
Trong các phản ứng hóa học cacbon
 Xem đáp án
Xem đáp án
Đáp án C
Trong các phản ứng hóa học cacbon thể hiện tính oxi hóa và tính khử vì đơn chất cacbon vừa có thể tăng hoặc giảm số oxi hóa.
Câu 11:
Cacbon phản ứng với dãy chất nào sau đây:
 Xem đáp án
Xem đáp án
Đáp án B
Cacbon phản ứng được với các chất: H2, HNO3, và ZnO
Câu 12:
Khi cho 0,1 mol but-1-in tác dụng với dung dịch AgNO3/NH3 (dư) thu được m gam kết tủa, giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
→ m = 16,1 gam.
Câu 13:
Cho các tính chất sau:
(1) Tác dụng với nước ở nhiệt độ thường. (2) Tác dụng với dung dịch NaOH.
(3) Tác dụng với dung dịch HCl đặc nguội.
(4) Tác dụng với dung dịch HNO3 đặc nóng.
(5) Tác dụng với Cl2 ở nhiệt độ thường.
(6) Tác dụng với O2 nung nóng.
Trong các tính chất này, Al và Cr có chung:
 Xem đáp án
Xem đáp án
Đáp án D
Al và Cr có chung các tính chất: (3), (4), (6).
Câu 14:
Cho sơ đồ phản ứng:
polime Y
polime Z
Polime Y và polime Z lần lượt là
 Xem đáp án
Xem đáp án
Đáp án C
X là : CH2 = CH - CN
Polime Y là tơ olon :
Polime Z là cao su buna -N.
Câu 15:
Có các chất sau: phenol, axit axetic, glixeryl triaxetat, phenylamoni clorua và ancol etylic. Số chất tác dụng với dung dịch NaOH là
 Xem đáp án
Xem đáp án
Đáp án D
Chất tác dụng với dung dịch NaOH là: phenol, axit axetic, glixeryl triaxetat, phenylamoni clorua.
Câu 16:
Tiến hành các thí nghiệm sau:
(a) Sục khí Cl2 vào dung dịch NaOH ở nhiệt độ thường.
(b) Sục khí CO2 đến dư vào dung dịch KOH.
(c) Cho dung dịch chứa 1 mol AlCl3 vào dung dịch chứa 2 mol Ba(OH)2.
(d) Cho Cu vào dung dịch FeCl3 dư
(e) Cho KHS vào dung dịch NaOH vừa đủ.
Số thí nghiệm thu được hai muối là
 Xem đáp án
Xem đáp án
Đáp án A
Các thí nghiệm thu được hai muối là:
(a) 2 muối là: NaCl, NaClO.
(c) 2 muối là: BaCl2, Ba(AlO2)2.
(e) 2 muối là: K2S, Na2S.
Câu 17:
Tiến hành các thí nghiệm sau:
(1) Cho dung dịch NaOH vào dung dịch Ca(HCO3)2.
(2) Cho dung dịch HCl tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(3) Sục khí H2S vào dung dịch FeCl2.
(4) Sục khí NH3 tới dư vào dung dịch AlCl3.
(5) Sục khí CO2 tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
 Xem đáp án
Xem đáp án
Đáp án B
Các thí nghiệm thu được kết tủa là (1), (4), (5)
2NaOH + Ca(HCO3)2 → Na2CO3 + CaCO3 + H2O.
AlCl3 + 3NH3 + 3H2O → Al(OH)3 + 3NH4Cl.
CO2 + NaAlO2 + 2H2O → NaHCO3 + Al(OH)3.
Câu 18:
Kết quả thí nghiệm của các dung dịch X, Y, Z và T với thuốc thử được ghi lại ở bảng sau:
| X | Y | Z | T | |
| Dung dịch HCl | có phản ứng | không phản ứng | có phản ứng | có phản ứng |
| Dung dịch NaOH | có phản ứng | không phản ứng | không phản ứng | có phản ứng |
|
Dung dịch AgNO3/NH3 |
không phản ứng | có phản ứng | không phản ứng | không phản ứng |
Các chất X, Y, Z và T lần lượt là:
 Xem đáp án
Xem đáp án
Đáp án A
X là mononatri glutamat:
NaOOC-CH2- CH2 - CH(NH2) - COOH.
Y là glucozơ: CH2OH[CHOH]4CHO .
Z là etylamin: CH3 – CH2 – NH2
T là metyl acrylat: CH2 = CH - COO - CH3.
Câu 19:
Trong công nghiệp polietilen (PE) được điều chế từ metan theo sơ đồ:
Để tổng hợp 5,376 kg PE theo sơ đồ trên cần V m3 khí thiên nhiên (đktc, chứa 75% metan theo thể tích). Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Bảo toàn nguyên tố cacbon ta có:
Câu 20:
Lượng glucozơ cần dùng để tạo ra 1,82 gam sobitol với hiệu suất 80% là
 Xem đáp án
Xem đáp án
Đáp án A
Sobitol có công thức là: CH2OH- [CHOH]4-CH2OH. Công thức phân tử là C6H14O6.
Số mol glucozơ thực tế là:
Câu 21:
Trộn 200 ml dung dịch gồm HCl 0,1M và H2SO4 0,05M với 300 ml dung dịch Ba(OH)2 nồng độ x M thu được m gam kết tủa và 500 ml dung dịch có pH =13. Giá trị của x và m lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
Ta có:
Số mol OH- dư = 0,1.(0,2 + 0,3) = 0,05 mol.
Do đó 0,6x = 0,04 + 0,05 → x = 0,15.
Khối lượng kết tủa
Câu 22:
Tiến hành crackinh 10 lít khí butan, sau phản ứng thu được 18 lít hỗn hợp khí X gồm etan, metan, eten, propilen, butan (các khí đo cùng điều kiện). Hiệu suất của quá trình crackinh là
 Xem đáp án
Xem đáp án
Đáp án C
Phản ứng crackinh butan :
Câu 23:
Trung hoà 8,2 gam hỗn hợp gồm axit fomic và một axit đơn chức X cần 100 ml dung dịch NaOH 1,5M. Nếu cho 8,2 gam hỗn hợp trên tác dụng với một lượng dư dung dịch AgNO3 trong NH3, đun nóng thì thu được 21,6 gam Ag. Tên gọi của X là:
 Xem đáp án
Xem đáp án
Câu 23: Đáp án A
.
Tổng số mol axit = số mol NaOH phản ứng
= 0,1. 1,5 = 0,15 (mol).
→ nX = 0,15 - 0,1 = 0,05 (mol).
Vậy X là axit acrylic
Câu 24:
Hỗn hợp Z gồm hai este mạch hở X, Y tạo bởi cùng một ancol và hai axit cacboxylic kế tiếp nhau trong dãy đồng đẳng (MX < MY). Đốt cháy hoàn toàn m gam Z cần dùng 6,16 lít khí O2 (ở đktc), thu được 5,6 lít khí CO2 (ở đktc) và 4,5 gam H2O. Công thức cấu tạo của este X và giá trị m tương ứng là
 Xem đáp án
Xem đáp án
Đáp án C
.
Vậy hỗn hợp este X và Y là hai este no đơn chức mạch hở có công thức là .
Phương trình phản ứng đốt cháy:
Áp dụng định luật bảo toàn O:
Câu 25:
Cho m gam hỗn hợp X gồm axit glutamic và alanin tác dụng với dung dịch HCl dư. Sau phản ứng làm bay hơi cẩn thận dung dịch thu được (m + 11,68) gam muối khan. Nếu cho m gam hỗn hợp X tác dụng với dung dịch KOH vừa đủ, sau phản ứng làm bay hơi cẩn thận dung dịch thu được (m + 19) gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Khối lượng hỗn hợp X là:
m = 0,18.147 + 0,14.89 = 38,92 (gam)
Câu 26:
Khi thủy phân hoàn toàn 65,1 gam một peptit X (mạch hở) thu được 53,4 gam alanin và 22,5 gam glyxin. Đốt cháy hoàn toàn 19,53 gam X rồi dẫn sản phẩm vào Ca(OH)2 dư thu m gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Ta có:
Với 65,1 gam X
Với 19,53 gam X
Câu 27:
X là một α-aminoaxit no, chứa 1 nhóm -COOH và 1 nhóm -NH2. Từ 3m gam X điều chế được m1 gam đipeptit. Từ m gam X điều chế được m2 gam tripeptit. Đốt cháy m1 gam đipeptit thu được 1,35 mol nước. Đốt cháy m2 gam tripeptit thu được 0,425 mol H2O. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án B
Giả sử m gam X (CnH2n+1NO2) có a mol X. Ta có:
Với m1 gam đipeptit
Với m2 gam tripeptit
Câu 28:
Tỉ lệ số người chết về bệnh phổi do hút thuốc lá gấp hàng chục lần số người không hút thuốc lá. Chất gây nghiện và gây ung thư có trong thuốc lá là
 Xem đáp án
Xem đáp án
Đáp án A
Chất gây nghiện, gây ung thư có trong thuốc lá là nicotin.
Câu 29:
Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác bằng cách đẩy nước như hình vẽ sau.
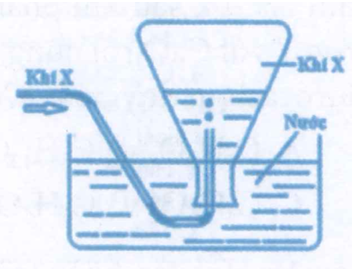
Phản ứng nào sau đây không áp dụng được cách thu khí này
 Xem đáp án
Xem đáp án
Đáp án A
Khí HCl không điều chế được theo phương pháp trên do tan trong nước.
Câu 30:
Đốt cháy 4,16 gam hỗn hợp Mg và Fe trong khí O2, thu được 5,92 gam hỗn hợp X chỉ gồm các oxit. Hòa tan hoàn toàn X trong dung dịch HCl vừa đủ, thu được dung dịch Y. Cho dung dịch NaOH dư vào Y, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được 6 gam chất rắn. Mặt khác cho Y tác dụng với dung dịch AgNO3 dư, thu được m gam kết tủa. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án A
Ta có
Nung Z cho số gam oxit lớn hơn
Câu 31:
Nung 1,92 gam hỗn hợp X gồm Fe và S trong bình kín không có không khí, sau một thời gian được chất rắn Y. Hòa tan hết Y trong dung dịch HNO3 đặc, nóng dư thu được dung dịch Z và V lít khí thoát ra (đktc). Cho Z tác dụng với dung dịch BaCl2 dư được 5,825 gam kết tủa. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B
Quá trình nhường electron:
→ ne = 3nFe + 6nS
= 0,02.3 + 0,025.6 = 0,21 (mol)
Quá trình nhận electron:
Thể tích của khí NO2 thu được là:
V = 0,21.22,4 = 4,704 lít.
Câu 32:
Hấp thụ hoàn toàn V lit CO2(ở đktc) vào bình đựng 200ml dung dịch NaOH 1M và Na2CO3 0,5M. Cô cạn dung dịch sau phản ứng thu được 19,9 gam chất rắn khan. Giá trị V là
 Xem đáp án
Xem đáp án
Đáp án A
Ta có:
Câu 33:
Khử hoàn toàn 4,06 gam một oxit kim loại bằng CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 dư, thấy tạo thành 7 gam kết tủa. Nếu lấy lượng kim loại sinh ra hoà tan hết vào dung dịch HCl dư thì thu được 1,176 lít khí H2 (đktc). Cho 4,06 gam oxit kim loại trên tác dụng hoàn toàn với 500 ml dung dịch H2SO4 đặc, nóng (dư) được dung dịch X và có khí SO2. Nồng độ mol/lít của muối trong dung dịch X là (coi thể tích dung dịch không đổi trong quá trình phản ứng):
 Xem đáp án
Xem đáp án
Đáp án C
Câu 34:
Hỗn hợp X gồm các aminoaxit no, mạch hở (trong phân tử chỉ có nhóm chức -COOH và -NH2) có tỉ lệ mol nO : nN = 2:1. Để tác dụng vừa đủ với 35,85 gam hỗn hợp X cần 300 ml dung dịch HCl 1,5M. Đốt cháy hoàn toàn 11,95 gam hỗn hợp X cần vừa đủ 9,24 lít khí O2 (đktc). Dẫn toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được m gam kết tủa, Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án D
Với 11,95 gam
Câu 35:
Cho hỗn hợp X gồm bốn este mạch hở, trong đó có một este đơn chức và ba este hai chức là đồng phân của nhau. Đốt cháy 11,88 gam X cần 14,784 lít O2 (đktc), thu được 25,08 gam CO2. Đun nóng 11,88 gam X với 300 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng thu được chất rắn Y và phần hơi chỉ chứa một ancol đơn chức Z. Cho Z vào bình Na dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng bình Na tăng 5,85 gam. Trộn Y với CaO rồi nung trong điều kiện không có không khí, thu được 2,016 lít (đktc) một hiđrocacbon duy nhất. Công thức phân tử của các este là
 Xem đáp án
Xem đáp án
Đáp án A
Áp dụng bảo toàn khối lượng, ta được:
Áp dụng bảo toàn nguyên tố O, ta được:
nO/X = 0,44 + 0,57.2 – 0,66.2 = 0,26 mol.
→ Số mol nhóm
Gọi công thức ancol đơn chức Z là ROH, công thức trung bình của 4 este là
(Do NaOH dư vì nNaOH phản ứng = nCOONa = nCOO = 0,13 mol < 0,17 mol)
Gọi công thức ba este hai chức là CnHm(COOC2H5)2 có số mol là x, công thức este đơn chức là CnHm+1COOC2H5 có số mol là y.
Bảo toàn “C”:
0,04(n + 6) + 0,05(n + 3) = 0,57
→ n = 2.
Bảo toàn “H”:
0,02(m + 10) + 0,025(m + 6) = 0,44
→ m = 2.
→ Công thức phân tử, của este đơn chức: C5H8O2.
→ Công thức phân tử, của ba este hai chức: C8H12O4.
Câu 36:
Hòa tan hoàn toàn a gam Al trong dung dịch Ba(OH)2 thu được dung dịch X. Nhỏ từ từ dung dịch H2SO4 0,5M vào dung dịch X và lắc nhẹ đến các phản ứng xảy ra hoàn toàn.
Đồ thị biểu diễn sự phụ thuộc tổng khối lượng kết tủa (m gam) theo thể tích H2SO4 (V ml) như sau:
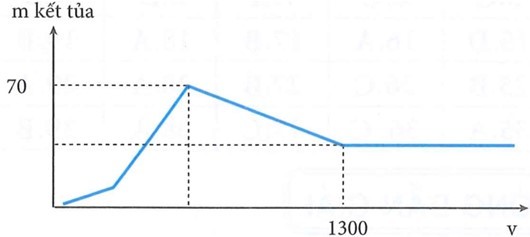
Giá trị của a là:
 Xem đáp án
Xem đáp án
Đáp án C
Dung dịch X chứa Ba2+ (x mol), (y mol), OH- (z mol).
Bảo toàn điện tích: 2x = y + z
m↓max = 233x + 78y = 70.
Khi hòa tan hết Al(OH)3 thì nH+ = 1,3 mol
→ = 1,3 = z + 4y
→ x = 0,2; y = 0,3; z = 0,1
→ mAl = 27.y = 8,1 (gam)
Câu 37:
.Hỗn hợp X gồm một số hợp chất hữu cơ bền, mỗi chất chỉ chứa 2 nhóm chức trong 3 nhóm chức ancol, anđehit, axit, ngoài ra không có nhóm chức nào khác và khi đốt cháy V lít mỗi chất đều thu được 2V lít CO2. Chia 31,44 gam hỗn hợp X thành ba phần bằng nhau:
- Cho phần một tác dụng với một lượng dung dịch NaHCO3 vừa đủ thu được 2,24 lít CO2 (đktc).
- Cho phần hai tác dụng với một lượng Na vừa đủ thu được 2,128 lít H2 (đktc).
- Cho phần ba tác dụng với một lượng dư dung dịch AgNO3/NH3 thu được m gam Ag.
Các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Trong X mỗi chất chỉ chứa 2 nhóm chức khác nhau (ancol, axit, andehit) → mỗi chất có ít nhất 2C.
Mà đốt V lít X sinh ra 2V lít CO2 → chứng tỏ mỗi chất trong X đều chứa 2C.
Luôn có nCOOH = = 0,1 mol.
Khi tham gia phản ứng với Na
.
Vì mỗi chất đều có 2C, và chứa 2 nhóm chức → chức ancol OH- phải đính với C no (hay nhóm CH2) → số mol nhóm CH2 là 0,09 mol.
Khối lượng mỗi phần là 31,44:3 = 10,48 gồm:
nAg =2nCHO = 0,22mol → mAg = 0,22.108 = 23,76 gam.
Câu 38:
Cho các chất hữu cơ mạch hở: X là axit no, hai chức, Y và Z là hai ancol không no, đơn chức (MY > MZ); T là este của X, Y, Z (chỉ chứa chức este). Đốt cháy hoàn toàn a gam hỗn hợp E gồm Y và T thu được 9,072 lít CO2 (đktc) và 5,13 gam H2O. Mặt khác, cho 0,09 mol E tác dụng vừa đủ với dung dịch NaOH, cô cạn dung dịch sau phản ứng thu được muối khan F và hỗn hợp ancol G. Đốt cháy hoàn toàn F thu được CO2; H2O và 0,06 mol Na2CO3. Đốt cháy hoàn toàn G thu được 10,08 lít CO2 (đktc). Phần trăm khối lượng của Y có trong E có giá trị gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Đáp án A
Câu 39:
Hỗn hợp X gồm FeO, Fe3O4 và kim loại M (có hóa trị không đổi), trong X số mol oxi bằng 0,6 lần số mol M. Hòa tan 15,52 gam X trong dung dịch HNO3 loãng dư thấy có 0,82 mol HNO3 phản ứng, sau phản ứng thu được 61 gam hỗn hợp muối và 0,448 lít NO (đktc). Phần trăm khối lượng của M trong X gần nhất với:
 Xem đáp án
Xem đáp án
Đáp án B
Bảo toàn điện tích:
Từ (1) và (2)
Câu 40:
Cho 9,6 gam Mg tác dụng với dung dịch chứa 1,2 mol HNO3, thu được dung dịch X và m gam hỗn hợp khí. Thêm 500 ml dung dịch NaOH 2M vào X, thu được dung dịch Y, kết tủa và 1,12 lít khí Z (đktc). Lọc bỏ kết tủa, cô cạn Y thu được chất rắn T. Nung T đến khối lượng không đổi, thu được 67,55 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
Do X + NaOH tạo khí Z nên X chứa NH4+
→ X chứa: H+ (có thể dư), NO3-, Mg2+
(0,4 mol), NH4+.
Kết tủa là Mg(OH)2 (0,4 mol), khí là NH3 (0,05 mol)
Xét NaOH dư thì 67,55 gam chất rắn chỉ có NaNO2 (a mol) và NaOH dư (b mol).
khối lượng chất rắn
Bảo toàn H:
Bảo toàn khối lượng:
