Đề thi thử THPT Quốc gia môn Hóa học năm 2022 có đáp án (30 đề)
Đề thi thử THPT Quốc gia môn Hóa học năm 2022 có đáp án (Đề số 8)
-
14711 lượt thi
-
40 câu hỏi
-
60 phút
Danh sách câu hỏi
Câu 1:
Muối nào sau đây không phải là muối axit?
 Xem đáp án
Xem đáp án
Đáp án D
Muối axit là muối mà gốc axit vẫn còn H có khả năng phân li ra ion Muối trung hòa là muối mà gốc axit không còn H có khả năng phân li ra ion .
Trong công thức cấu tạo của Na2HPO3 vẫn còn nguyên tử H, nhưng không có khả năng phân li ra ion , vì liên kết giữa H - P là liên kết cộng hóa trị không phân cực. Trong công thức cấu tạo của các muối còn lại vẫn còn nguyên tử H có khả năng phân li ra ion (do liên kết giữa H - O là liên kết cộng hóa trị có cực, cặp e dùng chung lệch hẳn về phía oxi là nguyên tử có độ âm điện lớn hơn).
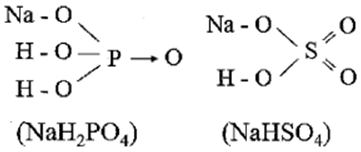
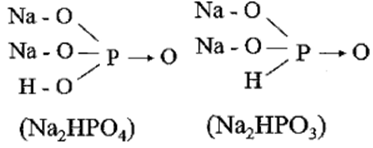
Câu 2:
Phản ứng thủy phân este trong môi trường kiềm, đun nóng gọi là phản ứng
 Xem đáp án
Xem đáp án
Đáp án A
Phản ứng thủy phân este trong môi trường kiềm, đun nóng gọi là phản ứng xà phòng hóa.
Câu 3:
Dung dịch nào sau đây làm quỳ tím chuyển thành màu xanh?
 Xem đáp án
Xem đáp án
Đáp án C
Công thức cấu tạo của lysin: H2N-[CH2]4-CH(NH2)-COOH, số nhóm chức -NH2 > -COOH → Lysin làm quỳ tím hóa xanh.
Câu 4:
Đun nóng tristearin trong dung dịch NaOH thu được glixerol và
 Xem đáp án
Xem đáp án
Đáp án B
Đun nóng tristearin trong dung dịch NaOH thu được glixerol và C17H35COONa.
Câu 5:
Peptit nào sau đây không có phản ứng màu biure?
 Xem đáp án
Xem đáp án
Đáp án A
Điều kiện để có phản ứng màu biure là peptit phải chứa 2 liên kết peptit -CO-NH- trở lên (từ tripeptit trở lên).
Câu 6:
Đun nóng este CH2=CHOOCCH3 với một lượng vừa đủ dung dịch NaOH, sản phẩm thu được là
 Xem đáp án
Xem đáp án
Đáp án C
CH2=CHOOCCH3 + NaOH → CH3COONa + CH3CHO
Câu 7:
Sự kết hợp các phân tử nhỏ (monome) thành các phân tử lớn (polime) có khối lượng bằng tổng khối lượng của các monome hợp thành được gọi là
 Xem đáp án
Xem đáp án
Đáp án B
Sự kết hợp các phân tử nhỏ (monome) thành các phân tử lớn (polime) có khối lượng bằng tổng khối lượng của các monome hợp thành được gọi là sự trùng hợp.
Câu 8:
Tính chất nào sau đây không phải tính chất vật lí chung của kim loại?
 Xem đáp án
Xem đáp án
Đáp án B
Kim loại có các tính chất vật lí chung là: Dẫn nhiệt, dẫn điện, ánh kim và tính dẻo.
Kim loại có các tính chất vật lí riêng là: Tính cứng, khối lượng riêng, nhiệt độ nóng chảy.
Câu 9:
Hợp chất nào sau đây có màu đỏ thẫm?
 Xem đáp án
Xem đáp án
Đáp án C
Cr2O3: màu lục thẫm; Cr(OH)3: màu lục xám; CrO3: màu đỏ thẫm; K2CrO4 : màu vàng
Câu 10:
Chọn một phương án đúng để điền từ hoặc cụm từ vào chỗ trống của các câu sau đây: Tương tự xenlulozơ, tinh bột không có phản ứng………………………(1)….., có phản ứng……………….(2)…….. trong dung dịch axit thành………………..(3)….. .
 Xem đáp án
Xem đáp án
Đáp án C
Tương tự xenlulozơ, tinh bột không có phản ứng tráng bạc, có phản ứng thủy phân trong dung dịch axit thành glucozơ.
Câu 11:
Sản phẩm chính sinh ra khi hidrat hóa ankin X (đồng đẳng kế tiếp với axetilen) trong điều kiện () là?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 12:
Khi cho isopren tham gia phản ứng cộng với H2 (xt, ), thu được tối đa bao nhiêu sản phẩm?
 Xem đáp án
Xem đáp án
Đáp án D
Isopren có thể tham gia phản ứng cộng với H2 theo tỉ lệ 1:1 và 1:2, thu được tối đa 4 dẫn xuất như sau:
Câu 13:
Cho các dung dịch: axit glutamic, valin, lysin, alanin, etylamin, anilin. Số dung dịch làm quỳ tím chuyển sang màu hồng, chuyển sang màu xanh và không chuyển màu lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
Cần nhớ công thức cấu tạo của các chất:
Axit glutamic: HOOC-CH(NH2)-CH2-CH2-COOH
Valin: (CH3)2CH-CH(NH2)-COOH
Lysin: H2N-[CH2]4-CH(NH2)-COOH
Alanin: NH2-CH(CH3)-COOH
Etylamin: C2H5NH2
Anilin: C6H5NH2
- Dung dịch làm quỳ tím chuyển màu hồng: axit glutamic
- Dung dịch làm quỳ tím chuyển màu xanh: lysin, etylamin
- Dung dịch không làm quỳ đổi màu: valin, alanin, anilin
Câu 14:
Đốt cháy hoàn toàn 7 gam sắt trong 3,36 lít khí Cl2 (đktc) thu được m gam FeCl3. Giá trị của m là?
 Xem đáp án
Xem đáp án
Đáp án A
Phương trình phản ứng:
Fe + Cl2 FeCl3
Ban đầu: 0,125 0,15
Phản ứng: 0,1 0,1 0,1
Sau phản ứng: 0,25 0 0,1
(gam).
Lưu ý: Mặc dù sau phản ứng trên Fe dư, nhưng không phản ứng với FeCl3 (phản ứng chỉ xảy ra trong dung dịch).
Câu 15:
Khối lượng phân tử của 1 loại tơ capron bằng 17063 đvC, của tơ enang bằng 21717 đvC. Số mắt xích trong công thức phân tử của mỗi loại tơ trên lần lượt là?
 Xem đáp án
Xem đáp án
Đáp án A
Mắt xích của tơ capron (nilon-6) và tơ enang (nilon-7) có cấu tạo lẩn lượt là:
(-HN-(CH2)5-CO-) và (-HN-(CH2)6-CO-).
Số mắt xích trong công thức phân tử của tơ carpon là:
Số mắt xích trong công thức phân tử của tơ enang là:
Câu 16:
Thể tích dung dịch HNO3 65% (khối lượng riêng là 1,5 gam/ml) cần dùng để tác dụng với xenlulozơ tạo thành 89,5 kg xenlulozơ trinitrat là (biết lượng HNO3 bị hao hụt là 25%)?
 Xem đáp án
Xem đáp án
Đáp án D
Vì lượng HNO3 hao hụt 25% nên hiệu suất phản ứng chỉ đạt 75%. Gọi x là số kg HNO3 đem phản ứng thì lượng HNO3 phản ứng là x.75% kg.
Phương trình phản ứng:
C6H7O2(OH)3 + 3HNO3 C6H7O2(ONO2)3 + 3H2O (1)
gam: 63.3 297
kg: x.75% 89,5
Theo (1) và giả thiết ta thấy khối lượng HNO3 nguyên chất đã tham gia phản ứng là:
Thể tích dung dịch HNO3 nguyên chất cần dùng là: lít.
Câu 17:
Nhiệt phân hoàn toàn một hỗn hợp 17,4g M2CO3 và CaCO3. Đến khi phản ứng kết thúc thu được 8,6g chất rắn X và V lít khí CO2 (đktc). Giá trị của V và kim loại M tương ứng là?
 Xem đáp án
Xem đáp án
Đáp án C
loại A và B.
Ta có hệ phương trình:
Câu 18:
Cho hỗn hợp X gồm Al, Zn, Cu, Mg tác dụng hết với dung dịch HNO3 đặc, nguội, dư thì thu được dung dịch Y và phần không tan Z. Thêm dung dịch NaOH dư vào dung dịch Y, lọc lấy kết tủa rồi đem nung đến khối lượng không đổi thì được chất rắn E. Nếu cho khí CO dư đi qua E nung nóng tới phản ứng hoàn toàn thì chất rắn thu được sau cùng có chứa
 Xem đáp án
Xem đáp án
Đáp án C
Câu 19:
Đốt cháy hoàn toàn 6,2 gam P trong khí O2 dư, toàn bộ sản phẩm sinh ra cho vào 500 ml dung dịch hỗn hợp NaOH 0,4M và KOH 0,6M, kết thúc phản ứng thu được dung dịch X. Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối có trong dung dịch X là?
 Xem đáp án
Xem đáp án
Đáp án C
Sơ đồ phản ứng:
P P2O5 H3PO4
0,2 → 0,1 → 0,2 (mol)
Câu 20:
X, Y, Z là ba hiđrocacbon mạch hở () có cùng số nguyên tử cacbon trong phân tử và đều phản ứng với dung dịch AgNO3 trong NH3 dư. Cho 15,6 gam hỗn hợp E gỗm X, Y, Z (có cùng số mol) tác dụng tối đa với a mol Br2 trong dung dịch. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án D
Từ dữ kiện:
Mặt khác, trong CTCT, X có 4 liên kết π, Y có 3 liến kết π, Z có 2 liên kết π
→ Tổng số liên kết .
Câu 21:
Cho hỗn hợp A gồm Fe, Ag, Cu, Al tác dụng với oxi dư khi đun nóng được chất rắn B. Cho B vào dung dịch HCL dư, khuấy kĩ, sau đó lấy dung dịch thu được cho tác dụng với dung dịch NaOH loãng, dư. Lọc lấy kết tủa tạo thành đem nung trong không khí đến khối lượng không đổi thu được chất rắn C. Biết các phản ứng xảy ra hoàn toàn. Thành phần của C gồm:
 Xem đáp án
Xem đáp án
Đáp án A
Câu 22:
Tách nước hoàn toàn từ 25,8 gam hỗn hợp A gồm hai ancol X và Y () sau phản ứng thu được hỗn hợp B gồm hai anken kế tiếp nhau trong dãy đồng đẳng. Đốt cháy hoàn toàn B cần 1,8 mol O2. Mặt khác, nếu tách nước không hoàn toàn 25,8 gam hỗn hợp trên ( , xúc tác H2SO4) sau phản ứng thu được 11,76 gam hỗn hợp ete. Biết hiệu suất ete hóa của Y là 50%. Hiệu suất ete hóa của X là?
 Xem đáp án
Xem đáp án
Đáp án C
Theo đầu bài ta có:
Câu 23:
Tripeptit X có công thức sau: H2N-CH2-CO-NH-CH(CH3)-CO-NH-CH(CH3)-COOH. Thủy phân hoàn toàn 0,15 mol X trong 250 ml dung dịch NaOH 2M. Khối lượng chất rắn thu được khi cô cạn dung dịch sau phản ứng là?
 Xem đáp án
Xem đáp án
Đáp án C
Theo đầu bài ta có: X là tripeptit nên một phân tử X phản ứng với 3 phân tử NaOH : 2 phân tử NaOH tham gia phản ứng thủy phân 2 liên kết peptit, 1 phân tử NaOH để trung hòa nhóm –COOH đồng thời giải phóng ra một phân tử nước.
Phương trình phản ứng tổng quát:
X + 3NaOH → muối + H2O (1)
mol: 0,15 → 0,45 → 0,15
Vậy theo phản ứng (1) ta thấy chất rắn thu được có cả NaOH dư. Áp dụng định luật bảo toàn khối lượng ta có:
Câu 24:
Hỗn hợp X gồm O2 và O3 có tỉ khối so với Heli là 11. Hỗn hợp khí Y gồm metylamin và etylamin có tỉ khối so với H2 là . Để đốt cháy hoàn toàn V1 lít Y cần vừa đủ V2 lít X (biết sản phẩm cháy gồm CO2, H2O và N2, các chất khí khi đo ở cùng điều kiện nhiệt độ, áp suất). Tỉ lệ V2 : V1 là:
 Xem đáp án
Xem đáp án
Đáp án C
Đặt CTPT trung bình của 2 amin là .
Theo giả thiết suy ra: .
Quy đổi hỗn hợp O3, O2 thành O, theo định luật bảo toàn khối lượng ta có .
Sơ đồ phản ứng:
(1)
mol: 1
Theo (1) ta có:
Vậy .
Câu 25:
Trong chất béo luôn có một lượng axit béo tự do. Khi thuỷ phân hoàn toàn 2,145 kg chất béo, cẩn dùng 0,3 kg NaOH, thu 0,092 kg glixerol, và m gam hỗn hợp muối Na. Khối lượng xà phòng chứa 60% muối natri về khối lượng thu được là?
 Xem đáp án
Xem đáp án
Đáp án D
Đặt công thức tổng quát của chất béo là .
Phương trình phản ứng hóa học:
+ 3NaOH → C3H5(OH)3 + (1)
+ NaOH → + H2O (2)
Xà phòng thu được bao gồm cả muối natri tạo ra ở (1) và (2).
Ta có: ;
trong khi số mol NaOH đã phản ứng là
và bằng số mol H2O tạo ra ở (2).
Áp dụng bảo toàn khối lượng ta có:
Khối lượng xà phòng chứa 60% muối natri về khối lượng thu được là:
Câu 26:
Cho 400 ml dung dịch E gồm AlCl3 a mol/lít và Al2(SO4)3 b mol/lít tác dụng với 612 ml dung dịch NaOH IM, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 (dư) thì thu được 33,552 gam kết tủa. Tỉ số a : b có giá trị là
 Xem đáp án
Xem đáp án
Đáp án C
Theo đầu bài ta có:
Mặt khác:
→ Kết tủa đạt cực đại sau đó bị hòa tan một phần
→
Câu 27:
Đốt cháy m gam hỗn hợp E gồm anđehit fomic, metyl fomat, benzen, etylen glicol thu được 6,72 lít CO2 (đktc) và 4,5 gam H2O. Mặt khác, cho 9,03 gam E tác dụng với Na dư thu được 1,344 lít H2 (đktc). Các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C
Hỗn hợp E gồm: HCHO, C2H4O2, C2H4(OH)2, C6H6.
Cách 1: Quy đổi E thành:
Cách 2: Phân tích hỗn hợp E ta thấy rằng:
Câu 28:
Để xà phòng hoá hoàn toàn 2,22 gam hỗn hợp hai este là đồng phân X và Y, cần dùng 30 ml dung dịch NaOH 1M. Khi đốt cháy hoàn toàn hỗn hợp hai este đó thì thu được khí CO2 và hơi nước với tỉ lệ thể tích . Tên gọi của hai este là?
 Xem đáp án
Xem đáp án
Đáp án B
Do 2 este no, đơn chức, mạch hở.
Công thức phân tử của este có dạng .
Trừ este của phenol, este đơn chức sẽ tác dụng với NaOH theo tỉ lệ mol 1:1.
Suy ra: (gam/mol).
Công thức phân tử C3H6O2 chỉ tồn tại 2 este đồng phân là HCOOC2H5 (etyl fomat) và CH3COOCH3 (metyl axetat).
Câu 29:
Thí nghiệm trên hình mô tả phản ứng nào sau đây? (Biết phản ứng đã xảy ra trong điều kiện thích hợp).
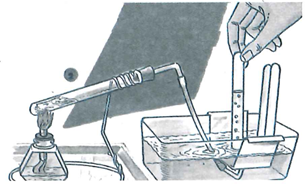
 Xem đáp án
Xem đáp án
Đáp án C
Sau phản ứng khí được thu bằng phương pháp đẩy nước → loại A và B vì H2S và NH3 tan trong nước nên không thu khí bằng phương pháp đẩy nước được. Loại D vì phản ứng xảy ra mãnh liệt ở điều kiện thường, không cần dùng đèn cồn đun nóng.
Câu 30:
Cho X, Y, Z, T là các chất khác nhau trong các chất: CH3NH2, NH3, C6H5OH (phenol), C2H5OH và các tính chất được ghi trong bảng sau:
| Chất | X | Y | Z | T |
| Nhiệt độ sôi () | 182 | 78 | -6,7 | -33,4 |
| Độ hòa tan trong nước (g/100 ml ở ) | 8,3 | 108,0 | 89,9 |
Kết luận nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án B
Chỉ có ancol etylic C2H5OH tan vô hạn trong nước → Y là C2H5OH.
Ở điểu kiện thường phenol là chất rắn, còn NH3 và CH3NH2 đều là các chất khí.
→ dựa vào nhiệt độ sôi X, Z, T còn lại → X là phenol; còn Z, T là một trong hai khí còn lại.
CH3NH2 có phân tử khối lớn hơn NH3 nên nhiệt độ sôi CH3NH2 lớn hơn NH3.
→ Z là CH3NH2 và còn lại T là NH3.
| Chất | X | Y | Z | T |
| Nhiệt độ sôi () | 182 | 78 | -6,7 | -33,4 |
| Độ hòa tan trong nước (g/100 ml ở ) | 8,3 | 108,0 | 89,9 | |
| Suy luận ra | C6H5OH | C2H5OH | CH3NH2 | NH3 |
Câu 31:
Cho các phát biểu sau:
a) Chất béo chứa các gốc axit no thường là chất lỏng ở nhiệt độ thường.
b) Chất béo bị thủy phân trong môi trường axit tạo ra etylen glicol và các axit béo.
c) Tơ nitron dùng để dệt vải may quần áo ấm hoặc bện thành sợi “len” đan áo rét.
d) Trong phân tử peptit mạch hở số liên kết peptit bao giờ cũng bằng số gốc α - aminoaxit.
e) Amilopectin và amilozơ là đồng phân, khác nhau ở cấu trúc có nhánh và không phân nhánh.
f) Để nhận biết metylamin, anilin, glyxin, metylíomat, có thể sử dụng quỳ tím và nước brom.
g) Este CH2=C(CH3)-COOCH3 có tên gọi là etyl acrylat.
Số phát biểu sai là:
 Xem đáp án
Xem đáp án
Đáp án D
(a) Sai, chất béo chứa các gốc axit no thường là chất rắn ở nhiệt độ thường.
(b) Sai, chất béo bị thủy phân trong môi trường axit tạo ra glixerol và các axit béo.
(c) Đúng.
(d) Sai, trong phân tử peptit mạch hở số liên kết peptit bao giờ cũng nhỏ hơn số gốc α - aminoaxit.
(e) Sai, amilopectin và amilozơ không phải là đồng phân của nhau.
(f) Đúng, metylamin (quỳ → xanh), anilin (không đổi màu quỳ, brom kết tủa trắng), glyxin (không đổi màu quỳ), metylfomat (không đổi màu quỳ, mất màu brom, sủi bọt khí CO2).
(g) Sai, este CH2=C(CH3)-COOCH3 có tên gọi là metyl metacrylat.
Câu 32:
Thực hiện các thí nghiệm sau:
(1) Cho hỗn hợp gồm 2a mol Na và a mol Al vào lượng nước dư.
(2) Cho a mol bột Cu vào dung dịch chứa a mol Fe2(SO4)3.
(3) Cho dung dịch chứa a mol KHSO4vào dung dịch chứa a mol KHCO3.
(4) Cho dung dịch chứa a mol BaCl2 vào dung dịch chứa a mol CuSO4.
(5) Cho dung dịch chứa a mol Fe(NO3)2 vào dung dịch chứa a mol AgNO3.
(6) Cho a mol Na2O vào dung dịch chứa a mol CuSO4.
(7) Cho hỗn hợp Fe2O3 và Cu (tỉ lệ mol tương ứng 2:1) vào dung dịch HCl dư.
Sau khi kết thúc thí nghiệm, số trường hợp thu được dung dịch chứa hai muối là
 Xem đáp án
Xem đáp án
Đáp án B
(1) Thu được NaOH (a) và NaAlO2 (a)
Na + H2O → NaOH + 1/2H2
NaOH + Al + H2O → NaAlO2 + 3/2H2
(2) Thu được CuSO4 (a) và FeSO4 (2a)
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
(3) Thu được K2SO4 (a)
KHSO4 + KHCO3 → K2SO4 + CO2 + H2O
(4) Thu được CuCl2 (a)
CuSO4 + BaCl2 → BaSO4 + CuCl2
(5) Thu được Fe(NO3)3 (a)
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
(6) Thu được Na2SO4 (a)
Na2O + H2O → 2NaOH
2NaOH + CuSO4 → Cu(OH)2 + Na2SO4
(7) Thu được FeCl3, FeCl2, CuCl2
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Cu + 2FeCl3 → CuCl2 + 2FeCl2
Câu 33:
Nhỏ từ từ đến dư dung dịch Ba(OH)2 vào dung dịch gồm Al2(SO4)3 và AlCl3. Sự phụ thuộc của khối lượng kết tủa vào số mol Ba(OH)2 được biểu diễn bằng đồ thị dưới đây. Nếu số mol Ba(OH)2 đã dùng là 0,065 mol, thì lượng kết tủa thu được sẽ là:
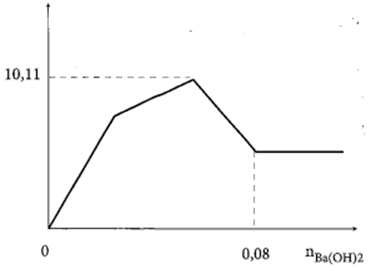
 Xem đáp án
Xem đáp án
Đáp án A
Gọi ta có bản chất thứ tự các phản ứng xảy ra như sau:
3Ba(OH)2 + Al2(SO4)3 → 2Al(OH)3 ↓ + 3BaSO4 ↓ (1)
3a a 2a 3a
3Ba(OH)2 + 2AlCl3 → 2Al(OH)3 ↓ + 3BaCl2 (2)
1,5b b b
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O (3)
(a + 0,5b) (2a + b)
Tại A: (4)
Tại B: (5)
Vậy:
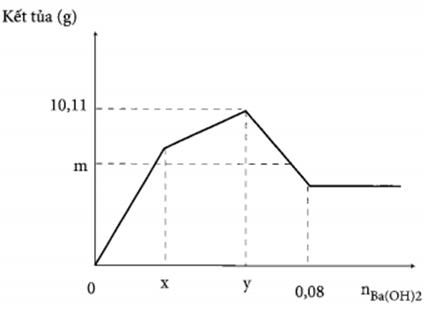
Khi kết tủa đạt cực đại tại A, nếu tiếp tục nhỏ thêm Ba(OH)2 vào, chỉ có Al(OH)3 bị hòa tan. Đoạn AB chính là đoạn hòa tan kết tủa. Tại điểm B, kết tủa Al(OH)3 bị hòa tan hết, đường đồ thị nằm ngang khi tăng lượng Ba(OH)2 là đường kết tủa BaSO4 không đổi.
Theo đầu bài dùng để hòa tan Al(OH)3 = 0,065 – 0,06 = 0,005 (mol)
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
0,005 → 0,01
Khối lượng kết tủa còn lại là: m = 10,11 – 0,01.78 = 9,33 (gam).
Câu 34:
Điện phân dung dịch chứa 0,2 mol KCl và a mol Cu(NO3)2 (điện cực trơ, màng ngăn xốp) sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 21,5 gam. Cho thanh sắt vào dung dịch X đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng thanh sắt giảm 2,6 gam và thấy thoát ra khí NO (sản phẩm khử duy nhất). Biết Cu(NO3)2 còn dư sau khi quá trình điện phân kết thúc. Giá trị của a là
 Xem đáp án
Xem đáp án
Đáp án C
Bản chất quá trình: về catot − bị khử tạo thành Cu, về anot + bị oxi hóa → Cl2
Vì cho Fe + X có khí thoát ra, Cu(NO3)2 còn dư sau quá trình điện phân, KCl hết → quá trình điện phân chia 2 giai đoạn, ở giai đoạn 2 chưa kết thúc.
→ Khối lượng dung dịch giảm = mCu + mCl2 ↑ + mO2 ↑
Cu(NO3)2 + 2KCl → Cu + Cl2 + 2KNO3
0,1 0,2 0,1 0,1 0,2
2Cu(NO3)2 + 2H2O → 2Cu + O2 + 4HNO3
x x 0,5x 2x
Khối lượng dung dịch giảm:
Dung dịch sau phản ứng gồm:
Khối lượng thanh sắt giảm:
Câu 35:
Một học sinh nghiên cứu tính chất của ba dung dịch lần lượt chứa các chất A, B, C như sau:
- A tác dụng với B thu được kết tủa X, cho X vào dung dịch HNO3 loãng dư, thấy thoát ra khí không màu hóa nâu ngoài không khí; đồng thời thu được kết tủa Y.
- B tác dụng với C thấy khí thoát ra, đồng thời thu được kết tủa.
- A tác dụng C thu được kết tủa Z, cho Z vào dung dịch HCl dư, thấy khí không màu thoát ra.
Các chất A, B và C lần lượt là
 Xem đáp án
Xem đáp án
Đáp án C
- A tác dụng với dung dịch B:
Vậy kết tủa X gồm Fe(OH)2 và BaSO4.
- X tác dụng với HNO3 loãng dư: 3Fe(OH)2 + 10HNO3 → 3Fe(NO3)3 + NO + 8H2O.
Vậy kết tủa Y là BaSO4.
- B tác dụng với dung dịch C: Ba(OH)2 (B) + (NH4)2CO3 (C) → + + 2H2O
- A tác dụng với dung dịch C: FeSO4 (A) + (NH4)2CO3 (C) → (Z) + (NH4)2SO4
- Z tác dụng với dung dịch HCl thì: FeCO3 (Z) + 2HCl → FeCl2 + CO2 ↑ + H2O
Câu 36:
Hỗn hợp X gồm Na, K, BaO, Al2O3 (trong đó oxi chiếm 17,527% khối lượng hỗn hợp). Cho m gam hỗn hợp X tan hết vào nước thu được dung dịch Y và 3,36 lít H2 (đktc). Cho dung dịch Y tác dụng với 400ml dung dịch hỗn hợp HCl 1,25M và H2SO4 0,35M thu được 37,32 gam kết tủa T và dung dịch Z chỉ chứa 31,61 gam muối clorua và sunfat trung hoà. Phần trăm khối lượng BaO trong hỗn hợp X gần nhất với
 Xem đáp án
Xem đáp án
Đáp án D
Đổi X
Số mol điện tích kim loại (1)
Tổng khối lượng muối, kết tủa: (2)
Đặt:
Câu 37:
Hòa tan hoàn toàn hai chất rắn X, Y (có số mol bằng nhau) vào nước thu được dung dịch Z. Tiến hành các thí nghiệm sau:
Thí nghiêm 1: Cho dung dịch NaOH dư vào V ml dung dịch Z, thu được a mol kết tủa.
Thí nghiệm 2: cho dung dịch NH3 dư vào V ml dung dịch Z, thu được b mol kết tủa.
Thí nghiệm 3: Cho dung dịch AgNO3 dư vào V ml dung dịch Z, thu được c mol kết tủa.
Biết các phản ứng xảy ra hoàn toàn và a < b < c. Hai chất X, Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án D
Vì CuCl2 tạo phức với dung dịch NH3 nên a > b → loại câu A, B. Nếu đáp án là câu c thì a = b → Chỉ có D thoả mãn.
Câu 38:
Cho 30 gam hỗn hợp T gồm Mg, FeCO3, Fe và Fe(NO3)2 tác dụng vừa đủ với dung dịch HCl, kết thúc phản ứng thu được dung dịch X chứa 54,33 gam muối và 6,78 gam hỗn hợp khí Y gồm NO; H2 và 0,08 mol CO2. Cho dung dịch X tác dụng tối đa với 510 ml dung dịch NaOH 2M, thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi thu được 26,4 gam rắn. Khối lượng của kim loại Fe trong T có giá trị gần nhất với
 Xem đáp án
Xem đáp án
Đáp án C
Quy đổi hỗn hợp (T) thành Mg, Fe, CO3 và NO3 ta có sơ đồ:
.
+ Natri cuối cùng đi về NaCl (gam)
+ Bảo toàn khối lượng (mol).
+ Phương trình theo (1).
+ Bảo toàn nguyên tố hidro: 4a + 2c = 0,34 (2).
+ Phương trình theo khối lượng khí thoát ra: 30b + 2c = 3,26 (3).
Giải hệ (1) (2) và (3) ta có a = 0,02, b = 0,1 và c = 0,13.
+ Đặt và ta có:
+ PT theo (3).
+ PT theo tổng khối lượng oxit thu được: (4).
Giải hệ (3) và (4) (mol).
Câu 39:
Cho X, Y, Z là ba peptit mạch hở (có số nguyên tử cacbon trong phân tử tương ứng là 5, 7, 11); T là este no, đơn chức, mạch hở. Chia 268,32 gam hỗn hợp E gồm X, Y, Z, T thành hai phần bằng nhau. Đốt cháy hoàn toàn phần một cần vừa đủ 7,17 mol O2. Thủy phân hoàn toàn phần hai bằng dung dịch NaOH vừa đủ, thu được ancol etylic và hỗn hợp G (gồm bốn muối của Gly, Ala, Val và axit cacboxylic). Đốt cháy hoàn toàn G, thu được Na2CO3, N2, 2,58 mol CO2 và 2,8 mol H2O. Phần trăm khối lượng của Y trong E là
 Xem đáp án
Xem đáp án
Đáp án C
Hỗn hợp E
Gọi số cacbon trung bình của peptit là n, Este là .
→ Chỉ có n = 10 và m = 4 là phù hợp (vì 5 < n < 11 và ).
Số N trung bình – 0,44/0,1 = 4,4 → Z phải là Gly4Ala: a mol (vì có peptit , số C max = 11).
→ X là GlyAla: b mol.
→ Y là Gly-Val: c mol (Vì muối gồm Gly, Ala, Val → loại Gly2Ala).
→ % khối lượng của Y trong E .
Câu 40:
Cho hỗn hợp E gồm một axit hữu cơ A, no mạch hở, và 2 hợp chất hữu cơ B, C (có cùng số nguyên tử cacbon, ). Biết các hợp chất hữu cơ B, C chứa chức este của axit hữu cơ A. Đốt cháy hoàn toàn 0,06 mol hỗn hợp E cần vừa đủ 3,08 lít khí O2, thu được 4,48 lít khí CO2 và 2,07 gam nước. Mặc khác, cho 0,06 mol hỗn hợp E phản ứng vừa đủ với 60 gam dung dịch NaOH 10% đun nóng, sau phản ứng hoàn toàn, thu được dung dịch X. Cô cạn X thì thu được 9,24 gam chất rắn và phần hơi Z chỉ gồm 3 chất. Ngưng tụ rồi chia Z làm 2 phần bằng nhau, phần một cho tác dụng hoàn toàn với Na dư thì thu được 17,332 lít khí H2. Còn phần hai, thêm tiếp AgNO3 trong NH3 dư vào dung dịch thì thu được 2,7 gam kết tủa Ag. Nếu thêm từ từ NaHCO3 vào ½ hỗn hợp E cho tới khi khí ngừng thoát ra thì thu được 0,728 lít CO2. Các khí đo ở đktc, các phản ứng xảy ra hoàn toàn. Khối lượng este có phân tử lượng nhỏ hơn trong E gần nhất với giá trị nào sau đây:
 Xem đáp án
Xem đáp án
Đáp án B
Từ phản ứng đốt cháy: E + O2 → CO2 + H2O
Số nguyên tử C trung bình
Số nguyên tử H trung bình
số nguyên tử oxi trung bình = 4
Vậy: Axit A phải là: HOOC – COOH
Từ phản ứng E + NaOH
Từ
gồm
Chỉ có ancol CH3OH thỏa mãn.
→ 32.0,015 + 0,0125.M = 1,03 → M = 44 (CH3CHO)
Theo đầu bài, vì B và C có cùng số cacbon ()
Vậy 1/2E gồm
Khối lượng este B có phân tử lượng nhỏ hơn trong E là: (gam).
