Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (Đề 3)
-
6390 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn B.
Câu 4:
 Xem đáp án
Xem đáp án
Chọn C.
Câu 5:
 Xem đáp án
Xem đáp án
Chọn A.
Câu 7:
 Xem đáp án
Xem đáp án
Chọn B.
Câu 10:
 Xem đáp án
Xem đáp án
Chọn B.
Câu 11:
 Xem đáp án
Xem đáp án
Chọn A.
Câu 19:
 Xem đáp án
Xem đáp án
Chọn C.
Ăn mòn điện hóa xuất hiện khi có cặp cực tiếp xúc với nhau và cùng tiếp xúc với môi trường điện ly.
Chọn (Cặp Ni-Cu) và AgNO3 (Cặp Ni-Ag).
Câu 21:
 Xem đáp án
Xem đáp án
Chọn A.
Câu 22:
 Xem đáp án
Xem đáp án
Chọn B.
Câu 24:
 Xem đáp án
Xem đáp án
Chọn C.
nên H3PO4 và OH- đều hết.
Bảo toàn khối lượng:
m muối
m muối = 4,7 gam.
Câu 25:
 Xem đáp án
Xem đáp án
Chọn B.
(X có 9H)
Câu 26:
 Xem đáp án
Xem đáp án
Chọn A.
HNO3 dư nên sản phẩm là Fe3+
Bảo toàn electron
gamCâu 27:
Thủy phân hoàn toàn 10,56 gam este X trong dung dịch NaOH, sau phản ứng thu được muối của axit cacboxylic đơn chức và 3,84 gam ancol metylic. Công thức của X là
 Xem đáp án
Xem đáp án
Chọn D.
Câu 28:
Hình vẽ sau đây mô tả thí nghiệm điều chế chất hữu cơ Y:
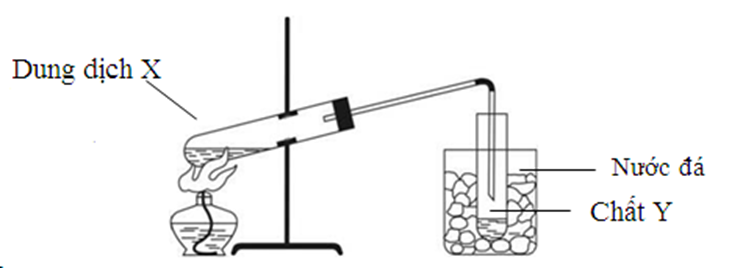
Phản ứng nào sau đây xảy ra trong thí nghiệm trên?
 Xem đáp án
Xem đáp án
Chọn C.
Loại ngay B, D vì không sinh ra chất hữu cơ ở dạng hơi.
Theo hình vẽ thì chất hữu cơ Y được sinh ra ở dạng hơi và ngưng tụ lại trong cốc đựng nước đá
Nhiệt độ hóa lỏng không quá thấp.
Phản ứng phù hợp:
Câu 29:
 Xem đáp án
Xem đáp án
Chọn C.
đốt ankan = gam
Câu 30:
 Xem đáp án
Xem đáp án
Chọn D.
Câu 31:
Cho các phát biểu sau:
(a) Cho Mg tác dụng với dung dịch FeCl3 dư, thu được kim loại Fe
(b) Cho kim loại Ba tác dụng với dung dịch CuSO4 thu được kim loại Cu
(c) Cho AgNO3 dư tác dụng với dung dịch FeCl2 thu được kim loại Ag
(d) Để gang trong không khí ẩm lâu ngày có xảy ra ăn mòn điện hóa học
(e) Dùng bột lưu huỳnh để xử lí thủy ngân khi nhiệt kế bị vỡ
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn C.
(a) Sai, dư
(b) Sai,
(c) Đúng,
(d) Đúng, cặp điện cực Fe-C
(e) Đúng, (chất rắn, ít độc hơn và dễ thu gom)
Câu 32:
. Tiến hành thí nghiệm sau:
- Bước 1: Cho vào ống nghiệm 2ml nước cất
- Bước 2: Nhỏ tiếp vài giọt anilin vào ống nghiệm, lắc đều, sau đó nhúng giấy quỳ tím vào dung dịch trong ống nghiệm
- Bước 3: Nhỏ tiếp 1ml dung dịch HCl đặc vào ống nghiệm
Cho các phát biểu sau:
(a) Sau bước 2, dung dịch thu được trong suốt
(b) Sau bước 2, giấy quỳ tím chuyển thành màu xanh
(c) Sau bước 3, dung dịch thu được trong suốt
(d) Sau bước 3, trong dung dịch có chứa muối phenylamoni clorua tan tốt trong nước
Số phát biểu đúng là Xem đáp án
Xem đáp án
Chọn C.
(1) Sai, anilin không tan nên phân lớp.
(2) Sai, anilin có tính bazơ rất yếu, không làm đổi màu quỳ tím.
(3) Đúng: (tan)
(4) Đúng
(5) Đúng
Câu 33:
Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Quỳ tím |
Chuyển màu đỏ |
|
Y |
Dung dịch I2 |
Có màu xanh tím |
|
Z |
Dung dịch AgNO3 trong NH3 |
Kết tủa trắng |
|
T |
Nước brom |
Kết tủa trắng |
Các chất X, Y, Z, T lần lượt là
 Xem đáp án
Xem đáp án
Chọn C.
Câu 34:
Cho các nhận định sau:
(a) Trong y học, glucozơ được dùng làm thuốc tăng lực
(b) Trong công nghiệp dược phẩm, saccarozơ được dùng để pha chế thuốc
(c) Trong công nghiệp, một lượng lớn chất béo dùng để điều chế xà phòng và glixerol
(d) Phản ứng thế brom vào vòng thơm của anilin dễ hơn benzen
(e) Tơ tằm thuộc loại tơ nhân tạo
Số nhận định đúng là
 Xem đáp án
Xem đáp án
Chọn B.
(a) Đúng
(b) Đúng
(c) Đúng
(d) Đúng, do nhóm NH2 hoạt hóa vòng thơm.
(e) Sai, tơ tằm là tơ thiên nhiênCâu 35:
 Xem đáp án
Xem đáp án
Chọn B.
Các axit béo gọi chung là A. Các muối đều 18C nên X có 57C và A có 18C.
Số
Trong phản ứng xà phòng hóa: và
Quy đổi E thành và
Câu 36:
Cho sơ đồ phản ứng theo đúng tỉ lệ mol:
(a) X + 2NaOH → X1 + X2 + X3 (b) X1 + HCl → X4 + NaCl
(c) X2 + HCl → X5 + NaCl (d) X3 + CuO → X6 + Cu + H2O
Biết X có công thức phân tử C6H10O4 và chứa hai chức este: X1; X2 đều có hai nguyên tử cacbon trong phân tử và khối lượng mol của X1 nhỏ hơn khối lượng mol của X2. Phát biểu nào sau đây sai? Xem đáp án
Xem đáp án
Chọn A.
đều là các muối natri.
X1, X2 cùng C nên mỗi chất 2C là:
X1 là CH3COONa
X2 là
X3 là C2H5OH
X4 là CH3COOH
X5 là HO-CH2-COOH
X6 là CH3CHO
Phát biểu sai: Phân tử X2 có hai nguyên tử oxi.Câu 37:
 Xem đáp án
Xem đáp án
Chọn B.
>> Lập hệ khối lượng kim loại (11,6 gam) và khối lượng 2 oxit kim loại (16 gam) tính được:
>> Lập hệ tổng khối lượng chất rắn (KNO2 & KOH dư) 41,05 gam và tổng số mol (0,5 mol, bằng KOH ban đầu) tính được:
dư = 0,05
Bảo toàn thoát ra ở khí
Nhận thấy Tạo ra cả muối Fe3+ (a) và đã hết.
và b = 0,1
Phần khí quy đổi thành N (0,25) và O (u mol)
Bảo toàn electron:
m kim loại +
Dung dịch Z chứa 3 muối và và
C%Fe(NO3)2 = 20,18%
Câu 38:
 Xem đáp án
Xem đáp án
Chọn B.
Đốt và
và v = 0,56
Quy đổi E thành HCOOH (a), (COOH)2 (b), CH3OH (0,16), H2O (-0,16), CH2 (c) và H2 (-0,12)
và
Đốt X hoặc Y đều có nên X có k = 3 và Y có k = 2
X dạng
Y là
Muối gồm và
Câu 39:
 Xem đáp án
Xem đáp án
Chọn D.
Quy đổi E thành
gam
Bảo toàn khối lượng:
m muối
m muối = 10,78
Số N của là Gly-Ala-Val
là
Câu 40:
 Xem đáp án
Xem đáp án
Chọn B.
CH3OH và RCOOH phản ứng vừa đủ tạo este nên chúng cùng số mol
và –C2H5 (29)
và C2H5COOH