Bộ đề thi thử môn Hóa THPT Quốc gia năm 2022 có lời giải (30 đề)
Bộ đề thi thử THPT Quốc gia năm 2022 môn Hóa có lời giải (Đề 17)
-
6694 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Thủy phân hoàn toàn một tripeptit X (mạch hở) thu được hỗn hợp gồm alanin và glyxin theo tỷ lệ mol là 2 : 1. Số tripeptit thỏa mãn công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Chọn C.
X là X có các đồng phân mạch hở:
Ala-Ala-Gly
Ala-Gly-Ala
Gly-Ala-Ala
Câu 2:
Chất Có khả năng thao gia phản ứng trùng hợp tạo polime là
 Xem đáp án
Xem đáp án
Câu 3:
Tiến hành các thí nghiệm sau:
(a) Cho Mg vào dung dịch Fe2(SO4)3 dư
(b) Sục khí Cl2 vào dung dịch FeCl2
(c) Dẫn khí H2 dư qua bột CuO nung nóng
(d) Cho Na vào dung dịch CuSO4 dư
(e) Nhiệt phân AgNO3
(g) Đốt FeS2 trong không khí
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
 Xem đáp án
Xem đáp án
Chọn C.
(1) dư
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10) Zn dư (Thu được Zn dư).
Câu 4:
Chất khí X có thể được dùng làm chất dập tắt đám cháy. Công thức phân tử của khí X là
 Xem đáp án
Xem đáp án
Câu 5:
Thí nghiệm nào dưới đây không xảy ra phản ứng?
 Xem đáp án
Xem đáp án
Câu 7:
Cho các dung dịch riêng biệt: HNO3, Ba(OH)2, NaHSO4, H2SO4, NaOH. Số dung dịch tác dụng với dung dịch Ba(HCO3)2 tạo kết tủa là
 Xem đáp án
Xem đáp án
Chọn C.
Ba(OH)2
NaHSO4
H2SO4
NaOH
Câu 9:
Sục khí CO2 dư vào dung dịch chất X, thu được chất kết tủa. Chất X là
 Xem đáp án
Xem đáp án
Câu 11:
Để làm mềm nước cứng có chứa các ion Ca2+, Mg2+, Cl- người ta có thể
 Xem đáp án
Xem đáp án
Câu 13:
Etylamin (C2H5NH2) tác dụng được với chất nào sau đây trong dung dịch?
 Xem đáp án
Xem đáp án
Câu 15:
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (điện cực trơ), thu được khí H2 ở catot.
(b) Cho CO dư qua hỗn hợp Al2O3 và CuO đun nóng, thu được Al và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
Trong các phát biểu trên, số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn C.
(a) Đúng
(b) Sai, thu được Al2O3 và Cu
(c) Đúng, điện cực Zn-Cu
(d) Đúng
Câu 16:
Este CH3COOCH=CH2 không tác dụng được với hóa chất nào sau đây ?
 Xem đáp án
Xem đáp án
Câu 18:
Cho các chất: CH2=CH2, C6H5OH (phenol), CH3COOH, C6H5NH2 (anilin). Số chất làm mất màu dung dịch nước brom trong nước là:
 Xem đáp án
Xem đáp án
Câu 20:
Cacbohidrat X có đặc điểm:
- Bị thủy phân trong môi trường axit
- Thuộc loại polisaccarit
- Phân tử gồm nhiều gốc β-glucozơ
Cacbohidrat X là
 Xem đáp án
Xem đáp án
Câu 22:
Nguyên tử X có số hiệu nguyên tử Z = 12. Cấu hình electron lớp ngoài cùng của ion tạo ra từ X là
 Xem đáp án
Xem đáp án
Câu 24:
Trong môi trường kiềm, protein có khả năng phản ứng màu biure với
 Xem đáp án
Xem đáp án
Câu 25:
Phản ứng của este với dung dịch kiềm gọi là phản ứng
 Xem đáp án
Xem đáp án
Câu 26:
Để điều chế este etyl axetat bằng phản ứng este hóa, người ta cho axit axetic tác dụng với chất nào sau đây ?
 Xem đáp án
Xem đáp án
Câu 27:
Ở điều kiện thường, chất nào sau đây ở trạng thái lỏng
 Xem đáp án
Xem đáp án
Câu 29:
Cho hình vẽ mô tả thí nghiệm điều chế khí X khi cho dung dịch axit tác dụng với muối rắn
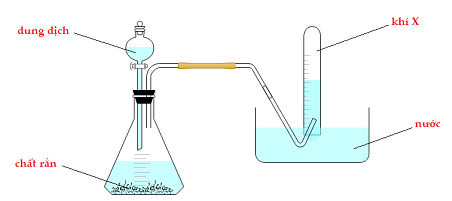
Hình vẽ trên không sử dụng điều chế khí nào sau đây?
 Xem đáp án
Xem đáp án
Chọn B.
Khí X thu bằng phương pháp dời nước nên X không tan hoặc có độ tan vừa phải.
không thể là HCl, vì HCl tan rất tốt (ở điều kiện thường 1 lít H2O hòa tan hết khoảng 400 lít HCl)
Câu 30:
Sục CO2 vào dung dịch Ca(OH)2 và NaOH ta thu được kết quả như hình vẽ.
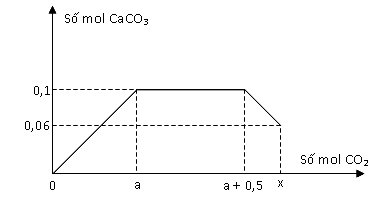
Giá trị của x là:
 Xem đáp án
Xem đáp án
Chọn C.
Đoạn 1: Tạo CaCO3
Đoạn 2: Tạo NaHCO3
đoạn này = 0,5
Đoạn 3: Hòa tan một phần CaCO3.
Các chất tại điểm đang xét gồm
Bảo toàn
Câu 31:
Cho 100ml dung dịch HCl aM tác dụng vừa đủ với 4,5 gam một amin đơn chức, sau phản ứng thu được 8,15 gam muối. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn D.
Câu 32:
Dung dịch X chứa 0,01 mol Fe(NO3)3 và 0,15 mol HCl có khả năng hòa tan tối đa bao nhiêu gam Cu kim loại ? (Biết NO là sản phẩm khử duy nhất của N+5)
 Xem đáp án
Xem đáp án
Chọn D.
nhận tổng
gam
Câu 33:
 Xem đáp án
Xem đáp án
Chọn D.
phản ứng
Bảo toàn liên kết pi:
phản ứng
Câu 34:
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hợp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa thu được dung dịch Y chứa 3 chất tan với tỉ lệ 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KmnO4 trong môi trường axit sunfuric?
 Xem đáp án
Xem đáp án
Chọn A.
và dư = 3x
và
Bảo toàn electron:
gam
Câu 35:
Hỗn hợp X gồm ba triglixerit được tạo bởi axit oleic và axit linoleic (có tỉ lệ mol tương ứng của hai axit là 2 : 1). Đốt cháy hoàn toàn a gam X thu được 37,62 gam CO2 và 13,77 gam H2O. Mặt khác, hiđro hóa hoàn toàn 2a gam X thu được chất hữu cơ Y. Đun Y với dung dịch KOH (vừa đủ) thu được glixerol và m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
X có công thức chung
và
Y là
Vậy từ 2a gam m muối
Câu 36:
Đốt cháy hết a gam chất hữu cỡ cần vừa đủ 30,8 lít không khí (20% O2 về thể tích, còn lại là N2). Cho sản phẩm cháy vào dung dịch nước vôi trong dư, thấy thoát ra 28 lít một chất khí, phản ứng thu được 30 gam một chất kết tủa và khối lượng dung dịch nước vôi giảm 6,9 gam so với ban đầu. Nếu cho a gam chất X tác dụng vừa đủ với 300ml dung dịch NaOH 1M tạo thành nước, 1 chất hữu cơ đa chức bậc I và m gam hỗn hợp muối vô cơ (các khí đo ở đktc, X có công thức đơn giản nhấ trùng với công thức phân tử). Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
n không khí và
tổng sản phẩm cháy
dư
là
chất hữu cơ đa chức bậc 1 + các muối vô cơ
là
Các muối gồm và
m muối = 19,10 gam
Câu 37:
Đốt cháy hoàn toàn hỗn hợp gồm metyl axetat và etyl axetat, thu được CO2 và m gam nước. Hấp thụ toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư, thu được 25 gam kết tủa. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn A.
dư
Các este đều no, đơn chức, mạch hở nên
gam.
Câu 38:
Cho 4,825 gam hỗn hợp bột Al và Fe (có tỉ lệ mol nAl : nFe = 3 : 2) vào 350 ml dung dịch AgNO3 1M. Khuấy kĩ cho phản ứng xảy ra hoàn toàn, thu được m gam chất rắn. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B.
Dễ thấy
phản ứng hết.
Chất rắn chỉ có
Câu 39:
Điện phân dung dịch X gồm Cu(NO3)2 và NaCl với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi I = 2,5A. Sau t giây, thu được 7,68 gam kim loại ở catot, dung dịch Y (vẫn còn màu xanh) và hỗn hợp khí ở anot có tỉ khối so với H2 bằng 25,75. Mặt khác, nếu điện phân X trong thời gian 12352 giây thì tổng số mol khí thu được ở hai điện cực là 0,11 mol. Giả thiết hiệu suất điện phân là 100%, các khí sinh ra không tan trong nước và nước không bay hơi trong quá trình điện phân. Số mol ion Cu2+ trong Y là
 Xem đáp án
Xem đáp án
Chọn B.
Sau t giây:
Catot:
Anot: và
Bảo toàn eletron
m khí
Khi thời gian là 12352 giây thì
Catot: và
Anot: và
Bảo toàn electron:
n khí
Bảo toàn electron: phản ứng
phản ứng = 0,09
gam.
Câu 40:
Thủy phân hoàn toàn 0,2 mol một este X cần dùng vừa đủ 100 gam dung dịch NaOH 24%, thu được một ancol Y và 43,6 gam hỗn hợp muối của hai axit cacboxylic đơn chức Z và T. Công thức của Z và T là
 Xem đáp án
Xem đáp án
Chọn A.
Vì nên E là este 3 chức
Sản phẩm thu được chứa 2 muối nên E có dạng
Muối gồm và
và B = 1 là nghiệm duy nhất.
Muối gồm HCOONa và CH3COONa
Các axit tương ứng là HCOONa và CH3COOH.
