[Năm 2022] Đề minh họa môn Hóa THPT Quốc gia có lời giải (25 đề)
[Năm 2022] Đề minh họa môn Hóa THPT Quốc gia có lời giải (Đề 11)
-
4993 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Kim loại nào sau đây dẫn điện tốt nhất?
 Xem đáp án
Xem đáp án
- Nhẹ nhất: Li (0,5g/cm3)
- Nặng nhất Os (22,6g/cm3).
- Nhiệt độ nc thấp nhất: Hg (−390C)
- Nhiệt độ cao nhất W (34100C).
- Kim loại mềm nhất là Cs (K, Rb) (dùng dao cắt được)
- Kim loại cứng nhất là Cr (có thể cắt được kính).
- Kim loại dẫn điện, dẫn nhiệt tốt nhất là Ag
Câu 2:
 Xem đáp án
Xem đáp án
Câu 3:
 Xem đáp án
Xem đáp án
Câu 4:
Kim loại nào sau đây có thể tan hoàn toàn trong nước ở điều kiện thường?
 Xem đáp án
Xem đáp án
Câu 5:
 Xem đáp án
Xem đáp án
Câu 6:
 Xem đáp án
Xem đáp án
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Câu 7:
 Xem đáp án
Xem đáp án
Câu 8:
 Xem đáp án
Xem đáp án
Câu 9:
Các bể đựng nước vôi trong để lâu ngày thường có một lớp màng cứng rất mỏng trên bề mặt, chạm nhẹ tay vào đó, lớp màng sẽ vỡ ra. Thành phần chính của lớp màng cứng này là
 Xem đáp án
Xem đáp án
Câu 10:
 Xem đáp án
Xem đáp án
Câu 11:
 Xem đáp án
Xem đáp án
Câu 12:
 Xem đáp án
Xem đáp án
Câu 14:
Etyl axetat bị thuỷ phân trong dung dịch NaOH cho sản phẩm muối nào sau đây?
 Xem đáp án
Xem đáp án
Câu 15:
 Xem đáp án
Xem đáp án
Câu 16:
Ở điều kiện thường chất nào sau đây tồn tại trạng thái khí?
 Xem đáp án
Xem đáp án
Câu 17:
 Xem đáp án
Xem đáp án
PTHH: 2CH3NH2 + H2SO4 → (CH3NH3)2SO4.
Câu 18:
 Xem đáp án
Xem đáp án
Câu 19:
 Xem đáp án
Xem đáp án
Câu 20:
 Xem đáp án
Xem đáp án
Câu 21:
 Xem đáp án
Xem đáp án
Câu 22:
 Xem đáp án
Xem đáp án
→ Este X chỉ có thể đơn chức và có thể có dạng RCOOCH = CH2 → MR = 29 (-C2H5)
Vậy X có công thức phân tử là C5H8O2
Các công thức cấu tạo phù hợp của X là
HCOOCH = CH– CH2 – CH3
HCOOCH = C(CH3) – CH3
CH3COOCH = CH – CH3
C2H5COOCH = CH2
Câu 23:
 Xem đáp án
Xem đáp án
Câu 24:
 Xem đáp án
Xem đáp án
2) Cu + 2FeCl3 → CuCl2 + 2FeCl2
3) 2FeCl3 + Fe → 3FeCl2
4) 3AgNO3 + FeCl3 → 3AgCl ↓ + Fe(NO3)3
Câu 25:
 Xem đáp án
Xem đáp án
Câu 26:
 Xem đáp án
Xem đáp án
PTHH: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3.
Vậy muối thu được là natri stearat.
Câu 27:
 Xem đáp án
Xem đáp án
Y là chất rắn dạng sợi, màu trắng, không có mùi vị
Câu 28:
 Xem đáp án
Xem đáp án
(C6H10O5)n → nC6H12O6 → 2nC2H5OH + 2nCO2
Theo PTHH → nC6H12O6 (LT) = nCO2/2 = nCaCO3/2 = 0,06 (mol)
→ ntinh bột (LT) = nC6H12O6(LT)/n = 0,06/n (mol).
Do H = 90% → ntinh bột (TT) = (0,06/n).(100%/90%) = 1/15n (mol).
Vậy m = 162n.1/15n = 10,8 (gam).
Câu 29:
 Xem đáp án
Xem đáp án
PTHH: HOOC – R – NH2 + HCl → HOOC – R – NH3Cl
BTKL mHCl = mmuối – mX = 2,92 (gam) nHCl = 0,08 (mol).
Theo PTHH nX = nHCl = 0,08 (mol)
MX = 45 + MR + 16 = 8,24/0,08 = 103 MR = 42 (-C3H6).
CTCT của α-amino axit X là H2NCH(C2H5)COOH.
Câu 30:
 Xem đáp án
Xem đáp án
B sai, đa số polime không tan trong các dung môi thông thường.
C sai, hầu hết polime là các chất rắn không bay hơi.
Câu 31:
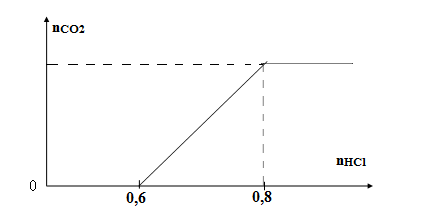
 Xem đáp án
Xem đáp án
Khi thì khí thoát ra hết nên
Câu 32:
(a) Các oxit của kim loại kiềm thổ đều tan tốt trong nước.
(b) Thạch cao nung được sử dụng để bó bột trong y học.
(c) Cho bột Al dư vào dung dịch FeCl3, phản ứng hoàn toàn thu được dung dịch chứa AlCl3 và FeCl2.
(d) Sục khí CO2 đến dư vào dung dịch NaAlO2 thu được kết tủa.
(e) Các kim loại kiềm khử nước dễ dàng ở nhiệt độ thường và giải phóng khí hiđro.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(b) Đúng
(c) Sai, Al dư
(d) Đúng, CO2 dư + FeCl3 AlCl3 + Fe
(e) Đúng
Câu 33:
 Xem đáp án
Xem đáp án
Đietylamin: C4H11N = C4H10 + NH
Etyl propionat: C5H10O2
Valin: C5H11O2N = C5H10O2 + NH
→ Quy đổi hỗn hợp thành C4H10, C5H10O2, NH
Sơ đồ:
+ nhh X = x + y = 0,4 (1)
+ BTNT O → 2nC5H10O2 + 2nO2 = 2nCO2 + nH2O
→ 2y + 2.2,66 = 2.(4x + 5y) + 5x + 5y + 0,5z
→ 13(x + y) + 0,5z = 5,32 (2)
Thay (1) vào (2) → z = 0,24.
Khí không bị hấp thụ là N2 → nN2 = 0,5z = 0,12 mol.
Câu 34:
(a) Có thể dùng giấm ăn để giảm mùi tanh của cá.
(b) Thủy phân hoàn toàn các triglixerit đều thu được glixerol.
(c) Cao su lưu hóa có tính đàn hồi tốt hơn cao su chưa lưu hóa.
(d) Khi nấu canh cua, riêu cua nổi lên trên là hiện tượng đông tụ protein.
(e) Vải làm từ tơ nilon-6,6 kém bền trong nước xà phòng có tính kiềm.
(g) Muối mononatri glutamat được sử dụng làm mì chính (bột ngọt).
Số nhận xét đúng là
 Xem đáp án
Xem đáp án
(b) đúng vì triglixerit là este của glixerol và axit béo.
(c) đúng.
(d) đúng.
(e) đúng vì vải làm từ nilon - 6,6 có nhóm CONH kém bền trong môi trường kiềm.
(g) đúng.
Câu 35:
 Xem đáp án
Xem đáp án
nH2=0,35 mol;
m(X)=23a+137b+16c=107,9 (1)
Áp dụng BTe a+2b-2c=0,35*2 (2)
n(NaOH) = a=0.7 mol (3)
Kết hợp 1,2,3 → a=0,7; b=0,6; c=0,6
ddY có nNa(+)=0,7; nBa(2+)=0.6; n(OH-)=1.9
n(OH-)/n(SO2)=1,9/0,8=2,375 >2 → tạo muối SO32-
SO2 + 2OH- → SO32-
0,8 0,8
nSO32- > nBa2+ → m=0,6*217=130,2 g
Câu 36:
 Xem đáp án
Xem đáp án
C2H8N2O3 là C2H5NH3NO3 (2x mol)
Muối gồm NaNO3 (2x) và Na2CO3 (3x)
m muối = 85.2x + 106.3x = 4,88 x = 0,01
Câu 37:
 Xem đáp án
Xem đáp án
nMg phản ứng
Bảo toàn electron:
Bảo toàn
Dung dịch muối chứa
m muối = 29,8
Câu 38:
 Xem đáp án
Xem đáp án
nO2 đốt Y = 0,25
đốt Z = 0,46 – 0,25 = 0,21
Z no, đơn chức, mạch hở nên
Nếu X mạch hở thì Z là C2H5OH
Bảo toàn khối lượng
Đặt a, b là số mol CO2 và H2O
Và
và b = 0,28
Số C = 5,57 và và
Các muối gồm và
là nghiệm duy nhất.
X gồm:
Câu 39:
 Xem đáp án
Xem đáp án
Gọi chất béo là A, các axit béo tự do là B.
Các axit béo đều no nên chất béo có k = 3
Bảo toàn O:
Bảo toàn khối lượng:
m muối +
m muối = 10,68.
Câu 40:
- Bước 2: Thêm 10 ml dung dịch H2SO4 20% vào bình thứ nhất, 20 ml dung dịch NaOH 30% vào bình thứ hai.
- Bước 3: Lắc đều cả hai bình, lắp ống sinh hàn, đun sôi nhẹ trong 5 phút, sau đó để nguội.
Cho các phát biểu sau:
(a) Kết thúc bước 2, chất lỏng trong hai bình đều phân thành hai lớp.
(b) Ở bước 3, có thể thay việc đun sôi nhẹ bằng đun cách thủy (ngâm trong nước nóng).
(c) Ở bước 3, trong bình thứ hai có xảy ra phản ứng xà phòng hóa.
(d) Sau bước 3, trong hai bình đều chứa chất có khả năng tham gia phản ứng tráng bạc.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(b) Đúng
(c) Đúng
(d) Đúng, đó là HCOOH và HCOONa.
