[Năm 2022] Đề minh họa môn Hóa THPT Quốc gia có lời giải (25 đề)
[Năm 2022] Đề minh họa môn Hóa THPT Quốc gia có lời giải (Đề 12)
-
5010 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
- Nhẹ nhất: Li (0,5g/cm3)
- Nặng nhất Os (22,6g/cm3).
- Nhiệt độ nc thấp nhất: Hg (−390C)
- Nhiệt độ cao nhất W (34100C).
- Kim loại mềm nhất là Cs (K, Rb) (dùng dao cắt được)
- Kim loại cứng nhất là Cr (có thể cắt được kính).
- Kim loại dẫn điện, dẫn nhiệt tốt nhất là Ag
Câu 2:
 Xem đáp án
Xem đáp án
Câu 3:
 Xem đáp án
Xem đáp án
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Câu 4:
 Xem đáp án
Xem đáp án
K Na Mg Al Zn Fe Ni Sn Pb H2 Cu Fe2+ Ag Hg Pt Au
Câu 5:
 Xem đáp án
Xem đáp án
Câu 6:
 Xem đáp án
Xem đáp án
Câu 7:
 Xem đáp án
Xem đáp án
Câu 8:
 Xem đáp án
Xem đáp án
Câu 9:
 Xem đáp án
Xem đáp án
Câu 10:
 Xem đáp án
Xem đáp án
Câu 11:
 Xem đáp án
Xem đáp án
Câu 12:
 Xem đáp án
Xem đáp án
Câu 13:
 Xem đáp án
Xem đáp án
Câu 14:
 Xem đáp án
Xem đáp án
Câu 15:
 Xem đáp án
Xem đáp án
Câu 16:
 Xem đáp án
Xem đáp án
Câu 17:
 Xem đáp án
Xem đáp án
Câu 18:
 Xem đáp án
Xem đáp án
PTHH: nCH2=CHCl (-CH2-CH(Cl)-)n
Câu 19:
 Xem đáp án
Xem đáp án
Câu 20:
 Xem đáp án
Xem đáp án
Câu 21:
 Xem đáp án
Xem đáp án
Câu 22:
 Xem đáp án
Xem đáp án
Câu 23:
 Xem đáp án
Xem đáp án
Câu 24:
 Xem đáp án
Xem đáp án
PTHH:
Fe + Fe2(SO4)3 → 3FeSO4
→ Dung dịch Y chứa 1 chất tan duy nhất là FeSO4.
FeSO4 + Ba(OH)2 → BaSO4 ↓ + Fe(OH)2 ↓
→ Hai chất rắn thu được sau phản ứng gồm BaSO4 và Fe(OH)2.
Câu 25:
 Xem đáp án
Xem đáp án
Câu 26:
 Xem đáp án
Xem đáp án
Câu 27:
 Xem đáp án
Xem đáp án
PTHH: HOCH2[CHOH]4CHO + 2AgNO3 + 3NH3 + H2O HOCH2[CHOH]4COONH4 + 2Ag ↓ + 2NH4NO3.
Câu 28:
 Xem đáp án
Xem đáp án
342 180
136,8 m
Câu 29:
 Xem đáp án
Xem đáp án
Ta có:
→ CTPT là C3H9N.
Câu 30:
 Xem đáp án
Xem đáp án
(1) là polime thiên nhiên.
(2) là polime bán tổng hợp (nhân tạo).
Câu 31:
 Xem đáp án
Xem đáp án
Câu 32:
(a) Cho Cu dư vào dung dịch Fe(NO3)3.
(b) Sục khí CO2 dư vào dung dịch NaOH.
(c) Cho dung dịch Na2CO3 dư vào dung dịch Ca(HCO3)2.
(d) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
(e) Hoà tan hỗn hợp rắn gồm Na và Al (có cùng số mol) vào lượng nước dư.
(f) Sục khí Cl2 dư vào dung dịch FeCl2.
Sau khi các phản ứng xảy ra hoàn toàn, dung dịch thu được chứa một muối tan
 Xem đáp án
Xem đáp án
→ không thỏa mãn vì thu được 2 muối là Cu(NO3)2, Fe(NO3)2.
(b) CO2 dư + NaOH → NaHCO3
→ thỏa mãn vì thu được 1 muối là NaHCO3.
(c) Na2CO3 dư + Ca(HCO3)2 → CaCO3 ↓ + 2NaHCO3
→ không thỏa mãn vì thu được 2 muối là NaHCO3 và Na2CO3 dư.
(d) Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
→ không thỏa mãn vì thu được 2 muối là Fe(NO3)3 và AgNO3 dư.
(e) 2Na + 2H2O → 2NaOH + H2
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
→ thỏa mãn vì thu được muối duy nhất là NaAlO2.
(d) Cl2 dư + 2FeCl2 → 2FeCl3
→ thỏa mãn vì thu được muối duy nhất là FeCl3.
Vậy có 3 dung dịch chứa 1 muối tan.
Câu 33:
 Xem đáp án
Xem đáp án
Câu 34:
(a) Hợp chất CH3COONH3CH3 có tên gọi là metyl aminoaxetat.
(b) Cho glucozơ vào ống nghiệm đựng dung dịch H2SO4 đặc, đun nóng thấy cốc chuyển sang màu đen, có bọt khí sinh ra.
(c) Dung dịch anilin làm quỳ tím chuyển sang màu xanh.
(d) Thủy phân hoàn toàn protein đơn giản chỉ thu được hỗn hợp các α-aminoaxit.
(e) Fructozơ và glucozơ là đồng phân cấu tạo của nhau.
(g) Hidro hóa hoàn toàn triolein (bằng H2, xúc tác Ni, đun nóng) thu được tristearin.
Số nhận xét đúng là
 Xem đáp án
Xem đáp án
(1) Sai vì đây là metylamoni axetat còn metyl aminoaxetat là NH2COOCH3
(2) Đúng vì H2SO4 đặc có tính háo nước sẽ rút H2O của đường còn lại cacbon (màu đen) và khí là do C phản ứng với H2SO4 tạo CO2 và SO2
(3) Sai vì anilin không làm đổi màu cả phenolphtalein và quỳ tím
(4) Đúng vì protein đơn giản chỉ tạo từ các a-aminoaxit, protein phức tạp mới có thêm các thành phần phi protein.
Câu 35:
 Xem đáp án
Xem đáp án
Câu 36:
 Xem đáp án
Xem đáp án
Câu 37:
 Xem đáp án
Xem đáp án
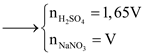
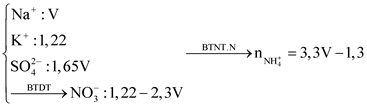

Câu 38:
 Xem đáp án
Xem đáp án
Gọi số mol triglixerit, axit béo trong X và số mol CO2 khi đốt cháy X lần lượt là x, y và z (mol)
* Xét phản ứng với NaOH
Ta có nNaOH = 3ntriglixerit + naxit béo = 3x + y = 0,25 (1)
X + NaOH → muối + C3H5(OH)3 (x mol) + H2O (y mol)
Áp dụng BTKL → m = mX = 69,78 + 92x + 18y – 0,25.40 = 92x + 18y + 59,78 (gam).
* Xét phản ứng đốt cháy
X + O2 (6,06 mol) → CO2 (z mol) + H2O
+ Axit béo trong X có 1 liên kết π trong phân tử → nCO2 = nH2O (khi đốt cháy).
+ Triglixerit trong X có 3 liên kết π trong phân tử → nCO2 – nH2O = 2ntriglixerit
→ Đốt cháy X ta có: nH2O = nCO2 – 2ntriglixerit = z – 2x (mol).
BTNT O → 6x + 2y + 6,06.2 = 2z + z – 2x → 8x + 2y – 3z = -12,12 (2)
BTKL → mX + mO2 = mCO2 + mH2O
→ 92x + 18y + 59,78 + 6,06.32 = 44z + 18z – 18.2x → 128x + 18y – 62z = -253,7 (3)
Từ (1)(2) và (3) → x = 0,08 ; y = 0,01 và z = 4,26.
Vậy m = 92x + 18y + 59,78 = 67,32 gam.
Câu 39:
 Xem đáp án
Xem đáp án
Câu 40:
Thực hiện thí nghiệm theo các bước như sau:
Bước 1: Thêm 4 ml ancol isoamylic và 4 ml axit axetic kết tinh và khoảng 2 ml H2SO4 đặc vào ống nghiệm khô. Lắc đều.
Bước 2: Đưa ống nghiệm vào nồi nước sôi từ 10 - 15 phút. Sau đó lấy ra và làm lạnh.
Bước 3: Cho hỗn hợp trong ống nghiệm vào một ống nghiệm lớn hơn chứa 10 ml nước lạnh.
Cho các phát biểu sau:
(a) Tại bước 2 xảy ra phản ứng este hóa.
(b) Sau bước 3, hỗn hợp chất lỏng tách thành hai lớp.
(c) Có thể thay nước lạnh trong ống nghiệm lớn ở bước 3 bằng dung dịch NaCl bão hòa.
(d) Sau bước 3, hỗn hợp chất lỏng thu được có mùi chuối chín.
(e) H2SO4 đặc đóng vai trò chất xúc tác và hút nước để chuyển dịch cân bằng.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
(a) đúng, khi đun nóng sẽ xảy ra phản ứng este hóa.
(b) đúng, do nước lạnh làm giảm độ tan của este.
(c) đúng, NaCl bão hòa sẽ làm tăng khối lượng riêng của lớp chất lỏng phía dưới khiến cho este dễ dàng nổi lên.
(d) đúng, vì phản ứng tạo este isoamyl axetat có mùi chuối chín.
(e) đúng.
