Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (30 đề)
Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (Đề 19)
-
6199 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 2:
Trên thế giới, mía là loại cây được trồng với diện tích rất lớn, cung cấp nguyên liệu đầu vào chủ yếu cho sản xuất đường (còn lại từ củ cải đưởng). Cacbonhiđrat trong đường mía thuộc loại
 Xem đáp án
Xem đáp án
Câu 3:
 Xem đáp án
Xem đáp án
Câu 4:
Cho các chất sau: Al, Cr, CO2, FeCl2, NaHCO3, CuSO4, MgCl2. Số chất phản ứng với dung dịch NaOH loãng nóng là
 Xem đáp án
Xem đáp án
Chọn D
Trừ Cr không phản ứng, các chất còn lại có phản ứng với dung dịch NaOH loãng nóng.
Câu 5:
Cho các chất sau: propin, but-2-in, etanal, vinylaxetilen, axit metanoic, glucozơ. saccarozơ, metyl axetat. Số chất phản ứng với dung dịch AgNO3 trong NH3 là
 Xem đáp án
Xem đáp án
Chọn B
Các chất chứa CH≡C-, -CHO, HCOO- có phản ứng với dung dịch AgNO3 trong NH3:
propin: CH≡C-CH3
etanal: CH3-CHO
vinylaxetilen: CH≡C-CH=CH2
axit metanoic: HCOOH
glucozơ: CH2OH-(CHOH)4-CHO
Câu 6:
Để tráng gương ruột phích người ta thủy phân 68,4 gam saccarozơ với hiệu suất 80%, sau đó lấy sản phẩm tạo thành thực hiện phản ứng với AgNO3 dư trong NH3 dư đun nóng, đến phản ứng hoàn toàn thu được m gam Ag. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn B
Saccarozơ —> 2C6H12O6 —> 4Ag
0,2……………….…………..0,8
nAg thực tế = 0,8.80% = 0,64
=> mAg = 69,12
Câu 8:
 Xem đáp án
Xem đáp án
Câu 9:
Chất nào dưới đây khi tham gia phản ứng trùng hợp tạo thành tơ?
 Xem đáp án
Xem đáp án
Câu 10:
Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,.. Thành phần chính của khí thiên nhiên là
 Xem đáp án
Xem đáp án
Câu 11:
 Xem đáp án
Xem đáp án
Câu 12:
Hòa tan hoàn toàn 9,6 gam bột Cu vào dung dịch H2SO4 đặc nóng thu được V lít khí mùi hắc (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Câu 13:
Cho sơ đồ chuyển hóa (mỗi mũi tên là một phương trình phản ứng):
Chất tan trong các dung dịch X, Y, X lần lượt là
 Xem đáp án
Xem đáp án
Câu 14:
Kết quả thí nghiệm của các dung dịch X, Y, Z và T với thuốc thử được ghi ở bảng sau:
|
Chất Thuốc thử |
X |
Y |
Z |
T |
|
Dung dịch HCl |
+ |
- |
+ |
+ |
|
Dung dịch NaOH |
+ |
- |
+ |
- |
|
Dung dịch AgNO3/NH3 |
+ |
Có kết tủa |
- |
Có kết tủa |
Quy ước: (+) có phản ứng, (-) không có phản ứng. Các chất X, Y, Z và T lần lượt là:
 Xem đáp án
Xem đáp án
Câu 15:
Ba chất hữu cơ X, Y, Z có cùng công thức phân tử C3H6O2 có đặc điểm sau:
- X tác dụng được với Na và tham gia phản ứng tráng bạc
- Y được điều chế trực tiếp từ axit và ancol có cùng số nguyên tử hiđro
- Z tác dụng được với NaOH và tham giam phản ứng tráng bạc
Các chất X, Y, Z lần lượt là
 Xem đáp án
Xem đáp án
Chọn D
+ X tác dụng với Na và tham gia phản ứng tráng bạc
—> X là HOCH2CH2CHO.
+ Y được điều chế trực tiếp từ axit và ancol có cùng số nguyên tử H
—> Y là CH3COOCH3 (Từ axit CH3COOH và ancol CH3OH)
+ Z tác dụng với NaOH và tham gia phản ứng tráng bạc
—> Z là HCOOCH2CH3.
Câu 18:
 Xem đáp án
Xem đáp án
Câu 19:
 Xem đáp án
Xem đáp án
Câu 20:
Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng một lượng dư kim loại nào sau đây?
 Xem đáp án
Xem đáp án
Câu 21:
Dãy chất nào sau đây đều là chất điện li mạnh?
 Xem đáp án
Xem đáp án
Câu 22:
Tàu biển với lớp vỏ thép dễ bị ăn mòn bởi môi trường không khí và nước biển. Để bảo vệ các tàu thép ngoài việc sơn bảo vệ, người ta còn gắn vào vỏ tàu một số tấm kim loại. Tấm kim loại đó là
 Xem đáp án
Xem đáp án
Câu 23:
 Xem đáp án
Xem đáp án
Câu 24:
Cho các chất sau: KHCO3, FeS, Ag, Fe(NO3)2. Có bao nhiêu chất khi cho vào dung dịch H2SO4 loãng thì có khí thoát ra?
 Xem đáp án
Xem đáp án
Chọn C
Có 3 chất thoát khí khi cho vào dung dịch H2SO4 loãng: KHCO3, FeS, Fe(NO3)2
HCO3- + H+ —> CO2 + H2O
FeS + H+ —> Fe2+ + H2S
Câu 25:
Trong sơ đồ phản ứng sau:
(1) Xenlulozơ → glucozơ → X + CO2 (2) X + O2 H2O
Các chất X, Y lần lượt là
 Xem đáp án
Xem đáp án
Câu 26:
Hỗn hợp X gồm sắt và oxit sắt có khối lượng 5,92 gam. Cho khí CO dư đi qua hỗn hợp X đun nóng. Khí sinh ra sau phản ứng cho tác dụng với Ca(OH)2 dư được 9 gam kết tủa. Khối lượng sắt thu được là
 Xem đáp án
Xem đáp án
Chọn D
bị lấy = = 0,09 gam
—> = 5,92 – 0,09.16 = 4,48 gam
Câu 27:
Chất khí X có các tính chất sau:
a) Khi phản ứng với dung dịch Ca(OH)2 dư tạo ra kết tủa;
b) Gây hiệu ứng nhà kính làm biến đổi khí hậu;
c) Không có phản ứng cháy;
d) Không làm mất màu nước brom.
Chất X là
 Xem đáp án
Xem đáp án
Chọn C
A. H2O: Thỏa mãn (b)(c)(d)
B. CH4: Thỏa mãn (b)(d)
C. CO2: Thỏa mãn tất cả
D. SO2: Thỏa mãn (a)
Câu 28:
 Xem đáp án
Xem đáp án
Chọn A
X đơn chức nên = 0,25
Số C = = 3
Số H = = 9
—> X là C3H9N
Câu 29:
 Xem đáp án
Xem đáp án
Chọn D
Phát biểu D sai, X là Gly-Ala-Ala
Câu 30:
Cho chất hữu cơ X có công thức C7H18O2N2 và thực hiện các sơ đồ phản ứng sau:
(1) X + NaOH X1 + X2 + H2O
(2) X1 + 2HCl → X3 + NaCl
(3) X4 + HCl → X3
(4) X4 tơ nilon-6 + H2O
Phát biểu nào sau đây là đúng
 Xem đáp án
Xem đáp án
Chọn C
(4) —> X4 là NH2-(CH2)5-COOH
(3) —> X3 là NH3Cl-(CH2)5-COOH
(2) —> X1 là NH2-(CH2)5-COONa
(1) —> X là NH2-(CH2)5-COO-NH3CH3
—> X2 là CH3NH2
A. Sai: = 162 < = 167,5
B. Sai, X2 làm quỳ tím ẩm hóa xanh
C. Đúng
D. Sai, dạng muối sẽ có nhiệt độ nóng chảy cao hơn axit tương ứng.
Câu 31:
Cho Al vào dung dịch chứa Fe(NO3)3 và HCl, thu được hỗn hợp khí X gồm NO và H2, dung dịch Y và chất rắn Z. Cho dung dịch NaOH dư vào Y đun nhẹ, thu được kết tủa và có khí mùi khai. Thành phần chất tan trong Y là
 Xem đáp án
Xem đáp án
Chọn B
Khí X chứa H2 nên đã bị khử hết
Cho dung dịch NaOH dư vào Y đun nhẹ, thu được kết tủa và có khí mùi khai
—> Y chứa NH![]()
Chất rắn Z là Fe, có thể có Al dư —> Y không chứa Fe3+
—> Thành phần chất tan trong Y là AlCl3, NH4Cl, có thể có FeCl2.
Câu 32:
Cho các phát biểu sau:
(a) Ở người, nồng độ glucozơ trong máu được giữ ổn định ở mức 0,1%
(b) Dùng dung dịch nước brom có thể phân biệt được anilin và glixerol
(c) Tơ xenlulozơ axetat thuộc loại tơ nhân tạo
(d) Thủy phân este đơn chức trong môi trường kiềm luôn cho sản phẩm là muối và ancol
(e) Số nguyên tử N có trong phân tử đipeptit Ala-Lys là 2
(f) Protein là một loại thức ăn quan trọng với con người
(g) Trong một phân tử triolein có 3 liên kết π
(h) Vinyl xianua được sử dụng để sản xuất tơ olon
(k) Dung dịch glucozơ và saccarozơ đều có phản ứng tráng bạc
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B
(a) Đúng
(b) Đúng, anilin tạo kết tủa trắng, glyxerol không phản ứng
(c) Đúng
(d) Sai, có thể không thu được ancol mà thay vào đó là anđehit,
xeton hay một muối khác
(e) Sai, đipeptit này có 3N
(f) Đúng
(g) Sai, triolein có 6 liên kết pi (3C=C và 3C=O)
(h) Đúng
(k) Sai, glucozơ có tráng bạc, saccarozơ không tráng bạc.
Câu 33:
Cho X, Y, Z là 3 este đều đơn chức, mạch hở (trong đó Y và Z không no chứa một liên kết C=C và có tồn tại đồng phân hình học). Đốt cháy 21,62 gam hỗn hợp E chứa X, Y, Z sản phẩm cháy dẫn qua dung dịch Ca(OH)2 dư thấy khối lượng dung dịch giảm 34,5 gam. Mặt khác, đun nóng 21,62 gam E với 300ml dung dịch NaOH 1M (vừa đủ), thu được hỗn hợp T chỉ chứa 2 muối và hỗn hợp gồm 2 ancol kế tiếp thuộc cùng dãy đồng đẳng. Khối lượng của muối có khối lượng phân tử lớn hơn trong hỗn hợp T là
 Xem đáp án
Xem đáp án
Chọn A
Đặt a, b là số mol CO2, H2O
—> Δm = 44a + 18b – 100a = -34,5
= 12a + 2b + 0,6.16 = 21,62
—> a = 0,87 và b = 0,79
—> Số C = —> X là HCOOCH3
—> – 0,08 = 0,22
Vậy nếu đốt Y và Z thu được:
= 0,87 – 0,22.2 = 0,43
—> Số C trung bình của Y, Z = 0,43/0,08 = 5,375
Y, Z có đồng phân hình học nên Y là:
CH3-CH=CH-COOCH3
Do sản phẩm xà phòng hóa chỉ có 2 muối và 2 ancol kế tiếp nên Z là:
CH3-CH=CH-COOCH5
Vậy muối có M lớn nhất là CH3-CH=CH-COONa (0,08 mol)
—> m muối = 0,08.108 = 8,64
Câu 34:
Đốt cháy hoàn toàn 45 gam hỗn hợp X gồm ancol metylic, ancol anlylic, etylenglicol, glixerol, sobitol thu được 39,2 lít CO2 (đktc) và m gam H2O. Mặt khác, khi cho 45 gam hỗn hợp X phản ứng hoàn toàn với Na dư, thu được 13,44 lít H2 (đktc). Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C
gam
Câu 35:
Hợp chất hữu cơ E (chứa các nguyên tố C, H, O và tác dụng được với Na). Cho 44,8 gam E tác dụng với dung dịch NaOH vừa đủ thu được dung dịch F chỉ chứa hai chất hữu cơ X, Y. Cô cạn F thu được 39,2 gam chất X và 26 gam chất Y. Tiến hành hai thí nghiệm sau:
+ TN1: Đốt cháy 39,2 gam X thu được 13,44 lít CO2 (đktc); 10,8 gam H2O và 21,2 gam Na2CO3
+ TN2: Đốt cháy 26 gam Y thu được 29,12 lít CO2 (đktc); 12,6 gam H2O và 10,6 gam Na2CO3. Biết E, X và Y có công thức phân tử trùng với công thức đơn giản nhất và phản ứng xảy ra hoàn toàn
Số công thức cấu tạo của E thỏa mãn các tính chất trên là
 Xem đáp án
Xem đáp án
Chọn C
Đốt chất X:
= 0,4
—> C : H : O : Na = 2 : 3 : 3 : 1
—> X là C2H3O3Na: HO-CH2-COONa
Đốt chất Y:
—> C : H : O : Na = 7 : 7 : 1 : 1
—>
Vì E tác dụng NaOH tạo ra 2 muối X và Y
nên Y phải là muối của phenol.
Cấu tạo của Y là CH3-C6H4-ONa (o, m, p)
Từ cấu tạo của X, Y và nên E là
HO-CH2-COO-CH2-COO-C6H4-CH3 (o, m, p)
Câu 36:
Hòa tan hoàn toàn 14,58 gam Al trong dung dịch HNO3 loãng, đun nóng thì có 2,0 mol HNO3 đã phản ứng, đồng thời có V lít khí N2 thoát ra (đktc). Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn A
= 0,54
Đặt a, b là số mol N2 và
Bảo toàn electron —> 10a + 8b = 0,54.3
= 2 = 12a + 10b
—> a = 0,05 và b = 0,14
—> V = 1,12 lít
Câu 37:
Hỗn hợp rắn X gồm Mg, MgO, Fe3O4 và (trong đó oxi chiếm 21,951% khối lượng hỗn hợp). Dẫn 6,72 lít CO (đktc) đi qua ống sứ chứa 32,8 gam X, nung nóng. Sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hòa tan hết toàn bộ Y trong dung dịch HNO3 loãng, dư. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 122,7 gam muỗi và 4,48 lít (đktc) hỗn hợp khí gồm NO và N2O có tỉ khối so với He là 8,375. Số mol HNO3 tham gia phản ứng là
 Xem đáp án
Xem đáp án
Chọn C
X gồm kim loại (25,6 gam) và O (0,45 mol)
Z gồm CO2 (0,15) và CO dư (0,15)
—> Y gồm kim loại (25,6) và O (0,45 – 0,15 = 0,3)
Sản phẩm khử gồm NO (0,15), N2O (0,05) và (a)
—> nNO3- trong muối kim loại = = 8a + 1,45
—> m muối = 25,6 + 62(8a + 1,45) + 80a = 122,7
—> a = 0,0125
Câu 38:
Dẫn từ từ đến dư khí CO2 vào dung dịch chứa đồng thời NaOH và Ba(OH)2. Sự phụ thuộc của khối lượng kết tủa vào thể tích khí CO2 ở đktc được biểu diễn bằng đồ thị bên
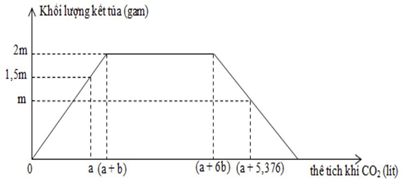
Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C
Đặt x = a/22,4; y = b/22,4 và z = m/197
Đoạn 1: CO2 + Ba(OH)2 —> BaCO3 + H2O
x = 1,5z (1)
x + y = 2z (2)
Đoạn 2:
CO2 + 2NaOH —> Na2CO3 + H2O
Na2CO3 + CO2 + H2O —> 2NaHCO3
Đoạn 3:
CO2 + H2O + BaCO3 —> Ba(HCO3)2
hòa tan BaCO3 = x + 0,24 – (x + 6y) = 0,24 – 6y
—> còn lại = z = 2z – (0,24 – 6y) (3)
(1)(2)(3) —> x = 0,09; y = 0,03; z = 0,06
—> m = 197z = 11,82
Câu 39:
Cho hỗn hợp E gồm 0,1 mol X (C5H9O4N) và 0,15 mol Y (C3H9O3N, là muối của axit vô cơ) tác dụng hoàn toàn với dung dịch KOH, đun nóng, thu được một ancol hai chức và một amin no (có cùng số nguyên tử cacbon) và dung dịch T. Cô cạn dung dịch T, thu được hỗn hợp G gồm ba muối khan (trong đó có một muối của α-amino axit). Phần trăm khối lượng của muối có phân tử khối lớn nhất trong G là
 Xem đáp án
Xem đáp án
Chọn D
Y là C2H5NH3HCO3
—> Amin và ancol là C2H5NH2 và C2H4(OH)2
G chứa 3 muối khan —> X là NH2-CH2-COO-CH2-CH2-OOC-H
—> Muối gồm HCOOK (0,1), GlyK (0,1) và K2CO3 (0,15)
—> %K2CO3 = 51,24%
Câu 40:
Điện phân 1 lít dung dịch X gồm Cu(NO3)2 0,6M và FeCl3 0,4M đến khi anot thoát ra 17,92 lít khí (đktc) thì dừng lại. Lấy catot ra khỏi bình điện phân, khuấy đều dung dịch để phản ứng xảy ra hoàn toàn thì thu được dung dịch Y. Giả thuyết kim loại sinh ra đều bám lên catot, sản phẩm khử của N+5 (nếu có) là NO duy nhất. Giá trị (mX – mY) gần nhất với giá trị nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D
và
Bảo toàn Cl —> = 0,6
Anot thoát ra 0,8 mol khí —> = 0,2
Tại thời điểm bên catot hết Cu2+ thì bên anot đã có O2 từ trước đó,
khi đó H+, thực chất coi như sẽ bị điện phân tiếp.
Bảo toàn electron —> = 0,2 mol
Dung dịch sau điện phân chứa Fe2+ (0,4), (1,2) —> H+ (0,4)
Khuấy đều —> / 4 = 0,1
