Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (30 đề)
Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (Đề 15)
-
6201 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
 Xem đáp án
Xem đáp án
Chọn B.
Các tên gọi không đúng là:
(3) CH2=C(CH3)-COOCH3: metyl metacrylic (gọi đúng là metyl metacrylat)
(5) CH3COOC6H5: benzyl axetat (gọi đúng là phenyl axetat)
Câu 2:
 Xem đáp án
Xem đáp án
Câu 4:
 Xem đáp án
Xem đáp án
Câu 6:
 Xem đáp án
Xem đáp án
Câu 7:
Ứng với công thức phân tử C4H10O2, có bao nhiêu đồng phân bền có thể hoà tan được Cu(OH)2?
 Xem đáp án
Xem đáp án
Chọn D.
Ứng với công thức phân tử C4H10O2,
có 3 đồng phân bền có thể hoà tan được Cu(OH)2:
CH3-CH2-CHOH-CH2OH
CH3-CHOH-CHOH-CH3
CH3-C(CH3(OH)-CH2OH
Câu 8:
 Xem đáp án
Xem đáp án
Câu 10:
Cho các chất sau: CO, Na2CO3, C2H6O, C2H5Cl. Những chất thuộc hợp chất hữu cơ là
 Xem đáp án
Xem đáp án
Câu 11:
Hãy dự đoán hiện tượng khi thêm từ từ dung dịch NaOH loãng vào dung dịch muối FeCl2 là:
 Xem đáp án
Xem đáp án
Câu 12:
 Xem đáp án
Xem đáp án
Câu 13:
Có thể dùng hóa chất nào dưới đây để làm mềm nước cứng vĩnh cửu?
 Xem đáp án
Xem đáp án
Câu 14:
 Xem đáp án
Xem đáp án
Chọn A.
là Mg, muối là
Câu 15:
Để loại bỏ axetilen có lẫn trong etilen, người ta cho hỗn hợp khí này đi qua dung dịch chứa dư chất nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D.
Để loại bỏ axetilen có lẫn trong etilen, người ta
cho hỗn hợp khí này đi qua dung dịch chứa dư:
Khí thoát ra là C2H4.
Câu 16:
 Xem đáp án
Xem đáp án
Chọn D.
n không khí
Câu 17:
 Xem đáp án
Xem đáp án
Câu 18:
Kim loại M phản ứng được với dung dịch HCI, dung dịch Cu(NO3)2, dung dịch HNO3 (đặc, nguội). Kim
loại M là
 Xem đáp án
Xem đáp án
Câu 19:
Hỗn hợp X gồm metan và anken, cho 5,6 lít X qua dung dịch brom dư thấy khối lượng bình brom tăng 7,28 gam và có 2,688 lít khí bay ra (các khí đều đo ở đktc). CTPT của anken là:
 Xem đáp án
Xem đáp án
Chọn B.
m tang = 7,28
Câu 20:
Thủy phân este X có công thức C4H8O2 thu được muối natri propionat. Tên gọi X là
 Xem đáp án
Xem đáp án
Câu 23:
X là chất rắn, ở dạng bột vô định hình, màu trắng, không tan trong nước lạnh, Y là loại đường phổ biến nhất, có trong nhiều loài thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt. Tên gọi của X và Y lần lượt là
 Xem đáp án
Xem đáp án
Chọn C.
X và Y là hai cacbohiđrat.
X là chất rắn, ở dạng bột vô định hình,
màu trắng, không tan trong nước lạnh X là tinh bột.
Y là loại đường phổ biến nhất, có trong nhiều loài thực vật,Câu 24:
Cho m gam hỗn hợp X gồm Na và Al vào nước dư thu được 8,96 lít H2 (đktc). Nếu cho m gam hỗn hợp tác dụng với dung dịch NaOH dư thu được 12,32 lít H2 (đktc). Phần trăm khối lượng Al trong X là
 Xem đáp án
Xem đáp án
Chọn D.
Ban đầu: và
Với : Al dư , phản ứng
Với NaOH dư, cả Al và Na đều hết.
Câu 25:
Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3.
(b) Nung FeS2 trong không khí.
(c) Nhiệt phân KNO3.
(d) Cho dung dịch CuSO4 vào dung dịch NH3 (dư).
(e) Cho Fe vào dung dịch CuSO4.
(f) Cho Zn vào dung dịch FeCl3 (dư).
(h) Nung Ag2S trong không khí.
(i) Cho Ba vào dung dịch CuSO4 (dư).
Số thí nghiệm thu được kim loại sau khi các phản ứng kết thúc là
 Xem đáp án
Xem đáp án
Chọn B.
(a)
(b)
(c)
(d) dư
(e)
(g) dư
(h)
(i)
Câu 26:
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là
 Xem đáp án
Xem đáp án
Chọn B.
Đặt và
n khí
m khí
và
Kim loại M hóa trị x, bảo toàn electron:
là Mg.
Câu 27:
Cho mô hình thí nghiệm dùng để điều chế SO2 trong phòng thí nghiệm như hình vẽ. Hỏi X và Y là chất gì?
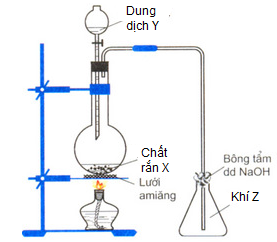
 Xem đáp án
Xem đáp án
Chọn A.
Điều chế trong phòng thí nghiệm:
là Na2SO3 và Y là dung dịch H2SO4 đặc.
Câu 28:
 Xem đáp án
Xem đáp án
Chọn A.
Tự chọn V = 1 lít
A.
B.
C.
D.
Câu 29:
Nhận xét nào dưới đây là đúng?
 Xem đáp án
Xem đáp án
Câu 30:
Nhiệt độ nóng chảy, nhiệt độ sôi và độ tan trong nước của ba chất hữu cơ X, Y, Z được trình bày trong bảng sau:
|
|
Nhiệt độ sôi 181,7 |
Nhiệt độ nóng chảy 43 |
Độ tan trong nước (g/ 100mL) |
|
|
20oC |
80oC |
|||
|
X |
181,7 |
43 |
8,3 |
|
|
Y |
Phân hủy trước khi sôi |
248 |
23 |
60 |
|
Z |
78,73 |
-114 |
|
|
X, Y, Z tương ứng là chất nào sau đây:
 Xem đáp án
Xem đáp án
Câu 31:
 Xem đáp án
Xem đáp án
Chọn B.
Dung dịch sau phản ứng chứa
bảo toàn điện tích
Chất rắn gồm dư
rắn = 36,1 gam.
Câu 32:
Hỗn hợp X gồm 1 mol aminoaxit no, mạch hở và 1 mol amin no, mạch hở. X có khả năng phản ứng tối đa với 3 mol HCl hoặc 2 mol NaOH. Đốt cháy hoàn toàn X thu được 8 mol CO2, x mol H2O và y mol N2. Tổng x + y bằng:
 Xem đáp án
Xem đáp án
Chọn D.
có
có
Các chất đều no, mạch hở nên X có
Công thức chung của X là
Và
Câu 33:
Cho các phát biểu sau:
(a) Khi ngâm trong nước xà phòng có tính kiềm, vải lụa làm bằng tơ tằm sẽ nhanh hỏng.
(b) Thủy phân hoàn toàn anbumin của lòng trắng trứng trong môi trường kiêm thu được ![]() aminoaxit.
aminoaxit.
(c) Xenlulozơ trinitrat được dùng làm thuốc súng không khói.
(d) Đốt cháy hoàn toàn este no, đơn chức, mạch hở, thu được CO2 và H2O có số mol bằng nhau.
(e) Ứng với công thức C4H8O2 có 3 đồng phân este có khả năng tham gia phản ứng tráng gương.
Số phát biểu đúng là:
 Xem đáp án
Xem đáp án
Chọn C.
(a) Đúng, do CONH dễ bị thủy phân
(b) Sai, thu được muối của a-amino axit
(c) Đúng
(d) Đúng
(e) Sai, chỉ cô 2 đồng phân este tráng gương.
Câu 34:
 Xem đáp án
Xem đáp án
Chọn C.
và
là este của ancol (x mol) và Y là este của phenol (y mol)
và
và
Bảo toàn
Số
X là có n nguyên tử C.
là
Muối gồm và
m rắn = 4,56
Câu 35:
 Xem đáp án
Xem đáp án
Chọn A.
X tạo 2 este với CH3OH nên X là
Z là
Q là
và
Câu 36:
Đốt cháy hoàn toàn m gam triglixerit X cần vừa đủ 3,08 mol O2, thu được CO2 và 2 mol H2O. Cho m gam X tác dụng với dung dịch NaOH vừa đủ, thu được glixerol và 35,36 gam muối. Mặt khác, m gam X tác dụng tối đa với a mol Br2 trong dung dịch. Giá trị của a là:
 Xem đáp án
Xem đáp án
Chọn C.
Đặt và
Bảo toàn O:
và
Bảo toàn khối lượng:
và y = 2,2
X có độ không no là k.
Câu 37:
Hoà tan m1 gam FeCO3 vào dung dịch HCl 80%. Sau phản ứng hoàn toàn thu dung dịch Y, trong Y nồng độ phần trăm của HCI là 37,1%. Cho vào dung dịch Y m2 gam BaCO3, sau phản ứng hoàn toàn thu được dung dịch Z có nồng độ của HCI là 19,7%. Nồng độ phần trăm của muối trong dung dịch Y và 1 muối trong dung dịch Z lần lượt là:
 Xem đáp án
Xem đáp án
Chọn A.
Tự chọn
dư ban đầu
dư
(Chọn A)
Nếu tính tiếp: Đặt
còn lại
dư
(Chú ý: Bài có nhiều lần làm tròn kết quả trung gian nên kết quả cuối cùng bị lệch).
Câu 38:
Cho hỗn hợp X gồm 2 este đơn chức (hơn kém nhau 1 nguyên tử C trong phân tử). Đem đốt cháy m gam X cần vừa đủ 0,46 mol O2. Thủy phân m gam X trong 70 ml dung dịch NaOH 1M (vừa đủ) thì thu được 7,06 gam hỗn hợp muối Y và một ancol Z no, đơn chức, mạch hở. Đem đốt hoàn toàn hỗn hợp muối Y thì cần 5,6 lít (đktc) khí O2. Phần trăm khối lượng của este có phân tử khối lớn hơn trong X là?
 Xem đáp án
Xem đáp án
Chọn B.
đốt X = 0,46
đốt Y = 0,25
đốt Z
Z no, đơn chức, mạch hở nên
Nếu X mạch hở thì là
Bảo toàn khối lượng
Đặt a, b là số mol CO2 và H2O.
Và
và
Số và
Các muối gồm và
là nghiệm duy nhất.
X gồm:
Câu 39:
Cho 360 ml dung dịch KOH 1M hay 420 mi dung dịch KOH 1M vào 250 ml dung dịch AICl3 x mol/l đều thu được cùng lượng kết tủa. Giá trị x là
 Xem đáp án
Xem đáp án
Chọn A.
Khi hay 0,42 đều thu được cùng lượng kết tủa
nên khi thì kết tủa chưa max và khi
thì kết tủa đã bị hòa tan một phần.
và
Câu 40:
Đun nóng 45,54 gam hỗn hợp E gồm hexapeptit X và tetrapeptit Y cần dùng 580 ml dung dịch NaOH 1M chỉ thu được dung dịch chứa muối natri của glyxin và valin. Mặt khác đốt cháy cùng lượng E trên trong O2 vừa đủ thu được hỗn hợp CO2, H2O và N2; trong đó tổng khối lượng của CO2 và H2O là 115,18 gam. Công thức phân tử của peptit X là
 Xem đáp án
Xem đáp án
Chọn B.
Quy đổi E thành:
mol
mol
mol
Đặt x, y là số mol của X và Y
Đặt u, v là số mol Gly và Val
và
X là
Y là
Với và
là
