Đề thi thử THPT Quốc gia môn Hóa năm 2022 chọn lọc, có lời giải (30 đề)
Đề thi thử THPT Quốc gia môn Hóa 2022 chọn lọc, có lời giải (Đề 11)
-
6031 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 2:
Axit fomic có trong nọc kiến. Khi bị kiến cắn, nên chọn chất nào sau đây bôi vào vết thương để giảm sưng tấy?
 Xem đáp án
Xem đáp án
Câu 3:
 Xem đáp án
Xem đáp án
Câu 4:
Hai chất hữu cơ X và Y là đồng phân của nhau có công thức phân tử C9H8O2. Thủy phân hoàn toàn hỗn hợp X, Y bằng dung dịch NaOH vừa đủ, thu được sản phẩm hữu cơ gồm 3 muối và một hợp chất hữu cơ Z (MZ < 120). Phân tử khối của Z là
 Xem đáp án
Xem đáp án
Chọn A.
muối + chất hữu cơ Z
nên trong X< Y có 1 este của phenol.
Chọn cặp
và
Các muối gồm
Z làCâu 5:
 Xem đáp án
Xem đáp án
Câu 6:
 Xem đáp án
Xem đáp án
Chọn C.
X là trong X có đoạn mạch
nên X có các cấu tạo:
Gly-Ala-Val-Gly-Ala
Gly-Ala-Val-Ala-Gly
Gly-Gly-Ala-Val-Ala
Ala-Gly-Ala-Val-Gly
Gly-Ala-Gly-Ala-Val
Ala-Gly-Gly-Ala-Val
Câu 7:
Trước những năm 50 của thế kỷ XX, công nghiệp hữu cơ dựa trên nguyên liệu chính là axetilen. Ngày nay, nhờ sự phát triển vượt bậc của công nghiệp khai thác và chế biến dầu mỏ, etilen trở thành nguyên liệu rẻ tiền và tiện lợi hơn so với axetilen. Công thức phân tử của etilen là
 Xem đáp án
Xem đáp án
Câu 8:
 Xem đáp án
Xem đáp án
Câu 9:
Đốt cháy đơn chất X trong không khí thu được khí Y. Khi đun nóng X với H2, thu được khí Z. Khi cho Y tác dụng với Z thu được chất rắn màu vàng. Đơn chất X là
 Xem đáp án
Xem đáp án
Câu 10:
Cho 15,6 gam hỗn hợp X gồm Al và Al2O3 tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí H2 (đktc). Khối lượng của Al2O3 trong X là
 Xem đáp án
Xem đáp án
Chọn B.
gam
Câu 11:
Oxit nhôm (Al2O3) không có tính chất hay ứng dụng nào sau đây?
 Xem đáp án
Xem đáp án
Câu 12:
Các vật liệu chứa nhiều xenlulozơ như tre, gỗ, nứa ... thường được dùng làm vật liệu xây dựng, đồ dùng gia đình. Ngoài ra, xenlulozơ nguyên chất và gần nguyên chất được chế thành sợi, tơ, giấy viết, giấy làm bao bì. Xenlulozơ có cấu trúc mạch không phân nhánh, do các mắt xích –C6H10O5– liên kết với nhau tạo nên. Mỗi mắt xích –C6H10O5– có 3 nhóm OH tự do nên công thức cấu tạo của xenlulozơ là
 Xem đáp án
Xem đáp án
Câu 13:
Kim loại có nhiệt độ nóng chảy cao nhất, dùng làm dây tóc bóng đèn là:
 Xem đáp án
Xem đáp án
Câu 14:
 Xem đáp án
Xem đáp án
Chọn A.
là
gam
Câu 15:
Cho 12,8 gam bột Cu vào 200 ml dung dịch Fe2(SO4)3 0,6M. Sau khi kết thúc phản ứng, thu được dung dịch X và m gam kim loại. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn C.
dư
dư = 5,12
Câu 16:
 Xem đáp án
Xem đáp án
Chọn D.
X tác dụng được với Na, NaOH
và phải là axit axetic
Câu 17:
Cho 36 gam FeO phản ứng vừa đủ với dung dịch chứa a mol HCl. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn D.
Câu 18:
Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác theo hình vẽ bên.
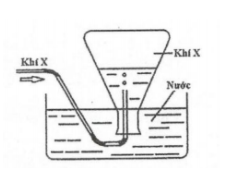
Khí X được tạo ra từ phản ứng hóa học nào sau đây?
 Xem đáp án
Xem đáp án
Chọn D.
Khí X thu bằng phương pháp đẩy nên khí X không tan (hoặc ít tan)
trong và không phản ứng với .
NH3 tan rất tốt, và tan tốt nên phản ứng D là phù hợp.
Câu 19:
Điều khẳng định nào sau đây là sai?
 Xem đáp án
Xem đáp án
Câu 20:
Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
 Xem đáp án
Xem đáp án
Chọn đáp án D. thạch cao sống.
Câu 21:
Đun 12 gam axit axetic với 13,8 gam etanol (có H2SO4 đặc làm xúc tác) đến khi phản ứng đạt tới trạng thái cân bằng, thu được 11 gam este. Hiệu suất của phản ứng este hoá là
 Xem đáp án
Xem đáp án
Chọn C.
Câu 22:
Lấy 16,32 gam phenyl axetat tác dụng với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được m gam muối. Giá trị m là.
 Xem đáp án
Xem đáp án
Chọn B.
Muối gồm và
m muối = 23,76
Câu 23:
Thủy phân este X mạch hở (có công thức phân tử C7H10O4) thu được hai ancol no Y, Z (MY < MZ) và axit cacboxylic T. Cho các phát biểu sau:
(a) Có ba este thỏa mãn tính chất của X.
(b) Nhiệt độ sôi của Z thấp hơn H2O.
(c) Chất Y tan vô hạn trong nước.
(d) Hai chất Y, Z đều thuộc dãy đồng đẳng của ancol etylic.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn C.
X là:
Y là là là
(a) Đúng
(b) Đúng
(c) Đúng
(d) Đúng
Câu 24:
Công thức nào sau đây có thể là công thức của chất béo?
 Xem đáp án
Xem đáp án
Câu 25:
Cho các sơ đồ phản ứng theo đúng tỉ lệ mol:
(a) X + 2NaOH → X1 + X2 + H2O (đun nóng)
(b) X1 + H2SO4 → X3 + Na2SO4
(c) nX3 + nX4 → Poli(etilen terephtalat) + 2nH2O (đun nóng, xúc tác)
(d) X3 + 2X2 ↔ X5 + 2H2O (đun nóng, H2SO4 đặc xúc tác)
Cho biết: X là hợp chất hữu cơ có công thức phân tử C9H8O4; X1, X2, X3, X4, X5 là các hợp chất hữu cơ khác nhau. Phân tử khối của X5 là:
 Xem đáp án
Xem đáp án
Chọn A.
là là là
(a) có nên X chứa chức axit
là
Và là
là
Câu 26:
Cho hỗn hợp chứa 5,76 gam Mg và 7,56 gam MgCO3 vào dung dịch HNO3 loãng dư, kết thúc phản ứng thu được dung dịch X (không chứa muối NH4NO3) và V lít (đktc) hỗn hợp khí Y có tỉ khối so với He bằng 11. Giá trị của V là
 Xem đáp án
Xem đáp án
Chọn D.
gồm và
Bảo toàn electron
lít
Câu 27:
Hòa tan hết 11,24 gam hỗn hợp gồm Mg, Al, Mg(NO3)2 trong dung dịch chứa x mol HNO3, kết thúc phản ứng, thu được dung dịch X chỉ chứa các muối trung hòa có khối lượng 62,0 gam và hỗn hợp khí Y gồm N2O và N2 (tỉ lệ mol 1 : 1). Cho dung dịch NaOH dư vào X, thu được 13,34 gam kết tủa. Nếu đem cô cạn dung dịch X, lấy phần rắn đem nung đến khối lượng không đổi, thu được 46,68 gam hỗn hợp khí và hơi. Cho các phát biểu sau về bài toán
(1) Thể tích hỗn hợp khí Y ở đktc là 1,344 lít.
(2) Giá trị của x là 0,96.
(3) Phần trăm khối lượng Al trong hỗn hợp ban đầu là 28,826%.
(4) Số mol ion NO![]() trong dung dịch X là 0,82.
trong dung dịch X là 0,82.
(5) Số mol NaOH phản ứng tối đa với dung dịch X là 0,85.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn D.
X chứa và
Bảo toàn điện tích:
m muối
Cô cạn X rồi nung chất rắn thu được
khí và hơi (tổng 46,68). Bảo toàn khối lượng:
m muối
Bảo toàn electron:
phản ứng
(1) Đúng,
(2) Đúng
(3) Đúng
(4) Sai,
(5) Sai,
Câu 28:
Cho 200 gam dung dịch glucozơ a% vào dung dịch AgNO3 trong NH3 đun nóng (dùng dư), thu được 25,92 gam Ag. Giá trị của a là
 Xem đáp án
Xem đáp án
Chọn C.
Câu 29:
Xà phòng hóa hoàn toàn 17,8 gam chất béo X cần vừa đủ dung dịch chứa 0,06 mol NaOH. Cô cạn dung dịch sau phản ứng, thu được m gam muối khan. Giá trị của m là
 Xem đáp án
Xem đáp án
Chọn D.
Bảo toàn khối lượng:
m chất béo m xà phòng
m xà phòng = 18,36
Câu 30:
Cho dãy các chất: (a) NH3, (b) CH3NH2, (c) C6H5NH2 (anilin). Thứ tự tăng dần lực bazơ của các chất trong dãy là?
 Xem đáp án
Xem đáp án
Chọn D.
có gốc thơm nên tính bazơ yếu nhất,
có gốc no nên tính bazơ mạnh nhất.
Câu 31:
Cho m gam hỗn hợp gồm glyxin và alanin tác dụng vừa đủ với 250 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được 26,35 gam muối khan. Giá trị của m là:
 Xem đáp án
Xem đáp án
Chọn C.
m muối
Câu 32:
Kim loại X được sử dụng trong nhiệt kế, áp kế và một số thiết bị khác. Ở điều kiện thường, X là chất lỏng. Kim loại X là
 Xem đáp án
Xem đáp án
Câu 33:
Cho 2,13 gam P2O5 vào dung dịch chứa x mol NaOH và 0,02 mol Na3PO4. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 6,88 gam hai chất tan. Giá trị của x là:
 Xem đáp án
Xem đáp án
Chọn A.
Bảo toàn
Nếu sản phẩm là
Nếu sản phẩm là
Nếu sản phẩm là
Dễ thấy Sản phẩm là và
và
Bảo toàn
Câu 34:
Thực hiện các thí nghiệm sau:
(a) Cho kim loại Cu vào dung dịch Fe2(SO4)3 (dư).
(b) Hấp thụ hết 0,15 mol CO3 vào dung dịch chứa 0,2 mol NaOH.
(c) Cho Fe3O4 vào dung dịch H2SO4 đặc, nóng (dư).
(d) Cho a mol Fe vào dung dịch HNO3, thu được 0,8a mol khí NO là sản phẩm khử duy nhất.
(e) Cho dung dịch NaHCO3 (dư) vào dung dịch Ba(OH)2.
(f) Cho K2Cr2O7 tác dụng với dung dịch HCl đặc dư, đun nhẹ.
(g) Cho phèn chua tác dụng với dung dịch Ba(OH)2 dư.
(h) Cho a mol Na2O vào dung dịch chứa a mol CuSO4.
(i) Cho 1 mol ClH3NCH2COOH tác dụng với 2 mol NaOH trong dung dịch.
(k) Nhỏ từ từ từng giọt dung dịch chứa a mol HCl vào dung dịch chứa a mol Na2CO3.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch có chứa hai muối là
 Xem đáp án
Xem đáp án
Chọn D.
(a) (Có dư)
(b) Tạo
(c)
(d) Tạo và
(e) (Có dư)
(f)
(g) Chứa 2 muối và kiềm dư
(h)
(i)
(k)
Câu 35:
Tiến hành thí nghiệm phản ứng tráng gương của glucozơ theo các bước sau đây:
Bước 1: Cho 1 ml dung dịch AgNO3 1% vào ống nghiệm sạch.
Bước 2: Nhỏ từng giọt dung dịch NH3 5% đến dư vào ống nghiệm và lắc đều đến khi thu được hiện tượng không đổi.
Bước 3: Thêm 1 ml dung dịch glucozơ vào ống nghiệm.
Bước 4: Lắc đều ống nghiệm, đun c|ch thủy (trong cốc nước nóng) vài phút ở 60 – 70oC.
Cho các phát biểu sau:
(a) Sau bước 4 quan sát thấy thành ống nghiệm sáng bóng như gương.
(b) Ở bước 2 quan sát được hiện tượng xuất hiện kết tủa rồi lại tan hết thành dung dịch trong suốt.
(c) Có thể thay glucozơ bằng saccarozơ thì các hiện tượng không đổi.
(d) Sản phẩm hữu cơ thu được trong dung dịch sau bước 4 có công thức phân tử là C6H15NO7.
(e) Ở bước 4 xảy ra phản ứng oxi hóa – khử trong đó glucozơ là chất bị khử.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B.
(a) Đúng
(b) Đúng
(c) Sai, saccarozơ không tráng gương
(d) Đúng, sản phẩm là hay
(e) Đúng, glucozơ là chất khử Ag+ thành Ag.
Câu 36:
Phát biểu đúng là:
 Xem đáp án
Xem đáp án
Câu 37:
Điện phân dung dịch chứa đồng thời NaCl và CuSO4 (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan các khí trong nước và sự bay hơi nước) với cường độ dòng điện không đổi. Kết quả của thí nghiệm cho ở bảng sau:
|
Thời gian điện phân (giây) |
Khối lượng catot tăng (gam) |
Khí thoát ra ở anot |
Dung dịch thu được sau điện phân có khối lượng giảm so với khối lượng dung dịch ban đầu (gam) |
|
965 |
m |
Một khí duy nhất |
2,70 |
|
3860 |
4m |
Hỗn hợp khí |
9,15 |
|
t |
5m |
Hỗn hợp khí |
11,11 |
Giá trị của t là
 Xem đáp án
Xem đáp án
Chọn B.
Trong 1930 giây:
m giảm
trong 1930s
Trong 7720 giây: và
m giảm
Bảo toàn electron
và
Trong t giây: và
m giảm
Bảo toàn electron
trong t giây
Câu 38:
 Xem đáp án
Xem đáp án
Chọn C.
X là
gồm và KOH dư (0,15)
Câu 39:
Hòa tan 27,32 gam hỗn hợp E gồm hai muối M2CO3 và MHCO3 vào nước, thu được dung dịch X. Chia X thành hai phần bằng nhau.
- Cho phần một tác dụng hoàn toàn với dung dịch Ba(OH)2 dư, thu được 31,52 gam kết tủa.
- Cho phần hai tác dụng hoàn toàn với dung dịch BaCl2 dư, thu được 11,82 gam kết tủa.
Phát biểu nào dưới đây đúng? Xem đáp án
Xem đáp án
Chọn A.
Đặt u, v là số mol và trong mỗi phần.
Phần 1:
Phần 2:
m mỗi phần
A. Sai:
B. Đúng, tạo
C. Sai
D. Sai,
Câu 40:
Hợp chất hữu cơ M mạch hở, không phân nhánh, có công thức phân tử là C11H16O8. Cho 0,05 mol M tác dụng vừa đủ với 0,2 mol NaOH thu được 0,1 mol muối X, 0,05 mol muối Y và 0,1 mol chất hữu cơ Z tác dụng được với Cu(OH)2 ở điều kiện thường tạo dung dịch màu xanh lam. Biết X, Z có cùng số nguyên tử cacbon. X và Y phản ứng với NaOH dư trong CaO khan, nung nóng đều thu được cùng một chất khí T. Cho các phát biểu sau:
(a) M là hợp chất hữu cơ tạp chức.
(b) Tổng khối lượng muối X và Y thu được là 16,5 gam.
(c) Khí T là thành phần chính của khí thiên nhiên.
(d) X và M đều tham gia phản ứng tráng bạc.
(e) Axit hóa các muối X và Y đều thu được axit có cùng số nguyên tử H.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Chọn B.
G có đều nằm trong 4COO nên các gốc hiđrocacbon đều no.
Do X, Z cùng C và ít nhất 2C nên X, Z đều có 2C và Y có 3C
Vôi tôi xút X, Y thu cùng sản phẩm T nên X đơn chức, Y hai chức
G là
X là là là
Z là
(1) Sai, G đa chức
(2) Đúng: và m muối = 31,2
(3) Đúng
(4) Sai
(5) Đúng, thu được và
