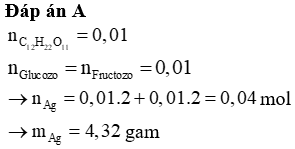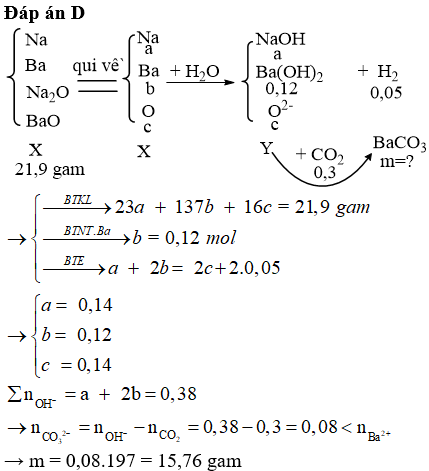30 đề thi THPT Quốc gia môn Hóa năm 2022 có lời giải (Đề số 8)
-
45507 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 3:
Xenlulozơ là cacbohidrat thuộc nhóm
 Xem đáp án
Xem đáp án
Đáp án B
Monosaccarit gồm glucozơ và fructozơ
Đisaccarit gồm saccarozơ (mantozơ đã giảm tải)
Polisacarit gồm tinh bột và xenlulozơ
Câu 7:
X là kim loại có nhiệt độ nóng chảy cao nhất, được sử dụng để làm sợi tóc bóng đèn thay thế cho sợi than, sợi osimi. X là kim loại nào dưới đây?
 Xem đáp án
Xem đáp án
Đáp án A
W là kim loại có nhiệt độ nóng chảy cao nhất, được sử dụng để làm sợi tóc bóng đèn thay thế cho sợi than, sợi osimi.
Câu 8:
Trong các ion sau: Zn2+, Cu2+, Fe2+, Fe3+, ion có tính oxi hóa yếu nhất là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 12:
Kim loại nào sau đây tan hết trong nước dư ở nhiệt độ thường tạo ra dung dịch?
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 14:
Khi để vôi sống trong không khí ẩm một thời gian sẽ có hiện tượng một phần bị chuyển hóa trở lại thành đá vôi. Khí nào sau đây là tác nhân gây ra hiện tượng trên?
 Xem đáp án
Xem đáp án
Đáp án D
Vì trong không khí có chứa cacbon đioxit (CO2) → sẽ phản ứng chậm với vôi sống (CaO) tạo đá vôi:
CO2 + CaO → CaCO3.
Câu 15:
Khi điện phân Al2O3 nóng chảy (điện cực trơ bằng than chì), khí nào sau đây không sinh ra ở điện cực anot?
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 17:
Crom tác dụng với lưu huỳnh đun nóng, thu được sản phẩm trong đó crom có số oxi hóa là
 Xem đáp án
Xem đáp án
Đáp án A
2Cr + 3S → Cr2S3. (số oxi hóa của crom là +3)
Câu 18:
Một trong những nguyên nhân gây tử vong trong nhiều vụ cháy là do nhiễm độc khí X. Khi vào cơ thể, khí X kết hợp với hemoglobin, làm giảm khả năng vận chuyển oxi của máu. Khí X là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 21:
Cho các este sau: etyl axetat, propyl fomat, metyl propionat, metyl metacrylat. Có bao nhiêu este có phản ứng tráng bạc?
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 23:
Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều trong quả nho chín nên còn gọi là đường nho. Khử chất X bằng H2 thu được chất hữu cơ Y. Tên gọi của X và Y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 24:
Đốt cháy hoàn toàn 0,2 mol amin no X bằng O2, thu được N2, 0,4 mol CO2 và 0,8 mol H2O. Cho 0,2 mol X tác dụng hết với dung dịch HCl dư, số mol HCl đã phản ứng là
 Xem đáp án
Xem đáp án
Đáp án B
Đốt cháy amin no:
=> = 0,2 mol
=> nHCl = 2 = 0,4 mol
Câu 25:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án B
A sai vì thủy phân nilon-6 thu được H2N[CH2]5COOH, còn thủy phân nilon-6,6 thu được H2N-[CH2]2-NH2 và HOOC-[CH2]2-COOH.
B đúng vì tở tằm là protein có liên kết –CONH- không bền trong môi trường axit hoặc bazơ
C sai trùng hợp buta-1,3-ddien cần xúc tác Na, to, tạo cao su buna.
D sai vì polietilen được tạo thành từ phản ứng trùng hợp etilen.
Câu 26:
Cho 11,7 gam hỗn hợp Cr và Zn phản ứng hoàn toàn với dung dịch HCl dư, đun nóng, thu được dung dịch X và 4,48 lít khí H2 (đktc). Khối lượng muối trong X là
 Xem đáp án
Xem đáp án
Đáp án D
mMuoi
= mKL + mCl
= 11,7 + 35,5*nCl-
= 11,7 + 35,5*2nH2
= 11,7 + 35,5*2*0,2 = 25,9 gam.
Câu 27:
Cho 5,4 gam Al phản ứng hoàn toàn với khí oxi dư, thu được m gam oxit. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
BTNT (Al): = 0,1 = 10,2 gam.
Câu 28:
Trường hợp nào sau đây tạo hai muối của sắt?
 Xem đáp án
Xem đáp án
Đáp án D
Các phản ứng hóa học xảy ra:
FeO + 2HCl → FeCl2 + H2O.
Fe(OH)3 + 3HCl → FeCl3 + 3H2O.
Fe2O3 + 6HCl → 2FeCl3 + 3H2O.
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O.
Câu 29:
Cho các chất: Fe, FeCl3, Fe2O3, Fe(NO3)3. Số chất vừa có tính oxi hóa, vừa có tính khử là
 Xem đáp án
Xem đáp án
Đáp án C
Fe, FeCl3, Fe(NO3)3 vừa có tính oxi hóa, vừa có tính khử.
Câu 31:
Hỗn hợp X gồm ba chất béo đều được tạo bởi glyxerol và hai axit oleic và stearic. Đốt cháy hoàn toàn 0,15 mol X cần dùng 12,075 mol O2, thu được CO2 và H2O. Xà phòng hóa 132,9 gam X trên với dung dịch KOH vừa đủ, thu được m gam muối. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A
Ta thấy chất béo tạo từ 2 gốc axit
BTNT C:
BTNT O:
BTKL trong X:
Ta có:
Câu 32:
Tiến hành thí nghiệm điều chế etyl axetat theo các bước sau đây:
Bước 1: Cho 1 ml C2H5OH, 1 ml CH3COOH và vài giọt dung dịch H2SO4 đặc vào ống nghiệm.
Bước 2: Lắc đều ống nghiệm, đun cách thủy (trong nồi nước nóng) khoảng 5 - 6 phút ở 65 - 70oC.
Bước 3: Làm lạnh, sau đó rót 2 ml dung dịch NaCl bão hòa vào ống nghiệm.
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án B
Mục đích chính của việc thêm dung dịch NaCl bão hòa là để este tách ra khỏi dung dịch.
Câu 33:
Cho các phát biểu sau:
(a) Mỡ động vật hoặc dầu dừa có thể dùng làm nguyên liệu để sản xuất xà phòng.
(b) Thủy phân hoàn toàn tinh bột và xenlulozơ đều thu được glucozơ.
(c) Khi ngâm trong nước xà phòng có tính kiềm, vải lụa làm bằng tơ tằm sẽ nhanh hỏng.
(d) Giấm ăn có thể dùng để khử mùi tanh của cá.
(e) Aminoaxit là tinh thể không màu, khó tan trong nước.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án C
(e) Sai, Aminoaxit là tinh thể không màu, dễ tan trong nước.
Câu 34:
Đun nóng 14,8 gam hỗn hợp X gồm (CH3COOCH3, HCOOC2H5, C2H5COOH) trong 100,0 ml dung dịch chứa NaOH 1,0M và KOH aM (phản ứng vừa đủ) thì thu được 4,68 gam hỗn hợp hai ancol (tỷ lệ mol 1: 1) và m gam muối. Vậy giá trị m là:
 Xem đáp án
Xem đáp án
Đáp án A
=> x + y + z = = 0,2 (Do 3 chất cùng PTK)
Mặc khác, => x = y = = 0,06
=> z = 0,08
nNaOH = 0,1 mol => nKOH = x + y + z - 0,1 = 0,1 mol
Bảo toàn khối lượng: mX + mKOH + mNaOH = mmuối + m ancol +
<=> 14,8 + 0,1.(56 + 40) = m + 4,68 + 0,08.18
=> m = 18,28 g
Câu 35:
Đốt cháy hoàn toàn hỗn hợp X gồm 2 amin đều no đơn chức, mạch hở và hơn kém nhau 2 nguyên tử cacbon trong phân tử bằng lượng không khí vừa đủ (O2 chiếm 20% và N2 chiếm 80% về thể tích) thu được hỗn hợp Y gồm CO2, H2O và N2. Dẫn toàn bộ X qua bình dung dịch Ba(OH)2 dư thấy khối lượng bình tăng 21,3 gam; đồng thời khí thoát ra khỏi bình có thể tích 48,16 lít (đktc). Công thức của amin có khối lượng phân tử lớn là
 Xem đáp án
Xem đáp án
Đáp án B
Đốt:
Bảo toàn nguyên tố O có:
Thay ngược lại có nCO2 = 0,3 mol và nE = 2x = 0,1 mol
→ Ctrung bình = 3.
→ Lại thêm giả thiết 2 amin hơn kém nhau 2C → cặp amin này là C2H7N và C4H9N.
Câu 36:
Dẫn từ từ 5,6 lít khí CO2 (đktc) vào 400 ml dung dịch chứa, đồng thời các chất NaOH 0,3M; KOH 0,2M; Na2CO3 0,1875M và K2CO3 0,125M thu được dung dịch X. Thêm dung dịch CaCl2 vào dung dịch X tới dư, số gam kết tủa thu được là
 Xem đáp án
Xem đáp án
Đáp án A
Câu 38:
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch NaOH vào dung dịch Ba(HCO3)2.
(b) Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
(c) Sục khí CO2 tới dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4]).
(d) Cho dung dịch AgNO3 vào dung dịch MgCl2.
(e) Sục khí H2S vào dung dịch FeCl2.
(g) Cho Mg vào dung dịch FeCl3 dư.
Sau khi các phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
 Xem đáp án
Xem đáp án
Đáp án B
Các phương trình phản ứng xảy ra khi tiến hành các thí nghiệm:
(a) 2NaOH + Ba(HCO3)2 → Na2CO3 + BaCO3↓ + 2H2O.
(b) 3NH3 + AlCl3 + 3H2O → Al(OH)3↓ + 3NH4Cl.
(c) CO2 + 2H2O + NaAlO2 → Al(OH)3↓ + NaHCO3.
(d) 2AgNO3 + MgCl2 → 2AgCl↓ + Mg(NO3)2.
(e) H2S + FeCl2 → phản ứng không xảy ra (vì kết tủa FeS tan trong axit HCl).
(g) Mg + 2FeCl3 → MgCl2 + 2FeCl2 (vì FeCl3 dùng dư).
Theo đó, có tất cả 4 thí nghiệm thu được kết tủa khi kết thúc các phản ứng.
Câu 39:
Đốt cháy hoàn toàn m gam hỗn hợp E gồm 3 este X, Y, Z (đều mạch hở và chỉ chứa este, Z chiếm phần trăm khối lượng lớn nhất trong E) thu được lượng CO2 lớn hơn H2O là 0,25 mol. Mặt khác m gam E phản ứng vừa đủ với dung dịch NaOH thu được 22,2 gam 2 ancol hơn kém nhau 1 nguyên tử cacbon và hỗn hợp T gồm 2 muối. Đốt cháy hoàn toàn T cần vừa đủ 0,275 mol O2 thu được CO2, 0,35 mol Na2CO3 và 0,2 mol H2O. Phần trăm khối lượng của Z trong E là
 Xem đáp án
Xem đáp án
Đáp án C
* Bảo toàn Na: nO/T=2nNaOH=0,7 (mol); bảo toàn O:
*
muối gồm HCOONa: a mol và (COONa)2: b mol
Bảo toàn H: a=0,4 (mol)
b=0,15 (mol)
mT=0,4,68+0,15.134=47,3 (gam)
Bảo toàn khối lượng: mE=22,2+47,3-0,7.40=41,5 (gam)
* mE= nC.12+ nH.1+0,7.2.16=41,5; nC -nH/2= 0,25
nC=1,4 (mol); nH=2,3 (mol)
Bảo toàn C: C/ancol=C/E-C/T= 1,4-0,7=0,7 (mol) = nOH/ancol hay ancol no, mạch hở
Bảo toàn H: H/ancol =H/E+H/NaOH-H/T=2,3+0,7-0,2.2= 2,6 (mol)
* CnH2n+2Ox: c mol; Cn-1H2(n-1)+2O; d mol
cn+d(n-1)=0,7; c(2n+2)+d[2(n-1)+2]=2,6
(c+d)=0,6 (mol)
Số C trung bình của ancol là 0,7/0,6=1,33
ancol là CH3OH (0,5 mol) và C2H4(OH)2 (0,1 mol)
* E chứa HCOOCH3(0,2 mol); HCOO-C2H4-OOCH (0,1 mol); Z: (COOCH3)2 (0,15 mol)
%mZ=(0,15.118).100%/(0,2.60+0,1.118+0,15118)= 42,65%
Câu 40:
Hỗn hợp X gồm Al, Mg, FeO, Fe3O4 trong đó oxi chiếm 20,22% khối lượng hỗn hợp. Cho 25,32 gam hỗn hợp X tác dụng với dung dịch HNO3 dư thu được 3,584 lít hỗn hợp khí NO và N2O (đktc) có tỉ khối so với hiđro là 15,875 và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Nung muối khan này trong không khí đến khối lượng không đổi 30,92 gam chất rắn khan. Giá trị gần nhất của m là
 Xem đáp án
Xem đáp án
Đáp án C