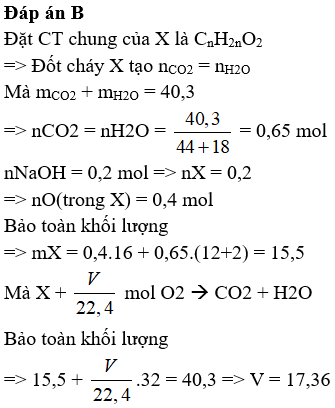30 đề thi THPT Quốc gia môn Hóa năm 2022 có lời giải (Đề số 4)
-
45345 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Thuỷ phân este X trong môi trường kiềm, thu được natri axetat và ancol etylic. Công thức của X là:
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 5:
Phân tử amino axit nào sau đây có hai nhóm amino?
 Xem đáp án
Xem đáp án
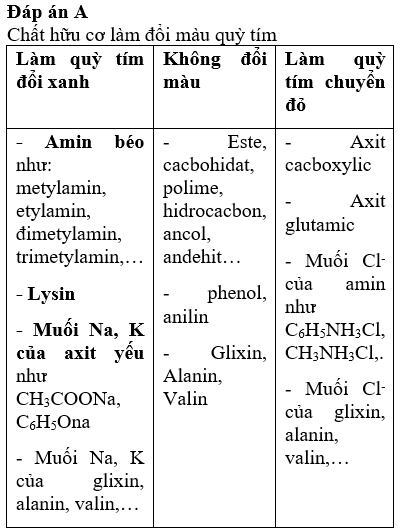
Đáp án A
Cấu tạo phân tử tương ứng của các amino axit:
A. Lysin: H2N–[CH2]4–CH(NH2)COOH.
B. Valin: (CH3)2CHCH(NH2)COOH.
C. Axit glutamic: HOOCCH2CH2CH(NH2)COOH.
D. Alanin: H2NCH(CH3)COOH.
Câu 7:
Kim loại nào sau đây cứng nhất trong các kim loại?
 Xem đáp án
Xem đáp án
Đáp án A
Kim loại cứng nhất: Cr
Kim loại có nhiệt độ nóng chảy cao nhất : W
Kim loại có nhiệt độ nóng chảy thấp nhất : Hg
Kim loại dẻo nhất : Au
Kim loại dẫn điện tốt nhất : Ag
Kim loại có tính nhiễm từ : Fe
Câu 9:
Muốn chuyển hóa những ion kim loại trong hợp chất hóa học thành kim loại ta thực hiện quá trình
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 10:
Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
 Xem đáp án
Xem đáp án
Đáp án D
Ca, Na, Mg chỉ điều chế được bằng phương pháp điện phân nóng chảy
Câu 12:
Kim loại phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 14:
Nung CaCO3 ở nhiệt độ cao, thu được sản phẩm gồm chất rắn X và khí CO2. Chất X là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 15:
Vào mùa lũ, để có nước sử dụng, dân cư ở một số vùng thường sử dụng chất X (Có công thức K2SO4.Al2(SO4)3.24H2O) để làm trong nước. Chất X được gọi là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 18:
Ô nhiễm không khí có thể tạo ra mưa axit, gây ra tác hại rất lớn với môi trường. Hai khí nào sau đây đều là nguyên nhân gây ra mưa axit?
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 19:
Các loại phân lân đều cung cấp cho cây trồng nguyên tố
 Xem đáp án
Xem đáp án
Đáp án A
Phân lân cung cấp nguyên tố photpho
Câu 21:
Cho các este sau: etyl axetat, propyl axetat, metyl propionat, metyl metacrylat. Có bao nhiêu este không no?
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 22:
Thủy phân hoàn toàn hỗn hợp etyl propionat và etyl fomat trong dung dịch KOH, thu được sản phẩm gồm
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 23:
Thủy phân hoàn toàn cacbohiđrat A thu được hai mosaccarit X và Y. Hiđro hóa X hoặc Y đều thu được chất hữu cơ Z. Hai chất A và Z lần lượt là
 Xem đáp án
Xem đáp án
Đáp án D
Saccrarozơ + H2O Glucozơ + Fructozơ
Glucozơ + H2 Sobitol
Fructozơ + H2 Sobitol
Câu 24:
Thủy phân 10,8 gam xenlulozơ trong môi trường axit. Cho sản phẩm tác dụng với AgNO3 dư trong NH3 đun nóng, sau phản ứng hoàn toàn thu được 11,88 gam Ag. Hiệu suất của phản ứng thủy phân là
 Xem đáp án
Xem đáp án
Đáp án D
H = 0,55.162/108 = 82,5%.
Câu 25:
Biết m gam amin X (no, đơn chức, mạch hở) tác dụng vừa đủ với 0,2 mol HCl. Đốt cháy m gam X thu được CO2, H2O và V lít khí N2. Giá trị của V là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 26:
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án C
Tơ nitron được điều chế bằng phản ứng trùng hợp.
Câu 27:
Hòa tan hoàn toàn 13,8 gam hỗn hợp X gồm Al, Fe vào dung dịch H2SO4 loãng, thu được 10,08 lít khí (đktc). Phần trăm về khối lượng của Al trong X là
 Xem đáp án
Xem đáp án
Đáp án C
Câu 28:
Cho m gam Al phản ứng với khí oxi dư, thu được 10,2 gam oxit. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án D
BTNT (Al):
Câu 29:
Cho từ từ Cu dư vào dung dịch X, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y chứa hai muối. Dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 30:
Cho các chất: Fe2O3, FeO, Fe(OH)3, Fe2(SO4)3. Số chất tác dụng với dung dịch HNO3 loãng, dư sinh ra khí NO là
 Xem đáp án
Xem đáp án
Đáp án A
Cho FeO tác dụng với HNO3 sinh khí NO theo phản ứng
3FeO + 10HNO3 3Fe(NO3)3 + NO + 5H2O
Câu 32:
Thực hiện phản ứng phản ứng điều chế isoamyl axetat (dầu chuối) theo trình tự sau:
Bước 1: Cho 2 ml ancol isoamylic, 2 ml axit axetic kết tinh và 2 giọt axit sunfuric đặc vào ống nghiệm.
Bước 2: Lắc đều, đun nóng hỗn hợp 8-10 phút trong nồi nước sôi.
Bước 3: Làm lạnh, rót hỗn hợp sản phẩm vào ống nghiệm chứa 3-4 ml nước lạnh.
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án D
Hỗn hợp sau phản ứng chứa phân thành 2 lớp (isoamyl axetat ở trên), để tách isoamyl axetat từ hỗn hợp thu được ta dùng phương pháp chiết.
Câu 33:
Cho các phát biểu sau:
(a) Thủy phân vinyl axetat bằng NaOH đun nóng, thu được natri axetat và fomanđehit.
(b) Anilin là một bazơ, dung dịch của nó có thể làm quỳ tím chuyển xanh.
(c) Glu–Ala tác dụng với dung dịch HCl theo tỉ lệ mol 1: 2.
(d) Trong một phân tử triolein có 3 liên kết p.
(e) Tinh bột và xenlulozơ là đồng phân của nhau.
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án A
(a) Sai, Thủy phân vinyl axetat bằng NaOH đun nóng, thu được natri axetat và anđehit axetic.
(b) Sai, Anilin là một bazơ yếu, dung dịch của nó không làm quỳ tím chuyển xanh.
(d) Sai, Trong một phân tử triolein có 6 liên kết p.
(e) Sai, Tinh bột và xenlulozơ không là đồng phân của nhau.
Câu 35:
Đốt cháy hoàn toàn 0,3 mol hỗn hợp X gồm propilen và 2 amin no mạch hở đồng đẳng kế tiếp trong oxi dư thu được 16,8 lít CO2, 2,016 lít N2 (đktc) và 16,74 gam H2O. Khối lượng của amin có khối lượng mol phân tử nhỏ hơn là
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 36:
Cho 3,36 lít khí CO2 (đktc) vào 400 ml dung dịch hỗn hợp KOH 0,25M và K2CO3 0,4M thu được dung dịch X. Cho dung dịch BaCl2 dư vào dung dịch X thu được kết tủa, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là:
 Xem đáp án
Xem đáp án
Đáp án C
Câu 37:
Hòa tan hết m gam hỗn hợp X gồm Na, Na2O, K, K2O, Ba và BaO, trong đó oxi chiếm 8,75% về khối lượng vào nước thu được 400 ml dung dịch Y và 1,568 lít H2 (đktc). Trộn 200 ml dung dịch Y với 200 ml dung dịch hỗn hợp gồm HCl 0,2M và H2SO4 0,15M thu được 400 ml dung dịch có pH = 13. Các phản ứng xảy ra hoàn toàn. Giá trị m gần giá trị nào nhất sau đây?
 Xem đáp án
Xem đáp án
Đáp án B
Câu 38:
Thực hiện các thí nghiệm sau:
(a) Cho dung dịch HCl dư vào ống nghiệm chứa dung dịch NaAlO2.
(b) Dẫn khí CO2 dư vào ống nghiệm chứa dung dịch NaAlO2.
(c) Cho dung dịch Ba(OH)2 dư vào ống nghiệm chứa dung dịch Al2(SO4)3.
(d) Cho dung dịch NH3 dư vào ống nghiệm chứa dung dịch Al2(SO4)3.
(e) Cho dung dịch AlCl3 dư vào ống nghiệm chứa dung dịch NaOH.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được kết tủa là
 Xem đáp án
Xem đáp án
Đáp án D
Các phản ứng xảy ra khi tiến hành các thí nghiệm (với điều kiện tương ứng) là:
☒ (a) 4HCl + NaAlO2 → NaCl + AlCl3 + 2H2O.
☑ (b) CO2 + NaAlO2 + H2O → Al(OH)3↓ + NaHCO3.
☑ (c) 4Ba(OH)2 + Al2(SO4)3 → Ba(AlO2)2 + 3BaSO4↓ + 4H2O.
☑ (d) 6NH3 + Al2(SO4)3 + 6H2O → 2Al(OH)3↓ + 3(NH4)2SO4.
☑ (e) AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl.
Theo đó, cuối cùng khi kết thúc các phản ứng có 4 thí nghiệm thu được kết tủa.
Câu 40:
Hòa tan 17,32 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 cần vừa đúng dung dịch hỗn hợp gồm 1,04 mol HCl và 0,08 mol HNO3, đun nhẹ thu được dung dịch Y và 2,24 lít hỗn hợp khí Z (đktc) có tỉ khối hơi đối với H2 là 10,8 gồm hai khí không màu trong đó có một khí hóa nâu ngoài không khí. Cho dung dịch Y tác dụng với một lượng dung dịch AgNO3 vừa đủ thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa nung đến đến khối lượng không đổi thu được 20,8 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án A