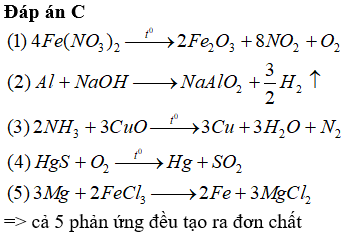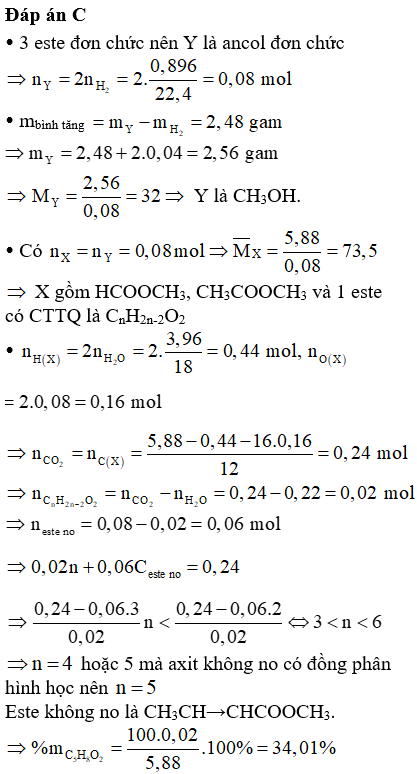30 đề thi THPT Quốc gia môn Hóa năm 2022 có lời giải (Đề số 27)
-
45512 lượt thi
-
40 câu hỏi
-
50 phút
Danh sách câu hỏi
Câu 1:
Đun nóng este CH3COOC2H5 với một lượng vừa đủ dung dịch NaOH, sản phẩm thu được là
 Xem đáp án
Xem đáp án
Đáp án B
PTHH: CH3COOC2H5 + NaOH → CH3COONa + C2H5OH
Câu 6:
Polime X là chất rắn trong suốt, có khả năng cho ánh sáng truyền qua tốt nên được dùng chế tạo thủy tinh hữu cơ plexiglas. Tên gọi của X là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 7:
Cho dãy các kim loại: Cs, Cr, Rb, K. Ở điều kiện thường, kim loại cứng nhất trong dãy là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 9:
Sự phá hủy bề mặt kim loại hoặc hợp kim do tác dụng của các chất trong môi trường là
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 10:
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện?
 Xem đáp án
Xem đáp án
Đáp án B.
Câu 11:
Dãy gồm các kim loại đều tác dụng được với dung dịch HCl nhưng không tác dụng với dung dịch HNO3 đặc, nguội là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 12:
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường, tạo ra dung dịch có môi trường kiềm là
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 13:
Ở nhiệt độ thường, kim loại X không tan trong nước nhưng tan trong dung dịch kiềm. Kim loại X là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 18:
Ở trạng thái rắn, hợp chất X tạo thành một khối trắng gọi là “nước đá khô”. Nước đá khô không nóng chảy mà thăng hoa, được dùng để tạo môi trường lạnh không có hơi ẩm. Chất X là
 Xem đáp án
Xem đáp án
Đáp án A.
Câu 22:
Este X có CTPT là C3H6O2, có khả năng tham gia phản ứng tráng bạc. Công thức cấu tạo của X là
 Xem đáp án
Xem đáp án
Đáp án D.
Câu 24:
Thực hiện phản ứng tráng gương 36 gam dung dịch fructozơ 10% với lượng dung dịch AgNO3 trong NH3, nếu hiệu suất phản ứng 40% thì khối lượng bạc kim loại thu được là
 Xem đáp án
Xem đáp án
Đáp án C
Ta có:
Câu 25:
Đốt cháy hoàn toàn 0,2 mol một amin no, mạch hở, đa chức X bằng oxi vừa đủ thu được 1,2 mol hỗn hợp Y gồm khí và hơi. Cho 6,1 gam X tác dụng vừa đủ với V lít dung dịch HCl 2M. Giá trị của V là:
 Xem đáp án
Xem đáp án
Đáp án A
Dồn X về
Vậy amin phải là: lít
Câu 26:
Phát biểu nào sau đây đúng?
 Xem đáp án
Xem đáp án
Đáp án C
A sai vì amilozơ có cấu trúc mạch không phân nhánh
B sai vì Poliacrylonitrin được điều chế bằng phản ứng trùng hợp
D sai vì Poli(vinyl clorua) được điều chế bằng phản ứng trùng hợp vinyl clorua.
Câu 27:
Hoà tan hoàn toàn 2,43 gam hỗn hợp Mg và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng, sau phản ứng thu được 1,12 lít H2 (đktc) và dung dịch X. Khối lượng muối trong dung dịch X là
 Xem đáp án
Xem đáp án
Đáp án A
Ta có:
gam
Câu 28:
Hòa tan hết 3,24 gam kim loại X trong 100 ml dung dịch NaOH 1,5M thu được 4,032 lít H2 (đktc) và dung dịch Y. Kim loại X là
 Xem đáp án
Xem đáp án
Đáp án C
Kim loại X hóa trị n, bảo toàn electron:
=>X là Al.
Câu 29:
Thí nghiệm nào sau đây thu được muối sắt (II) sau khi kết thúc phản ứng?
 Xem đáp án
Xem đáp án
Đáp án B
Các phản ứng hóa học xảy ra khi tiến hành các thí nghiệm:
A. Fe + 4HNO3 dư → Fe(NO3)3 + NO + 2H2O.
B. Fe + 2FeCl3 → 3FeCl2.
C. Fe + HNO3 → Fe(NO3)3 + NO2 + H2O.
FeO + HNO3 → Fe(NO3)3 + NO2 + H2O.
D. Fe + 3AgNO3 dư → Fe(NO3)3 + 3Ag↓.
Câu 30:
Phản ứng nào sau đây chứng minh hợp chất sắt (III) có tính oxi hóa?
 Xem đáp án
Xem đáp án
Đáp án C
2FeCl3 + Mg 2FeCl2 + Mg
Số oxi hóa của sắt giảm từ +3 xuống +2 => FeCl3 thể hiện tính oxi hóa
Câu 31:
Hỗn hợp X gồm 2 triglixerit A và B (MA<MB; tỉ lệ số mol tương ứng là 12:13). Đun nóng m gam hỗn hợp X với dung dịch KOH vừa đủ thu được dung dịch chứa glixerol và hỗn hợp gồm x gam kali oleat, y gam kali linoleat và z gam kali panmitat, m gam hỗn hợp X tác dụng tối đa với 198,4 gam brom. Đốt m gam hỗn hợp X thu được 616 lít CO2 và 454,68 gam H2O. Giá trị của x+z là:
 Xem đáp án
Xem đáp án
Đáp án B
Ta có:
Xem như hidro hóa X rồi đốt cháy
Câu 32:
Tiến hành thí nghiệm điều chế xà phòng theo các bước sau đây:
Bước 1. Cho vào bát sứ nhỏ 1ml dầu ăn và 3ml dung dịch NaOH 40%
Bước 2. Đun sôi hỗn hợp nhẹ và liên tục khuất đều bằng đũa thủy tinh khoảng 8-10 phút. Tỉnh thoản thêm vài giọt nước để giữ thể tích hỗn hợp không đổi.
Bước 3. Rót them vào hỗn hợp 4-5 ml dung dịch NaCl bão hòa nóng, khuấy nhẹ, sau đó để nguội.
Phát biểu nào sau đây sai?
 Xem đáp án
Xem đáp án
Đáp án D
D sai vì sau bước 3, khi để nguội thấy có phần chất rắn màu trắng đục nổi lên trên.
Câu 33:
Cho các phát biểu sau:
(a) Thủy phân vinyl axetat bằng NaOH đun nóng, thu được natri axetat và axetanđehit.
(b) Polietilen được điều chế bằng phản ứng trùng ngưng etilen.
(c) Ở điều kiện thường, anilin là chất lỏng.
(d) Xenlulozo thuộc loại polisaccarit.
(e) Thủy phân hoàn toàn abumin, thu được các α-amino axit.
(g) Tripanmitin có tham gia phản ứng cộng H2 (Ni, to).
Số phát biểu đúng là
 Xem đáp án
Xem đáp án
Đáp án C
a) đúng CH3COOCH=CH2 + NaOH → CH3COONa + CH3-CHO
b) sai Polietilen được điều chế bằng phản ứng trùng hợp etilen.
c) đúng
d) đúng
e) đúng
g) sai
=> có 4 đáp án đúng
Câu 34:
Hỗn hợp E chứa 1 axit cacboxylic, 1 ancol no Y và 1 este Z (X, Y, Z đều đơn chức, mạch hở). Đun nóng 11,28 gam E với 100ml dung dịch NaOH 1M vừa đủ thu được 9,4 gam 1 muối và hỗn hợp 2 ancol cùng dãy đồng đẳng kế tiếp. Mặt khác đốt cháy 11,28 gam E cần dùng 0,66 mol O2. Phần trăm số mol của Y có trong E là?
 Xem đáp án
Xem đáp án
Đáp án D
Ta có:
Tách axit, este có 1 liên kết đôi C=C, mạch hở thành ; ancol Y tách thành
Câu 35:
Trộn 3 thể tích khí O2 với 2 thể tích khí O3 thu được hỗn hợp khí X. Để cháy hoàn toàn 14,2 gam hỗn hợp khí Y gồm metylamin, amoniac và hai anken cần dùng vừa đủ 22,4 lít khí X (ở đktc), sau phản ứng thu được hỗn hợp Z gồm CO2, H2O, N2. Dẫn toàn bộ Z qua dung dịch Ba(OH)2 dư thì khối lượng kết tủa thu được là
 Xem đáp án
Xem đáp án
Đáp án A
22,4 lít X ↔ 1 mol X có 0,6 mol O2 và 0,4 mol O3 quy ra 2,4 mol O để đốt.
Hỗn hợp Y: metylamin = CH2 + NH3; amoniac = NH3 và hai anken (CH2)n
→ Quy đổi Y
Đốt 14,2 gam Y gồm {x mol CH2 và y mol NH3} + 2,4 mol O → CO2 + H2O + N2.
Có hệ: mY = 14x + 17y = 14,2 gam; lượng O cần đốt: 3x + 1,5y = 2,4
suy ra x = 0,65 mol và y = 0,3 mol → nCO2 = 0,65 mol
Theo đó, yêu cầu giá trị m↓ BaCO3 = 0,65 × 197 = 128,05 gam.
Câu 36:
Dung dịch X gồm NaOH x mol/l và Ba(OH)2 y mol/l và dung dịch Y gồm NaOH y mol/l và Ba(OH)2 x mol/l. Hấp thụ hết 0,04 mol CO2 vào 200 ml dung dịch X, thu được dung dịch M và 1,97 gam kết tủa. Nếu hấp thụ hết 0,0325 mol CO2 vào 200 ml dung dịch Y thì thu được dung dịch N và 1,4775 gam kết tủa. Biết hai dung dịch M và N phản ứng với dung dịch KHSO4 đều sinh ra kết tủa trắng, các phản ứng đều xảy ra hoàn toàn. Giá trị của x và y lần lượt là
 Xem đáp án
Xem đáp án
Đáp án B
Câu 37:
Cho 1,792 lít O2 tác dụng hết với hỗn hợp X gồm Na, K và Ba thu được hỗn hợp rắn Y chỉ gồm các oxit và các kim loại dư. Hòa tan hết toàn bộ Y vào H2O lấy dư, thu được dung dịch Z và 3,136 lít H2. Cho Z tác dụng với lượng dư dung dịch NaHCO3, thu được 39,4 gam kết tủa. Mặt khác, hấp thụ hoàn toàn 10,08 lít CO2 vào dung dịch Z, thu được m gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án C.
Câu 40:
Cho 15,44 gam hỗn hợp rắn X gồm Mg, Fe3O4 và Cu(NO3)2 vào dung dịch chứa 0,61 mol HCl và 0,01 mol HNO3, đun nóng sau khi kết thúc phản ứng phản ứng thu được 0,06 mol hỗn hợp khí gồm NO và H2 (tỷ lệ mol tương ứng 2:1) và dung dịch Y chỉ chứa m gam muối (không có muối Fe2+). Giá trị của m là
 Xem đáp án
Xem đáp án
Đáp án B
Gọi